AOE-P04-M-04
-
Upload
sergio-herrera -
Category
Documents
-
view
240 -
download
0
Transcript of AOE-P04-M-04
EJECUTOR
INSTITUTO NACIONAL DE CANCEROLOGA E.S.E.CDIGO: AOE-P04-M-04
ATENCIN ONCOLGICA ESPECFICAVERSIN: 01
MANUAL DE CONTROL DE CALIDAD RADIOFARMACIA-VIGENCIA: 23-07-2013
Pgina 1 de 3
INSTITUTO NACIONAL DE CANCEROLOGA ESECDIGO: AOE-P04-M-04
ATENCIN ONCOLGICA ESPECFICAVERSIN: 01
MANUAL DE CONTROL DE CALIDAD RADIOFARMACIA-VIGENCIA: 23-07-2013
Pgina 2 de 2
MANUAL DE CONTROL DE CALIDAD RADIOFARMACIA-ATENCIN ONCOLGICA ESPECFICAELABORADO POR: QUMICOS FARMACUTICOS
RADIOFARMACIAINSTITUTO NACIONAL DE CANCEROLOGA ESE
2013TABLA DE CONTENIDO
41.CONTROL DE CALIDAD FISICOQUMICO
41.1. OBJETIVO
41.2. DESCRIPCIN
41.3. EQUIPOS
41.4. INSUMOS
41.5. PROCEDIMIENTO
61.6. NO CONFORMIDADES
62.CONTROL DE CALIDAD RADIOACTIVO
62.1.OBJETIVO
62.2.DESCRIPCIN
72.3.EQUIPOS
72.4.INSUMOS
72.5.PROCEDIMIENTO
72.5.1.Preparacin de la Muestra
82.5.2.Cromatografa en Capa Delgada
82.5.3.Cromatografa con Minicolumnas Cromatogrficas SEP-PACK
132.6DETERMINACIN DE LA PUREZA RADIONUCLIDICA
132.6.1 Determinacin de Molibdeno
142.7NO CONFORMIDADES
143.CONTROL DE CALIDAD MICROBIOLGICO
143.1.OBJETIVO
143.2.DESCRIPCIN
143.3.EQUIPOS
143.4.INSUMOS
153.5.PROCEDIMIENTO
153.5.1.Prueba de Esterilidad
163.5.2.Control Microbiolgico de reas
163.5.2.1.Ambientes
173.5.2.2.Superficies
183.5.3.Control microbiolgico de personal
183.5.4.Test de Llenado escptico
193.6.PRUEBA DE ENDOTOXINAS
203.7.NO CONFORMIDADES
204. CONTROL DE CALIDAD BIOLGICO
204.1. OBJETIVO
204.2. DESCRIPCIN
204.3. EQUIPOS
214.4. INSUMOS
214.5. PROCEDIMIENTO
214.5.1. Unin a Protenas
224.6. BIODISTRIBUCIN
224.7 NO CONFORMIDADES
235.CRITERIOS DE ACEPTACIN
286.MANEJO DE DESVIACIONES
296.1.ACCIONES A TOMAR FRENTE A DESVIACIONES ASOCIADAS A LOS PROCESOS DE ADECUACIN DE MEDICAMENTOS
327.DETERMINACIN DE PUREZA RADIOQUMICA POR HPLC
327.1 DETERMINACIN DE PUREZA RADIOQUIMCA PARA 99mTc-HYNIC-TOC
327.1.1 MTODO 1:
327.1.2 MTODO 2:
337.2 DETERMINACIN DE PUREZA RADIOQUIMICA PARA 177Lu-DOTATATE
337.2.1 MTODO 1:
347.3 CONTROL DE CALIDAD DE CPSULAS DE YODO 131 (131I)
358.ESTABILIDAD DE RADIOFRMACOS
358.1. FRACCIONAMIENTO DE KITS
1. CONTROL DE CALIDAD FISICOQUMICOResponsable: Qumico Farmacutico de Control de Calidad.
1.1. OBJETIVO
Asegurar que los radiofrmacos cumplan con todos los requerimientos y especificaciones fisicoqumicas establecidas.
1.2. DESCRIPCIN
El anlisis fisicoqumico de los radiofrmacos es un mtodo esencial para la determinacin de la pureza e integridad de los compuestos. Permiten caracterizar cada uno de los radiofrmacos de acuerdo a sus propiedades fsicas y dan un indicio de la cantidad y tipo de impurezas que puedan tener.
1.3. EQUIPOS
Cabina de Flujo laminar blindada
Detector de superficies
Balanza analtica
1.4. INSUMOS
Fondo negro
Fondo blanco
Papel tornasol para pH
Oxido de Aluminio
Amarillo de Alizarina
Portafiltro o soportes de membrana
Filtros de membrana de 8mm, 5mm y 3mm.
Etanol 70%
Etiquetas, bolgrafo
Viales estriles, apirgenos y al vaco (de 2 a 5 segn el nmero de alcuotas a obtener)
Contenedores de plomo para viales (de acuerdo al nmero de viales)
Pinzas para viales
1.5. PROCEDIMIENTO
APARIENCIA
Tome en una jeringa de 1mL, aproximadamente 0,2mL de la solucin de radiofrmaco a analizar.
Observe a travs del vidrio plomado y utilizando un fondo negro, la presencia o ausencia de partculas extraas blancas en la solucin.
Realice el mismo procedimiento observando a travs del vidrio plomado, pero utilizando un fondo blanco, la presencia o ausencia de partculas extraas oscuras en la solucin.
Registre su apreciacin en los diferentes formatos de Control de calidad de Radiofrmacos AOE-P04-F-08 AOE-P08-F-08Control de Calidad de Generadores de Radionclidos, AOE-P04-F-20 Control de Calidad de Kits de HYNIC-TOC Radiofarmacia, AOE-P04-F-24 Control de Calidad De Kits de Coloide de Estao Radiofarmacia, de acuerdo a la muestra a analizar.
Realice el mismo procedimiento observando a travs del vidrio plomado, pero utilizando un fondo blanco, la presencia o ausencia de partculas extraas oscuras en la solucin.
Ninguna muestra de radiofrmacos puede contener cualquier material particulado, oscuro. La presencia de partculas extraas es un indicio de contaminacin del producto y por lo tanto se considera un material rechazado.
PH Tome en una jeringa de 1mL, 0,2ml de muestra del radiofrmaco a analizar.
Coloque una gota de la muestra sobre el papel tornasol seleccionado para medir el rango de pH deseado.
Compare el color obtenido en la tira con la tabla de pH que trae anexa la caja de empaque del papel tornasol.
Registre los resultados en los formatos de Control de Calidad de cada radiofrmaco. AOE-P04-F-08 AOE-P08-F-08Control de Calidad de Generadores de Radionclidos, AOE-P04-F-17 Certificado Final de Control de Calidad, AOE-P04-F-20 Control de Calidad de Kits de HYNIC-TOC Radiofarmacia, AOE-P04-F-24 Control de Calidad De Kits de Coloide de Estao Radiofarmacia, AOE-P04-F-11 Control de Calidad de Radiofrmacos.
El pH ideal de un radiofrmaco debe ser 7. Generalmente es tolerado un rango entre 5 8.
DETERMINACIN DE ALUMINIO
Tome una tira de papel reactivo y colquele una gota del patrn de aluminio con el que viene el KIT y una gota de muestra del generador y compare la coloracin segn la tabla siguiente:
COLORINTERPRETACIN
Rosado AmarillentoAluminio menor de 10 g/mL
RosadoAluminio mayor de 10 g/mL
TAMAO DE PARTCULA
Prepare una muestra tomando 100L (0,1 mL en una jeringa de 1mL) de la solucin de coloide marcada y complete a 2mL con solucin salina normal o agua estril para inyeccin en una jeringa de 3mL.
Arme una batera de filtros, verificando previamente que cada portafiltro o soporte de membrana se encuentre limpio. Coloque cada filtro (8mm, 5mm y 3mm) dentro del portafiltro respectivo, manipulndolos con una pinza para evitar su contaminacin. Coloque el empaque de caucho encima de la membrana y cierre el portafiltro. Arme cada soporte, colocando el filtro ms grande primero, y de arriba hacia abajo hasta armar el ms pequeo.
Coloque un vial limpio, sin agrafe y sin tapn en el puerto de salida del portafiltro que contiene el filtro de 3mm, para recibir la muestra.
Tome la jeringa de 3 mL en la que est disuelto el radiofrmaco y pase la muestra por la batera de filtros a una velocidad de 4-5 gotas por segundo.
Pase mnimo 5mL de aire a travs de la batera y recoja el filtrado. Verifique el volumen de esta solucin y de ser necesario inyecte ms aire para presionar el paso de toda la muestra a travs de la batera de filtros.
Desarme con cuidado la batera de filtros.
Coloque cada portafiltros o soporte de membrana dentro de una bolsa plstica o envulvalo en una toalla adsorbente para realizar la medicin de la actividad.
Mida la actividad en el Activmetro.
La mayor cantidad de partculas se encontrar en el filtro que mayor actividad registre. Calcule el % de cada filtro y registre en el formato respectivo.
Si el radiofrmaco es para distribucin externa una vez realizados todos los controles de calidad requeridos segn el radiofrmaco, diligenciar el formato AOE-P04-F-17 Certificado Final de Control de Calidad1.6. NO CONFORMIDADES
Si el producto no cumple uno o ms criterios de aceptacin se debe: Repetir la prueba de control de calidad:
Si el producto no cumple el criterio evaluado se notificar al farmacutico supervisor de Control de Calidad y al Farmacutico Director Tcnico quienes sern responsables de la decisin final.
Si el producto cumple el criterio evaluado se debe repetir la prueba de control de calidad por tercera vez y se notificar al farmacutico supervisor de Control de Calidad y al Farmacutico Director Tcnico quienes sern responsables de la decisin final.
2. CONTROL DE CALIDAD RADIOACTIVO
Responsable: Qumico Farmacutico de Control de Calidad.2.1. OBJETIVO
Determinar la pureza e identidad radionucldica y radioqumica de los radiofrmacos preparados en la Radiofarmacia, asegurando que la(s) sustancia(s) qumica no deseada permanezca por debajo de los limites aprobados.
2.2. DESCRIPCIN
La determinacin de la pureza radionucldica me permite definir la identidad y pureza de los radiofrmacos obtenidos. Dichas impurezas pueden ser el resultado de una separacin incompleta de radioistopos, as como el resultado de impurezas propias de las reacciones nucleares, que ocasionan biodistribuciones diferentes, aumento de dosis de radiacin interna e interferencias con los estudios. La pureza radioqumica es generalmente analizada por tcnicas cromatogrficas como cromatografa de capa delgada, cromatografa en columna y HPLC.
2.3. EQUIPOS
Mdulo de extraccin para control de calidad
Secador
Contador Ludlum Pozo
Sonda Captus
2.4. INSUMOS
Probetas o recipientes para cromatografa de 15cm de altura.
Tiras de papel o de aluminio para cromatografa: papel whatman 3mm (W3), slica gel (SG) y solvent saturation pads (SSP)) de 1 cm x 10 cm.
Acetona (ACE).
Metiletilcetona (MEC).
Solucin salina 0,9% (SSN).
Metanol 85% (MET).
Etanol (ETO).
Acetonitrilo (ACN).
Amoniaco (NH3).
Suero fetal bovino (PBS).
Tetrahidrofurano (THF).
Cloroformo (CLF).
Minicolumnas cromatogrficas de Sep-pack.
Lpiz.
Marcador de tinta.
Tijeras.
Pinzas.
Contenedor de plomo para residuos.
Tubos de ensayo.
Etanol 70%
Etiquetas.
Bolgrafo.2.5. PROCEDIMIENTO
DETERMINACIN DE LA PUREZA RADIOQUMICA
2.5.1. Preparacin de la Muestra
Despus del tiempo de incubacin para la radiomarcacin, tome una muestra no mayor a 0.1mL del radiofrmaco en una jeringa de 1 mL. Entregue al Farmacutico de Control de Calidad para su anlisis.
Mida la actividad de la muestra en el Activmetro.
Coloque el volumen suficiente de solucin salina o agua estril para asegurarse de tener una concentracin final.
2.5.2. Cromatografa en Capa Delgada
Seleccione el sistema solvente para el radiofrmaco a analizar y de acuerdo a la Tabla 1. Informacin para realizar la pureza radioqumica de radiofrmacos.
Coloque 0,5mL del solvente seleccionado en un recipiente o probeta para cromatografa, de forma que alcance una altura de 2mm, desde el fondo del recipiente. Tape el recipiente para evitar la evaporacin del solvente y marque el recipiente con el nombre del solvente que contiene y si es el caso con la concentracin.
Tome una o ms tiras para cromatografa de acuerdo al radiofrmaco a analizar y de acuerdo a la Tabla N 1. Informacin para realizar la pureza radioqumica de radiofrmacos.
Marque con un lpiz, a 1 cm del borde superior de la tira y a 1cm del borde inferior donde se realizar la siembra de la muestra. Con una pipeta de precisin de 0,1L, tome 0.2 L de la muestra y simbrela sobre la tira de cromatografa en el punto de origen del recorrido, a un cm del borde inferior.
Coloque la tira de cromatografa lenta y suavemente dentro de la probeta o recipiente para cromatografa y tpela. Verifique que el lquido quede por debajo del punto de siembra.
Djela el tiempo necesario hasta que el solvente alcance la marca del final del recorrido.
Retire la tira del recipiente, squela y crtela por cada una de las marcas de 1 cm. Coloque cada segmento dentro de un tubo de ensayo limpio y descontaminado, debidamente identificado.
Mida la actividad de cada uno de los segmentos en el contador de pozo.
Realice los clculos respectivos y determine el porcentaje de radiofrmaco marcado.
Registre los resultados en los formatos AOE-P04-F-08 AOE-P08-F-08Control de Calidad de Generadores de Radionclidos y AOE-P04-F-11 Control de Calidad de Radiofrmacos.2.5.3. Cromatografa con Minicolumnas Cromatogrficas SEP-PACK
Tome una columna cromatogrfica tipo Sep-pack C18. Active la columna haciendo pasar 5-10mL de etanol
Con una jeringa de 5 mL tome 3 mL del solvente de acuerdo al radiofrmaco a analizar y de acuerdo a la Tabla N 1. Informacin para realizar la pureza radioqumica de radiofrmacos, y en la que estn disueltos 2uL del radiofrmaco y pselos por la columna una velocidad de 4-5 gotas por segundo, pase luego 3mL de aire a travs de la columna y recoja el eludo en un tubo de ensayo marcndolo como solucin A. Tome 5 mL Tome 5 mL del solvente B y pselo por la columna a una velocidad de 4-5 gotas por segundo, pase luego 3mL de aire a travs de la columna y recoja el eludo en un tubo de ensayo marcndolo como solucin B.
Ponga la columna en una bolsa plstica.
Determine la actividad de 2uL de la solucin A, 2uL de la solucin B y de la columna, midindolas en el contador de pozo.
Realice los clculos respectivos teniendo en cuenta la dilucin y determine el porcentaje de radiofrmaco marcado.
Registre los resultados en el formato AOE-P04-F-11 Control de Calidad de Radiofrmacos.TABLA N 1. INFORMACIN PARA REALIZAR LA PUREZA RADIOQUIMICA DE RADIOFRMACOS
FrmacoCROMATOGRAFA 1CROMATOGRAFA 2RPOBSERVACIONES
99mTcSOPORTESOLVENTENA> 95%Radiofrmaco estable 6 h.
SGSSN
RESULTADO
RF0RF0,3-0,4RF1
99mTc HR99Mo99mTc libre
99mTc-DTPASOPORTESOLVENTESOPORTESOLVENTE> 90%Radiofrmaco estable 6 h.
SG o W 1ACE o MECSGSSN
RESULTADORESULTADO
RF0RF1RF0RF1
99mTc-DTPA + 99mTc HR99mTc libre99mTc HR99mTc-DTPA + 99mTc libre
99mTc-DMSASOPORTESOLVENTESOPORTESOLVENTE> 90%Radiofrmaco estable 6 h.
SG o W 1ACE o MECSGSSN
RESULTADORESULTADO
RF0RF1RF0RF1
99mTc-DMSA + 99mTc HR99mTc libre99mTc HR99mTc-DMSA + 99mTc libre
99mTc-MAG3SOPORTESOLVENTE> 90%Radiofrmaco estable 6 h.
SepPack C-18ETOH/SSN1:1 Y 0.001N HCL
RESULTADO
A:
0.001N HCLB:
ETOH/SSN1:1Columna
99mTc libre
99mTc otras99mTc- MAG399mTc HR
99mTc-MDP
99mTc-HDPSOPORTESOLVENTESOPORTESOLVENTE> 90%Radiofrmaco estable 6 h.
SG o W3ACE o MECSG o WSSN
RESULTADORESULTADO
RF0RF1RF0RF1
99mTc-MDP + 99mTc HR99mTc libre99mTc HR99mTc-MDP + 99mTc libre
99mTc- MEBROFENINSOPORTESOLVENTESOPORTESOLVENTE> 90%Radiofrmaco estable 6 h.
SGACN/H2O 60/40SGSSN 2EQ/mL
RESULTADORESULTADO
RF0RF 0.7-1RF0RF1
99mTc HR99mTc-MFENIN + 99mTc libre
99mTc-MFENIN + 99mTc HR99mTc libre
99mTc-ANTI-CEA
SOPORTESOLVENTESOPORTESOLVENTE> 90%Radiofrmaco estable 6 h.
*Embebidas en albmina al 5%.
SGSSNSGACE
RESULTADORESULTADO
RF0RF1RF0RF1
99mTc-AcMo + 99mTc HR99mTc-MDP + 99mTc libre99mTc-AcMo + 99mTc-MDP+99mTc HR
99mTc libre
CROMATOGRAFA 3NA
SOPORTESOLVENTE
SG*ETO/NH3/H2O 2/1/5
RESULTADO
RF0RF0,3-0,8RF1
99mTc HR99mTc-AcMo99mTc-MDP + 99mTc libre
99mTc-HMPAOSOPORTESOLVENTESOPORTESOLVENTE> 90%Es necesario realizar las 3 cromatografas para el anlisis del radiofrmaco.
Radiofrmaco estable 30 min.
SGMECSGSSN
RESULTADORESULTADO
RF0RF1RF0RF1
99mTc-HMPAOsec + 99mTc HR99mTc-HMPAOlipo + 99mTc libre99mTc-HMPAOlipo + 99mTc-HMPAOsec + 99mTc HR99mTc libre
CROMATOGRAFA 3NA
SOPORTESOLVENTE
W1ACN/SSN 1/1
RESULTADO
RF0RF1
99mTc HR99mTc-HMPAOlipo + 99mTc-HMPAOsec + 99mTc libre
99mTc-MAASOPORTESOLVENTENA> 90%Radiofrmaco estable 6 h.
SGMET/H2O 85/15
RESULTADO
RF0RF1
99mTc-MAA + 99mTc HR99mTc libre
99mTc-FITATO COLOIDALSOPORTESOLVENTENA> 90%Radiofrmaco estable 6 h.
SG o W 1ACE o MEC
RESULTADO
RF0RF1
99mTc-Fitato + 99mTc HR99mTc libre
99mTc-ESTAO COLOIDAL SOPORTESOLVENTENA> 90%Radiofrmaco estable 6 h.
SG SSN
RESULTADO
RF0RF1
99mTc-Sn + 99mTc HR99mTc libre
99mTc-NANO-COLOIDESOPORTESOLVENTENA> 95%Radiofrmaco estable 4 h.
W1MET/H2O 85/15
RESULTADO
RF0-0.7RF0.7-1
99mTc-Nanocoloide99mTc libre
99mTc -MIBISOPORTESOLVENTESOPORTESOLVENTE> 90%La cromatografa 2 se realiza cuando no se puede realizar la cromatografa 1.
Radiofrmaco estable 6 h.
Oxido de AluminioEtanol 100%
SepPack C-18SSN Y ETO
RESULTADORESULTADO
RF0RF1A:
SSNB:
ETOHColumna
99mTc libre + 99mTc HR
99mTc-MIBI99mTc libre99mTc-MIBI99mTc HR
99mTc-HYNIC-TOCSOPORTESOLVENTESOPORTESOLVENTE> 90%Es necesario realizar las 3 cromatografas para el anlisis del pptido.
Radiofrmaco estable 6 h.
SG W3MECSGPBS
RESULTADORESULTADO
RF0RF1RF0RF1
99mTc-HYNIC + 99mTc-Tricina/EDDA + 99mTc HR
99mTc libre99mTc-HYNIC + 99mTc HR99mTc libre + 99mTc-Tricina/EDDA
CROMATOGRAFA 3NA
SOPORTESOLVENTE
SG o W3ACN/H2O 1/1
RESULTADO
RF0RF1
99mTc HR99mTc-HYNIC + 99mTc-Tricina/EDDA + 99mTc libre
177Lu-DOTATATESOPORTESOLVENTENA> 95%Radiofrmaco estable 72 h.
SepPack C-18Acetato Na 0.4M Y MET
RESULTADO
Acetato Na
0.4MMETColumna
177Lu libre177Lu-DOTATATE177Lu HR
188ReSOPORTESOLVENTENA> 90%Radiofrmaco estable 12 h.
SG o W3SSN
RESULTADO
RF0RF1
188Re HR188Re libre
188Re-HEDPSOPORTESOLVENTESOPORTESOLVENTE> 90%Radiofrmaco estable 12 h.
SG o W3ACESG o W3SSN
RESULTADORESULTADO
RF0RF1RF0RF1
188Re-HEDP + 188Re HR188Re libre188Re HR188Re-HEDP + 188Re libre
188Re-ESTAO COLOIDALSOPORTESOLVENTENA> 95%Radiofrmaco estable 12 h.
SG W3SSN
RESULTADO
RF0RF1
188Re-Sn + 188Re HR188Re libre
99mT -PIROFOSFATO
SOPORTESOLVENTESOPORTESOLVENTE> 90%Radiofrmaco estable 4h
SG o W3ACE o MECSGSSN
RESULTADORESULTADO
RF0RF1RF0RF1
99mTc-PIROFOSFATO + 99mTc HR99mTc libre99mTc HR99mTc-PIROFOSFATO + 99mTc libre
SG: SILICA GEL 60, W3: WAHTMAN 3, W1: WATHMAN 1: ACE: ACETONA, ACN: ACETONITRILO,
MET: METANOL, ACETATO Na: ACETATO DE SODIO, MEC: METIL-ETIL-CETONA, ETOH: ETANOL
2.6 DETERMINACIN DE LA PUREZA RADIONUCLIDICA
2.6.1 Determinacin de Molibdeno
Asigne una muestra de las eluciones realizadas el primer da, del Generador de Tc99m para realizar el ensayo de Molibdeno.
Mida la actividad de la muestra en el Activmetro. Registre todos los resultados en el formato AOE-P08-F-08Control de Calidad de Generadores de Radionclidos. Realice el ensayo en la Sonda Captus, seleccionando el analizador multicanal MCA y escogiendo el canal entre 275 y 425(start channel end cannel) correspondiente a la energa entre 550 850 KeV.
Programe como tiempo real 100 segundos.
Realice la medicin del fondo o Background y tenga en cuenta este valor para las determinaciones.
Tome la fuente de Cesio (Cs137) disponible y colquela en el pozo (well) de la Sonda Captus. Asegrese previamente de blindar la fuente para atenuar la radiacin beta y mida la radiacin.
Manteniendo la geometra, colocar la muestra de Tc99m dentro del mismo blindaje y realizar la lectura.
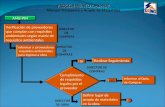
Aplique las siguientes ecuaciones para determinar la actividad de molibdeno en la muestra:
Calcule el factor de calidad de acuerdo a la siguiente ecuacin:
Registre todos los resultados en el formato AOE-P04-F-08 AOE-P08-F-08Control de Calidad de Generadores de Radionclidos.
NOTA: Si el radiofrmaco es para distribucin externa diligenciar el formato AOE-P04-F-17 Certificado Final de Control de Calidad2.7 NO CONFORMIDADES
Si el producto no cumple uno o ms criterios de aceptacin se debe: Repetir la prueba de control de calidad:
Si el producto no cumple el criterio evaluado se notificar al farmacutico supervisor de Control de Calidad y al Farmacutico Director Tcnico quienes sern responsables de la decisin final.
Si el producto cumple el criterio evaluado se debe repetir la prueba de control de calidad por tercera vez y se notificar al farmacutico supervisor de Control de Calidad y al Farmacutico Director Tcnico quienes sern responsables de la decisin final.
3. CONTROL DE CALIDAD MICROBIOLGICO
Responsable: Qumico Farmacutico de Control de Calidad.
3.1. OBJETIVO
Asegurar la estabilidad microbiolgica (bacterias, hongos y endotoxinas) de los radiofrmacos preparados.
3.2. DESCRIPCIN
La administracin intravenosa o subcutnea de los radiofrmacos, exige que las condiciones de marcacin y manipulacin de estos se realice con una tcnica asptica y en condiciones de completa esterilidad. Para ello, se hace necesario, planear y ejecutar una serie de pruebas que aseguren la ausencia de microorganismos (esterilidad) y que permitan cuantificar ciertos productos de su metabolismo como las endotoxinas.
3.3. EQUIPOS
Cabinas de Flujo laminar
Mdulo de Flujo laminar
Sistema Porttil de Deteccin Endosafe (PTS)
Detector de superficies.
3.4. INSUMOS
Cajas de Petri con Agar Sabouraud y Agar Sangre. (segn cabina y/o rea a evaluar)
Cartuchos del Sistema de Deteccin Endosafe.
Solucin de 99mTc y/o Radiofrmaco (segn programacin).
Solucin salina normal (SSN) x 100 mL (1).
Vial estril, apirgenos, al vaco (uno para cada muestra de radiofrmaco).
Jeringa de 1 mL
Jeringa de 3 mL
Etanol o isopropanol al 70%
Gasas estriles
Etiquetas, bolgrafo
Pinzas para viales
3.5. PROCEDIMIENTO
Los controles microbiolgicos de reas, productos y personal sern contratados externamente por el Instituto Nacional de Cancerologa, dentro de los siguientes parmetros:3.5.1. Prueba de Esterilidad
El procedimiento para la Prueba de Esterilidad deber ser llevado en condiciones escpticas y por personal entrenado y calificado. Todos los Radiofrmacos debern ser evaluados por la tcnica de FILTRACIN POR MEMBRANA O INOCULACIN DIRECTA.
Medios de Cultivo: Los medios de cultivo debern ser preparados segn Pharmacopea oficialmente aceptadas en Colombia como USP, Pharmacopea Europea, etc., debern ser estriles y permitir el crecimiento de aerobios, anaerobios, y hongos, y los procesos sern validados. Los medios de cultivo sern Tioglicolato para anaerobios, y casena de soya para hongos y aerobios.
Nmero de radiofrmacos a Examinar: Se enviar a cultivo una (1) muestra de 0.1mL de cada clase radiofrmaco producido en el transcurso de la semana y una vez verificado que se encuentre completamente decado, es decir sin actividad residual.
Tiempo de incubacin: La muestra deber ser incubada por 14 das a la temperatura especificada para el medio segn la USP (71).
Toma de muestra:
En la cabina de Flujo laminar proceda a seleccionar los viales que van a ser utilizados para cultivos microbiolgicos y marcados durante la misma semana. Tome un vial de muestra, por cada radiofrmaco marcado. Compruebe con el detector de superficies la ausencia de actividad. Verifique que cada vial contenga por lo menos 0.2mL de solucin. Si tiene algn vial con poco lquido, mida, 1mLde solucin salina normal y adicinelo al vial. Tome una (1) muestra de 0.1mL, rotlela con el Nombre de radiofrmaco, No Lote, fecha de marcacin, nombre del muestreador. Almacnela en la nevera por 3 semanas. Proceda a realizar el registro de cada muestra en el formato AOE-P04-F-14 Solicitud de Anlisis Microbiolgicos para Radiofrmacos, Cabinas y reas Radiofarmacia.
Coloque los viales en una bolsa plstica limpia o en una bandeja y entrguelos en el laboratorio microbiolgico contratado para su anlisis. Tenga en cuenta de recoger el reporte de resultados, a los 14 das despus de dicha entrega. (tiempo mnimo de incubacin). Promocin de Crecimiento: Las pruebas de promocin de crecimiento debern ser realizadas de acuerdo a lo establecido en la USP (71).
Interpretacin de los Resultados:
NO debe haber evidencia de crecimiento microbiolgico en el producto examinado.El test es invalidado si:
Los datos de monitoreo microbiolgico de las instalaciones para pruebas de esterilidad muestran falla
Fallas en los procedimientos analticos
Hay crecimiento microbiano en los controles negativos
La identificacin de los microorganismos aislados demuestra error en la tcnica.
3.5.2. Control Microbiolgico de reas
Los controles microbiolgicos de reas debern programarse con la firma contratada mensualmente y se realizarn el primer viernes de cada mes.
3.5.2.1. Ambientes
El muestreo se realizar por exposicin de las cajas de Petri con el agar una hora en el rea determinada segn FIGURA 1 PLANO DE RADIOFARMACIA el plano de la Radiofarmacia.
Figura N.1 PLANO DE RADIOFARMACIA Interpretacin de los Resultados:
para clase 100:
3UFC/placa/hora Para clase 10.000: 20UFC/placa/hora Para clase 100.000: 100UFC/placa/hora3.5.2.2. Superficies
El muestreo de superficies deber realizarse por la tcnica de CONTACTO CON LOS MEDIOS, O POR HISOPO y el agar deber permitir la cuantificacin de hongos, esporas y coliformes. El recorrido del hisopo debe ser aproximadamente 14-30cm2, tomar 5 puntos diferentes de cada superficie a muestrear.
Interpretacin de los Resultados:
para clase 100:
3UFC/30cm2 y coliformes ausentes Para clase 10.000: 5UFC/30cm2 y coliformes ausentes 10UFC/30cm2 (piso)
3.5.3. Control microbiolgico de personal
Los controles microbiolgicos de manos, guantes y uniformes del personal deber realizarse una (1) vez al mes por la tcnica de MUESTREO con HISOPO y el agar deber permitir la cuantificacin de hongos, esporas y coliforme.
Interpretacin de los Resultados:
para clase 100:
guantes :
3UFC/30cm2 y coliformes ausentes Uniformes: 5UFC/30cm2 y coliformes ausentes
Manos:
3UFC/30cm2 y coliformes ausentes
3.5.4. Test de Llenado escptico
Esta prueba ser realizada por una firma contratada externamente por el Instituto Nacional de Cancerologa y se realizar una vez cada 6 meses a todo el personal involucrado en la adecuacin de radiofrmacos. Se emplear como medio de cultivo caldo de casena de soya.
La metodologa empleada deber incluir los siguientes pasos:EQUIPOS
Cabina de Flujo laminar blindada.
Detector de superficies.
Activmetro.
INSUMOS
Gasas estriles.
Etanol o isopropanol al 70%.
Medios de cultivo lquido (600mL)
Viales estriles, apirgenos de 100ml
Jeringa de 50 ml
Jeringa de 10 mL
Viales de 10 mL
PROCEDIMIENTO
Ingrese a la Radiofarmacia segn AOE-P04-M-01 Manual de Seguridad para el Manejo y Adecuacin de Radiofarmacos.
Ingrese al rea de fraccionamiento de radiofrmacos. Encienda la cabina de flujo laminar.
Realice despeje de lnea y registre en el formato AOE-P04-F-50 Despeje de Lnea Radiofarmacia. Limpie la cabina segn AOE-P04-M-01 Manual de Seguridad para el Manejo y Adecuacin de Radiofarmacos.
Registre los datos de presin de la cabina segn el formato AOE-P04-F-39 Control de Presin Cabinas de Flujo Laminar Radiofarmacia. Aliste y sanitice todos los insumos no estriles con etanol al 70% o isopropanol antes de ingresarlos a la cabina.
Quite la tapa protectora de cada uno de los viales y limpie el tapn con etanol al 70% o isopropanol, permita que se evapore el exceso de alcohol; etiqutelos con nombre del istopo, nmero de alcuota, fecha y hora de elusin.
Con una jeringa de 50 mL transferir 100 mL de medio de cultivo a 6 frascos de 100mL estriles. Empleando una jeringa de 10mL transfiera dos alcuotas de 5 mL de caldo de un frasco de 100mL al otro de 100mL y agtelo. Repita el procedimiento con los mismos frascos pero a la inversa, es decir del frasco receptor se toman las dos alcuotas de 5mL y se transfieren nuevamente.
Empleando una jeringa de 10 mL transfiera alcuotas de 5 mL de cada uno de los frascos que contienen 100 mL a cada uno de los viales de 10 mL, tpelos e incbelos por 14 das Registre los datos en el formato AOE-P04-F-10 Marcacin de Radiofrmacos.
Limpie la cabina de flujo laminar nuevamente segn AOE-P04-M-01 Manual de Seguridad para el Manejo y Adecuacin de Radiofarmacos.
Registre el formato de AOE-P04-F-06 Uso de Equipos Radiofarmacia. Interpretacin de los Resultados:
No deber haber crecimiento bacteriano en ninguno de los frascos o viales.
respectivo de las reas, superficies y ambiente. Tenga en cuenta de recoger el reporte de resultados, a los 14 das despus de dicha entrega. (tiempo mnimo de incubacin).3.6. PRUEBA DE ENDOTOXINAS
Encienda el Endosafe. De acuerdo al manual AOE-P04-M-06 Manual de Uso Equipos de Radiofarmacia
Prepare la muestra del radiofrmaco a evaluar, teniendo en cuenta el clculo de la dilucin para evitar las interferencias. Esta dilucin debe permitir detectar el lmite de endotoxinas. Para esto, calcule la Mxima Dilucin Vlida (MDV),de acuerdo a:
La mayora de radiofrmacos tienen un volumen de dosis, menor a 1mL, para ellos la muestra se prepara tomado un vial estril, apirgeno y al vaco, se adiciona 0,1 mL de muestra a analizar y se completa a 4 ml con solucin salina estril. Este procedimiento le permite obtener un factor de dilucin de 40.
Realice la dilucin y coloque una muestra de 20uL en cada uno de los pozos del cartucho de endotoxinas
El Equipo automticamente le indicar el resultado.Resultado ser vlido si:
El Spike recovery 50%-200%
El coeficiente de variacin del control negativo: sanple Rxn Time CV 95 %
Pureza radionclida Deteccin de Molibdeno0.15Ci 99Mo por mCi de Tc99m
Endotoxinas Dilucin 40 Menor a 175UE/dosis
Esterilidad Cultivos NEGATIVOS para hongos y bacterias, despus de 7 das de incubacin a 37C.
99mTc-DTPA pH 3.8 7.5AOE-P08-F-11
Pureza Radioqumica Cromatografa TLC % 99mTc-DTPA >90 %
99mTc-DMSA pH 3.0 5.0|AOE-P08-F-11
Pureza Radioqumica Cromatografa TLC % 99mTc-DMSA >90 %
99mTc-MAG3 pH 5,0-6,0AOE-P08-F-11
AOE-P08-F-19
Esterilidad Cultivos NEGATIVOS para hongos y bacterias, despus de 7 das de incubacin a 37C.
Pureza Radioqumica Cromatografa TLC % 99mTc-MAG3 >90 %
Endotoxinas Dilucin 40 Menor a 175UE/dosis
PRODUCTOPRUEBAS DE CONTROLESPECIFICACINCRITERIO DE ACEPTACINFORMATO DE REGISTRO
99mTc-MDP pH 4.0 7.8AOE-P08-F-11
Pureza Radioqumica Cromatografa TLC % 99mTc-MDP >90 %
99mTc-MEBROFENIN pH 5.0-7.0 AOE-P08-F-11
Pureza Radioqumica Cromatografa TLC % 99mTc-MEBROFENIN >90 %
99mTc-ANTI-CEA Pureza Radioqumica Cromatografa TLC % 99mTc-ANTI-CEA >90 %AOE-P08-F-11
99mTc-HMPAO pH 9,0-10,0AOE-P08-F-11
Pureza Radioqumica Cromatografa TLC % 99mTc-HMPAO >90 %
99mTc-MAA pH 3.8 8-0AOE-P08-F-11
Pureza Radioqumica Cromatografa TLC % 99mTc-MAA >90 %AOE-P08-F-11
99mTc-FITATO COLOIDAL pH 5,0-7,0
AOE-P08-F-11
Pureza Radioqumica Cromatografa TLC % 99mTc-FITATO >90 %
99mTc-ESTAO COLOIDAL pH 6.0 - 7.0AOE-P08-F-11
AOE-P08-F-26
Pureza Radioqumica Cromatografa TLC % 99mTc-ESTAO COLOIDAL >90 %
PRODUCTOPRUEBAS DE CONTROLESPECIFICACINCRITERIO DE ACEPTACINFORMATO DE REGISTRO
99mTc-NANO-COLOIDE pH 6.0 - 7.4AOE-P08-F-11
Pureza Radioqumica Cromatografa TLC % 99mTc-NANOCOLOIDE >90 %
99mTc-MIBI pH 5.0 6.0AOE-P08-F-11
Pureza Radioqumica Cromatografa TLC Cromatografa en columna % 99mTc-MIBI >90 %
99mTc-LEUCOCITOS pH 6.0-7.0AOE-P08-F-15
Pureza Radioqumica % leucocitos marcados/ total 99mTc-LEUCOCITOS >60 %
99mTc-ERITROCITOS pH 6.0-7.0AOE-P08-F-11
Pureza Radioqumica % leucocitos marcados/ total in vitro > 90%,
Invivo-Invitro 80-90%
99mTc -Pirofosfato pH 4.0 7.5AOE-P08-F-11
AOE-P08-F-19
Pureza Radioqumica Cromatografa TLC % 99mTc-PIROFOSFATO >90 %
Endotoxinas Dilucin 40 Menor a 175UE/dosis
Esterilidad Cultivos NEGATIVOS para hongos y bacterias, despus de 7 das de incubacin a 37C.
99mTc - HMPAO pH 6.5 7.5AOE-P08-F-11
Pureza Radioqumica Cromatografa en capa delgada TLC % 99mTc-HMPAO >90 %
PRODUCTOPRUEBAS DE CONTROLESPECIFICACINCRITERIO DE ACEPTACINFORMATO DE REGISTRO
99mTc-HYNIC-TOC Apariencia Ausencia de partculasAOE-P08-F-22 AOE-P08-F-21 AOE-P08-F-19
pH 6,0-7,0
Pureza Radioqumica HPLC o Cromatografa en capa delgada TLC % 99mTc-HYNITOC >90 %
Endotoxinas Dilucin 40 Menor a 175UE/dosis
Esterilidad Permitir decaimiento por 60h Cultivos NEGATIVOS para hongos y bacterias, despus de 7 das de incubacin a 37C.
Unin a Protenas No mayor al 10%
Estabilidad en plasma Estabilidad +/- 5% que el porcentaje de pureza radioqumica
177Lu-DOTATATE Apariencia Ausencia de partculasAOE-P08-F-28 AOE-P08-F-19
pH 4.0-4.5
Pureza Radioqumica HPLC o Cromatografa en columna % 99mTc-DOTATATE >97 %
Endotoxinas Dilucin 40 Menor a 175UE/dosis
Esterilidad Permitir decaimiento por 170h Cultivos NEGATIVOS para hongos y bacterias, despus de 7 das de incubacin a 37C.
PRODUCTOPRUEBAS DE CONTROLESPECIFICACINCRITERIO DE ACEPTACINFORMATO DE REGISTRO
GENERADOR DE 188W/188Re Apariencia Ausencia de partculasAOE-P08-F-08
pH 4.5-7.5
Determinacin de Aluminio Menor a 10g/mL
Pureza Radioqumica % 188ReO4 LIBRE >95 %
Pureza radionuclida Deteccin de 188W 0.15Ci 188W por mCi de Re188
EndotoxinasDilucin 40 Menor a 175UE/preparado
Esterilidad Cultivos NEGATIVOS para hongos y bacterias, despus de 7 das de incubacin a 37C.
131I Cpsulas Pureza Radioqumica Cromatografa TLC 131-Yoduro >95%AOE-P08-F-30
Identidad Colorimetra Coloracin azul 131Yoduro
Actividad Porcentaje de variacin