Bioelementos Y Biomolculas 1218558388720374 8
-
Upload
lalo-garbander-garcia -
Category
Documents
-
view
609 -
download
0
Transcript of Bioelementos Y Biomolculas 1218558388720374 8

COMPOSICIÓN QUÍMICA DE LOS SERES VIVOS
BIOELEMENTOS BIOMOLÉCULAS
Uno de los retos de la Biología actual es la descripción de los complejos mecanismos químicos y físicos que sustentan la vida
Elementos químicos de la materia viva
Moléculas que componen a los seres vivos

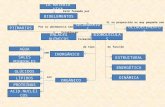
MAPA CONCEPTUALLa materia
viva
Bioelementos
Primarios Secundarios
Oligoelementos
Está formada por
Enlaces químicos
Por su abundancia son
Establecen
Biomoléculas
Formando
Inorgánicas
Orgánica
Sales minerales
Agua
Proteínas
Glúcidos
Nucleótidos
Lípidos
Son
Son
Estructural
Energética
Dinámica
De funciónDe tipo
Si su proporción es muy pequeña

BIOELEMENTOS
(a) Primarios o macroelementos
(b) Secundarios o microelementos
(c) Oligoelementos o elementos traza
Elementos químicos de la materia viva
Bioelementos
Primarios Secundarios
Oligoelementos
Por su abundancia son
Si su proporción es muy pequeña

(a) BIOELEMENTOS PRIMARIOS
Imprescindibles para formar los tipos principales de moléculas biológicas
Son los más abundantes 95% de la masa total de un ser vivo
Carbono (C)
Oxígeno (O)
Hidrógeno (H)
Nitrógeno (N)
Fósforo (P)
Azufre (S)

(b) BIOELEMENTOS SECUNDARIOS
En menor porcentanje (3,3%), pero imprescindibles para seres vivos
Calcio (Ca2+)
Cloro (Cl-)
Magnesio (Mg2+)
Contracción muscular
Movimiento celular
Regulación del funcionamiento enzimático, etc.
Constituyente de huesos y dientes
Coagulación sanguínea
Constituyente de la clorofila
Otras funciones
Sodio (Na+)
Potasio (K+)Conducción del impulso nervioso
Balance de agua en sangre y fluido intersticial

(c) OLIGOELEMENTOS
Presentes en organismos en cantidades muy pequeñas (menos del 0,1%), pero indispensables para el desarrollo armónico del organismo
Manganeso (Mn)Hierro (Fe)
Cobalto (Co)Cobre (Cu)
Zinc (Zn)
Boro (B)
Aluminio (Al)
Vanadio (V)
Molibdeno (Mo)
Yodo (I)
Silicio (Si)
Fluor (F)
Selenio (Se)
Funciones catalíticas imprescindibles

BIOMOLÉCULAS
(a) Inorgánicas
(b) Orgánicas
Moléculas que componen a los seres vivos
Distintas formas de asociación entre bioelementos
Biomoléculas
Inorgánicas
Orgánica
De tipo

(a) BIOMOLÉCULAS INORGÁNICAS
No son formadas sólo por los seres vivos, pero son muy importantes para ellos
(1) Agua
(2) Sales minerales
Biomoléculas
InorgánicasSales
minerales
Agua Son
De tipo

(a) BIOMOLÉCULAS INORGÁNICAS AGUA
Núcleo= protones + neutrones
Electrones de valencia
Niveles energéticos

O
H H
Oxígeno
Hidrógeno

O
H H
Enlaces covalentes
MOLÉCULA DE AGUA

MOLÉCULA DE AGUA
Mayor electronegatividad
Menor electronegatividad
O
H H

O
H H
Extremo parcialmente negativo
Extremo parcialmente positivo
MOLÉCULA DE AGUA

Extremo positivo sobre átomos de hidrógeno, y extremo negativo sobre el átomo de oxígeno
POLARIDAD DE LA MOLÉCULA DE AGUA
DIPOLO

Al existir un dipolo en la molécula, ésta puede atraer a sus vecinas por fuerzas de atracción entre cargas de diferente signo. Estas fuerzas se denominan atracción dipolo-dipolo
POLARIDAD DE LA MOLÉCULA DE AGUA

PUENTES DE HIDRÓGENO
La atracción dipolo-dipolo, que es inusualmente fuerte, se
denomina puente de hidrógeno

Enlaces covalentes
ESTRUCTURA DE LA MOLÉCULA DEL AGUA

ESTRUCTURA DE LA MOLÉCULA DEL AGUA

EL AGUA
75% de la superficie de la tierra
65% a 95% de la masa de los seres vivos
Surgió la vida
Extraordinarias propiedades físicas y químicas

PROPIEDADES DEL AGUA
Tensión superficial

PROPIEDADES DEL AGUA
Capilaridad
Movimiento ascendente de un líquido en un tubo estrecho
fuerzas entre moléculas de agua
fuerzas entre las moléculas de agua y paredes del capilar
atracción cohesiva

Alto calor específico
Cantidad de calor que necesita una sustancia para subir 1ºC la temperatura de 1 gramo de dicha sustancia
Calor específico
se necesita mucho calor para que el agua aumente su temperatura
no es fácil que el agua se caliente ni que se enfríe
se desprende mucho calor cuando ésta se enfría
Gran parte del calor es usado para romper los puentes de hidrógeno. Una vez conseguido esto, el calor se invierte en aumentar el movimiento de las moléculas, aumentando con ello la Tº

Congelación y Densidad
grandes porciones flotantes de glaciares muy frecuentes en las regiones polares
Icebergs
En estado sólido (hielo), el agua es menos densa que en estado líquido

Densidad =
MasaVolumen
> 4ºC
0 - 4ºC
Disminuye el movimiento
Moléculas se acercan
Moléculas se distancian
- T°C
Aumenta el volumen y por lo tanto disminuye la densidad
Disminuye el volumen

EL AGUA COMO DISOLVENTE
Uniones ion-dipolo
> Enlace iónico de la sal> Puentes de hidrógeno del agua
De compuestos iónicos
De compuestos polares
Como
AlcoholesAldehidosCetonas
Establece puentes de hidrógeno con ellos
Capacidad de solvatar: separar o disolver iones

(b) BIOMOLÉCULAS ORGÁNICAS
Sintetizadas exclusivamente por seres vivos
Se estructuran a base de átomos de carbono
(1) Carbohidratos
(2) Proteínas
(3) Lípidos
(4) Moléculas hechas de nucleótidos
Biomoléculas
OrgánicaProteínas
Glúcidos
Nucleótidos
Lípidos
Son
De tipo

Grupos de átomos unidos a una cadena de carbonos e hidrógenos
(b) BIOMOLÉCULAS ORGÁNICAS
Las moléculas orgánicas van a tener determinadas agrupaciones características de átomos que reciben el nombre de grupos funcionales
Hidroxilo (OH)
Carboxilo (COOH)
Amino (NH2)
Grupos funcionales de importancia en Biología:
Fosfato (H3PO4)

HIDROXILO (OH)
CARBOXILO (COOH)
AMINO (NH2)
Hace que las moléculas sean hidrosolubles Abundante en azúcares
Moléculas que lo poseen se llaman ácidos liberan un protón (H+) En aminoácidos y ácidos grasos
En aminoácidos
FOSFATO (H3PO4)
En fosfolípidos y en nucleótidos Se representa como P

(b) BIOMOLÉCULAS ORGÁNICAS
(1) Carbohidratos
(2) Proteínas
(3) Lípidos
(4) Moléculas hechas de nucleótidos

(1) CARBOHIDRATOS (CH2O)n
(Construidos de azúcares simples)
Se clasifican según el número de unidades de azúcar que contienen:
Monosacáridos
Disacáridos
Polisacáridos
Carbohidratos
Unidad (azúcar)
Enlace glucosídico (covalente)
Enlace glucosídico

Triosas
Pentosas
Hexosas
Monosacáridos
De 3 átomos de carbono (C3H6O3)
De 5 átomos de carbono (C5H10O5)
De 6 átomos de carbono (C6H12O6)
Gliceraldehído
Dihidroxiacetona
Ejemplos:
Participan en el metabolismo de los azúcares
Ribosa
Desoxirribosa
Ejemplos:
Parte de la estructura de nucleótidos
Glucosa
Fructosa
Galactosa
Ejemplos: Por contener muchos grupos hidroxilo son muy hidrosolubles
Unidad (azúcar)

Disacáridos
Sacarosa
Lactosa
Maltosa
Glucosa + Fructosa
Glucosa + Galactosa
Glucosa + Glucosa
Sintetizada por plantas, es la responsable del sabor dulce de los frutos
Es el azúcar de la leche

Polisacáridos
Almidón
Glucógeno
Celulosa
Forma en que las plantas almacenan glucosa en semillas y otras estructuras “Harina” forma saludable de consumir carbohidratos (como alternativa a dulces)
Forma en que los animales almacenan glucosa, principalmente en el hígado
No sirve para almacenamiento, sino que cumple un papel estructural, ej. pared celular

FUNCIONES DE CARBOHIDRATOS
C6H12O6 + 6O2 6CO2 + 6H2O + energía
Función energética fuente de energía inmediata para la célula
Función estructural por algunos polisacáridos entre los que destacan:
Función protectora
Función de reconocimiento
electrones
Se oxida
Reduce a “otros”
Celulosa
Quitina principal componente de exoesqueleto de artrópodos
Ciertos polisacáridos estructurales se asocian con proteínas y recubren los epitelios respiratorio y digestivo (mucinas de secreción)
Debido a la presencia de algunos oligosacáridos sobre la superficie de la membrana celular

(b) BIOMOLÉCULAS ORGÁNICAS
(1) Carbohidratos
(2) Proteínas
(3) Lípidos
(4) Moléculas hechas de nucleótidos

(2) PROTEÍNAS
Constituyen el 50% de masa seca de seres vivos
Responsables de características de células
Una célula difiere de otra por el tipo de proteína que predomina en ella, especialmente en lo que a su función se refiere

ESTRUCTURA
Polímeros de aminoácidos (aa)
Se caracterizan por poseer un grupo carboxilo (-COOH) y un grupo amino (-NH2)
Las otras 2 valencias del carbono se saturan con un átomo de H y un grupo variable denominado radical R
Se distinguen 20 tipos de aa

Los aa se unen por enlace covalente formado por deshidratación
Enlace peptídico
Entre el grupo carboxilo de un aa y el grupo amino del siguiente con desprendimiento de una molécula de agua

Hay 20 tipos de aa en las proteínas
Alanina
Valina
Leucina
Isoleucina Metionina
Fenilalanina Triptófano
No polares
Glicina Serina
Treonina
Cisteína
Asparina Glutamina
Tirosina
Polares sin carga
Ácido aspártico
Ácido glutámico
Ácidos
Lisina Arginina
Histidina
Básicos

NIVELES DE ORGANIZACIÓN
(a) Estructura primaria
Es la secuencia lineal de aa, es decir, el orden en que están colocados los aa en una proteína
La función de una proteína depende de su secuencia y de la forma que ésta adopte

(b) Estructura secundaria
Corresponde a plegamientos que se forman debido a interacciones entre aa no adyacentes
Entre las interacciones responsables de la e. secundaria están los puentes de hidrógeno
Forma helicoidal
Existen 2 tipos de estructura secundaria:
Forma laminar

Forma helicoidal
La estructura primaria se enrolla helicoidalmente sobre sí misma. Se debe a la formación de puentes de hidrógeno entre –C=O de un aa y el –NH- del cuarto aa siguiente
Predomina en proteínas fibrosas (ej. colágeno, elastina, queratina y seda). Estas fibras son elásticas debido a que los puentes de H se forman y se destruyen

Forma laminar
Se forma una cadena en forma de zigzag

(c) Estructura terciaria
Es la forma tridimensional, generalmente globular, de una proteína cuya estructura secundaria se ha plegado sobre sí misma, debido a interacciones entre aa no adyacentes

Se mantiene estable gracias a enlaces entre radicales R de aa:
Puentes disulfuro entre radicales de aa que tienen S Puentes de hidrógeno
Puentes eléctricos
Interacciones hidrófobas

La estructura terciaria es esencial para la función de una proteína
en un anticuerpo no se une al antígeno
en un receptor de membrana no captará la señal que corresponde
Alteración desnaturalización
en una enzima no calzará con reactantes

(d) Estructura cuaternaria
Unión, mediante enlaces débiles (no covalentes), de más de una cadena polipeptídica (subunidad o protómero) con estructura terciaria, para formar un complejo proteico
Ejemplos:
Hexoquinasa con 2 subunidades
Hemoglobina con 4 subunidades globulares

Los genes determinan el orden de aa en la proteína (E. primaria)
El orden de aa en la proteína determina la forma en que se pliega el polipéptido (E. secundaria y terciaria)
FORMA FUNCIÓN
Los genes determinan la función de las proteínas

FUNCIÓN ESTRUCTURAL
Algunas proteínas constituyen estructuras celulares
Glucoproteínas forman parte de membranas celulares y actúan como receptores o facilitan el transporte de sustancias
Histonas forman parte de cromosomas que regulan la expresión de genes
Principales componentes estructurales de células (crecimiento, desarrollo y reparación de
tejidos)

FUNCIÓN ESTRUCTURAL
Otras proteínas confieren elasticidad y resistencia a órganos y tejidos
Colágeno del tejido conjuntivo fibroso (tendones, cartílagos, pelos)
Elastina del tejido conjuntivo elástico
Queratina de la epidermis
Fibroina segregada por arañas y gusanos de seda para fabricar telas de araña y capullos de seda, respectivamente

Son las más numerosas y especializadas
FUNCIÓN ENZIMÁTICA
Biocatalizadores de reacciones químicas del metabolismo celular
Ácido graso sintetasa cataliza síntesis de ácidos grasos
Consideremos que todas las enzimas son proteínas (hacen posible las reacciones químicas)

FUNCIÓN HORMONAL
Insulina y glucagón regulan niveles de glucosa en la sangre
Hormona del crecimiento
Adrenocorticotrópica regula síntesis de corticosteroides
Calcitonina regula metabolismo del calcio
Acción hormonal en células
adyacentes
Acción hormonal en células lejanas

FUNCIÓN DEFENSIVA
Inmunoglobulinas actúan como anticuerpos frente a posibles antígenos
Trombina y fibrinógeno contribuyen a formación de coágulos sanguíneos para evitar hemorragias
Mucinas efecto germicida y protegen a las mucosas
Algunas toxinas bacterianas (Botulismo), o venenos de serpientes son proteínas con funciones defensivas
Todos los anticuerpos son proteínas

FUNCIÓN DE TRANSPORTE
Hemoglobina transporta oxígeno en la sangre de vertebrados
Hemocianina transporta oxígeno en la sangre de invertebrados
Mioglobina transporta oxígeno en los músculos
Lipoproteínas transportan lípidos por la sangre
Citocromos transportan electrones
Estructuras encargadas del transporte de sustancias a través de la membrana plasmáticas ( canales, transportadores y bombas)

FUNCIÓN CONTRÁCTIL
miofibrillas responsables de la contracción muscular
Dineina relacionada con movimiento de cilios y flagelos
Casi todos los movimientos se deben a la acción de combinaciones de proteínas
Actina
Miosina
Tubulina en microtúbulos, filamentos responsables de movimiento de cilios y flagelos

FUNCIÓN DE RESERVA
Ovoalbúmina clara de huevo
Gliadina del grano de trigo
Hordeína de la cebada
Lactoalbúmina de la leche
Reserva de aa para desarrollo de embrión

FUNCIÓN REGULADORA
Regulan la expresión de ciertos genesRegulan división celular Ciclina
FUNCIÓN HOMEOSTÁTICA
Mantienen el equilibrio osmótico y actúan con otros sistemas amortiguadores para mantener constante el pH del medio interno
Estructuras receptoras de señales en la membrana plasmática

(b) BIOMOLÉCULAS ORGÁNICAS
(1) Carbohidratos
(2) Proteínas
(3) Lípidos
(4) Moléculas hechas de nucleótidos

(3) LÍPIDOS
Grupo diverso de moléculas, con 2 características importantes: Contienen regiones extensas formadas casi exclusivamente por H y C, con enlaces C ― C
C ― HNo polares
Regiones no polares lípidos son hidrofóbicos
Aceites, grasas y ceras
Fosfolípidos
Esteroides
Lípidos

ACEITES, GRASAS Y CERAS
Sólo contienen C, H y O
Contienen una o más subunidades de ácido graso
Largas cadenas de C e H con grupo carboxilo en extremo
Grupo carboxilo
En general, no tienen estructuras en forma de anillo

GRASAS Y ACEITES
Deshidratación
Nombre químico: Triglicéridos
Se utilizan como almacén de energía a largo plazo, tanto en plantas como animales almacenan cierta cantidad de energía en menos masa que los carbohidratos


GRASAS Y ACEITES
Con enlaces sencillos en cadenas de C está saturado porque está “lleno” de átomos de H: tiene el mayor N° posible de átomos de H
Si hay dobles enlaces entre algunos átomos de C está insaturado, tiene menos átomos de H

GRASAS ACEITES
Sin dobles enlaces
cadena de ácido graso es recta ácidos grasos pueden acomodarse muy juntos , por lo que forman un sólido a T° ambiente
Con dobles enlaces
Dobles enlaces producen flexiones en la cadena de ácido graso
Flexiones mantienen separadas las moléculas de aceite, por lo que son líquidos a T° ambiente

CERAS
Se forman por la unión de un ácido graso y un monoalcohol, mediante un enlace éster

CERAS
Químicamente similares a grasas altamente saturadas, por lo que son sólidas a T° ambiente
En plantas terrestres:
En animales:
Impermeabilizantes para el pelo de mamíferos y pluma de aves
Impermeabilizantes para exoesqueletos de insectos
Construcción de complejas estructuras como colmenas
Recubrimiento impermeable en hojas y tallos
Molécula completamente apolar, hidrófoba función típica consiste en servir de impermeabilizante

FOSFOLÍPIDOS
Similares a aceites con excepción de que uno de los 3 ácidos grasos es reemplazado por un grupo fosfato que tiene unido un grupo funcional polar corto, el cual generalmente contiene N

Colas hidrofóbicas insolubles en agua
Cabeza polar tiene carga eléctrica y es soluble en agua (hidrofílica)
FOSFOLÍPIDOS

FOSFOLÍPIDOS
Importantes componentes estructurales de las membranas celulares

ESTEROIDES
Estructuralmente diferentes de todos los demás lípidos
4 anillos de C fusionados, de los cuales se proyectan diversos grupos funcionales
Las diferencias en los grupos funcionales unidos a los anillos pueden dar como resultado, grandes diferencias en la función de los esteroides

FUNCIONES
F. de reserva: son la principal reserva energética del organismo
F. estructural: forman las bicapas lipídicas de membranas celulares. Recubren y proporcionan consistencia a los órganos, y protegen mecánicamente estructuras o son aislantes térmicos como el tejido adiposo. Forman cubiertas impermeables en plantas o animalesF. catalítica: aportan vitaminas que facilitan el trabajo de enzimas en las reacciones biológicas. En ausencia de la vitamina, la enzima no puede funcionar con todos los perjuicios que puede ocasionar. Ej. retinoides (vitamina A), tocoferoles (vitamina E), naftoquinonas (vitamina K) y calciferoles (vitamina D).
F. informativa: muchas hormonas tienen estructura lipídica (esteroides, prostaglandinas, leucotrienos, calciferoles, etc) y constituyen señales químicas que permiten la adaptación del organismo a diversas condiciones ambientales

(b) BIOMOLÉCULAS ORGÁNICAS
(1) Carbohidratos
(2) Proteínas
(3) Lípidos
(4) Moléculas hechas de nucleótidos

ACIDOS NUCLEICOS
Largas cadenas de subunidades similares llamadas nucleótidos
(1) Un azúcar (pentosa)
(2) Un grupo fosfato
(3) Una base nitrogenada
Ribosa
Desoxirribosa

NUCLEÓSIDOS
Azúcar
Base nitrogenada

NUCLEÓTIDOS
Fosfato
Azúcar
Base nitrogenada
RibosaDesoxirribosa
Ácido desoxirribonucleic
o ADN
Ácido Ribonuclei
co ARN

Los nucleótidos se enlazan en largas cadenas cuando el grupo fosfato de un nucleótido forma un enlace covalente (unión fosfodiester) con el azúcar de otro

Ácido desoxirribonucleic
o ADN
Ácido Ribonuclei
co ARN
CADENAS DE NUCLEÓTIDOS

Tipos de base
nitrogenada
Cadena de nucleótidos
CADENAS DE NUCLEÓTIDOS

ÁCIDO DESOXIRRIBONUCLEICO

ÁCIDO DESOXIRRIBONUCLEICO
El ADN se encuentra en los cromosomas de todos los seres vivos y sus sucesión de nucleótidos deletrea la información genética necesaria paraconstruir las proteínas de cada organismo

CÓDIGO GENÉTICO
regla de correspondencia entre la serie de nucleótidos de los ácidos nucleicos y las series de aminoácidos (polipéptidos) en que se basan las proteínas

DOGMA CENTRAL DE LA BIOLOGÍA CELULAR

Coenzimas: NAD NADP FAD
NUCLEÓTIDOS LIBRES EN LAS CÉLULAS
Ribonucleótidos y desoxirribonucleótidos forman los ácidos nucleicos ARN, ADN
Transportadores de energía: ATP ADP
Mensajeros intracelulares:AMP cíclico (receptores hormonales)