Síntesis de biodiesel mediante catálisis acida heterogénea a partir ...
Catálisis heterogénea
-
Upload
anitafpardo -
Category
Documents
-
view
476 -
download
4
Transcript of Catálisis heterogénea

Catálisis Heterogénea
M.C. Manuel Román Aguirre

Negocio$$$$• En México, en la década
pasada tan solo la industria petroquímica consumía mas de:
10, 000 ton/año de catalizadores
equivalente a mas de
• US$ 300,000,000.00
•S. Fuentes. Appl. Catal. A. general, 142 (1996) 179-181
•Downstreamtoday.com
M. C. Manuel Román Aguirre

Vida cotidiana
El 80 % de los productos químicos
requiere al menos un proceso
catalítico, es decir, al menos un catalizador
M. C. Manuel Román Aguirre

Catalizador
• “Una entidad que cambia la velocidad de una reacción química tomando parte íntimamente en ella pero sin llegar a ser un producto”
• J. Blanco, R. Linarte, Catálisis: fundamentos y aplicaciones industriales. 1ra Ed. Trillas, México, 1976
M. C. Manuel Román Aguirre

Reacción catalizada
H3C O
+ H+
H3C O+H H
H
C+H3C
+ H2O
H3C
H+ +
H3C OH
+ H2O
CH3
M. C. Manuel Román Aguirre

Catalizador Heterogéneo
• Es un catalizador que no se encuentra en la misma fase que el medio de reacción. Por ejemplo: Un catalizador sólido en un sistema gaseoso
M. C. Manuel Román Aguirre

Catálisis heterogénea
Catalizador sólido
C
O
C
ON
O
N
O
2CO + 2NO 2CO2 + N2
M. C. Manuel Román Aguirre

La vida diaria
CO
CO
NO
NO
M. C. Manuel Román Aguirre

Fisicoquímica
• Fenómenos de adsorción y desorción
• Formación de complejos intermedios
• Energías de activación
• Cinética
M. C. Manuel Román Aguirre

Fisicoquímica
Langmuir: Premio Nobel de Quimica
1932
M. C. Manuel Román Aguirre

Fisicoquimica
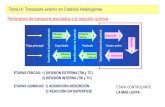
1. Difusión de reactivos desde la masa de fluido a la superficie del catalizador
2. Difusión de reactivos a través de los poros del catalizador
3. Adsorcion de los reactivos sobre la superficie del catalizador
4. Transformación química de las especies adsorbidas5. Desorción de los productos6. Difusión de los productos a través de los poros7. Difusión de los productos desde la superficie del
catalizador
M. C. Manuel Román Aguirre

Fisicoquímica: Adsorción, reacción y desorción
C2H2 + H2 C2H6
Ni
Adsorción de los
reactivos a la superficie
del catalizador
Formación de
complejos intermedios
(ruptura y formación
de enlaces)
desorción de los
reactivos de la superficie
del catalizador
Ni
M. C. Manuel Román Aguirre

Fisicoquímica: energía de activación
E Ea = EI - ER
ER
EP
EI
HR = Ep- ER
Ea = Energía de activación HR = Calor de reacción
C2H2 + H2 C2H6
M. C. Manuel Román Aguirre

E
Fisicoquímica: energía de activaciónM. C. Manuel Román Aguirre
C2H2 + H2 C2H6Ni

E
M. C. Manuel Román Aguirre
Fisicoquímica: energía de activación
El catalizador, disminuye la
barrera de energía que deben vencer los reactivos para llegar a productos

• Velocidad controlada por la difusión (que tan rápido difunden los reactivos a la superficie del catalizador o los productos hacia el flujo de reactivos))
• Velocidad controlada por la adsorción-desorción (que tan rápido se adsorben los reactivos a la superficie o que tan rápido se desorden los productos de la superficie)
Velocidad controlada por la reacción (que tan rápido se consumen los reactivos y se forman los productos)
M. C. Manuel Román Aguirre
Fisicoquímica: Cinética

• La velocidad global del proceso catalítico está
dominada por el fenómeno mas lento
M. C. Manuel Román Aguirre
Fisicoquímica: Cinética

Velocidad de reacción
Velocidad de difusión
T
Velo
cida
d
Velocidad real
M. C. Manuel Román Aguirre
Fisicoquímica: Cinética

v = kgA a(pAg-pAi
)
M. C. Manuel Román Aguirre
Fisicoquímica: Cinética
v = Velocidad de difusión
kgA = coeficiente de difusión
a = área superficial del catalizador
pAg = presión parcial de A en el flujo de gas
pAi = presión parcial de A en la superficie del catalizador

A + l Al
M. C. Manuel Román Aguirre
Fisicoquímica: Cinética
v = velocidad de adsorción
K= constante de equilibrio
L = concentración total de sitios activos por unidad de masa
CAl = Concentración de la especie Al
Cl = concentración de sitios activos libres
pAi = presión parcial de A en la superficie del catalizador
K =
CAl
Cl pA
k
k’
v = k Cl pA – k’CAl

Al + Bl Cl + Dl
M. C. Manuel Román Aguirre
Fisicoquímica: Cinética
v = velocidad de reaccion de las especies adsorbidas
K= constante de equilibrio
Ci = concentración de la especie i
k y k’Al = Constantes de velocidad
K =
CCl
k
k’
v = k CAl Cbl – k’CCl CDl
CDl
CAl CBl

M. C. Manuel Román Aguirre
Fisicoquímica: Cinética

Características de interés en un catalizador sólido
• Área superficial
• Diámetro de poro
• Número de sitios activos
• Propiedades mecánicas
• Estabilidad térmica y química
• ACTIVIDAD
• COSTO
M. C. Manuel Román Aguirre

SuperficieM. C. Manuel Román Aguirre
El área superficial aumenta con la porosidad

SuperficieM. C. Manuel Román Aguirre
El área superficial aumenta con la disminución del tamaño de partícula.

Diámetro de poro
El diámetro de poro debe ser suficientemente grande para que los reactivos puedan entrar e interaccionar con la superficie
M. C. Manuel Román Aguirre

SuperficieM. C. Manuel Román Aguirre
Soporte Área superficial
m2/g
Diámetro de poro
(Å)
MCM-41 (SiO2) 1000-1500 15-40
Sílice nanométrica
200- 400 NA
Carbón activado 2000 a 3000 8

Sitios activosM. C. Manuel Román Aguirre
Flujo de reactivos
Superficie del
catalizador
Sitios activos

Sitios activosM. C. Manuel Román Aguirre
Flujo de reactivos
Superficie del
catalizador
Sitios activos

Estabilidad térmica
El catalizador, ya sea en su fase activa o en el soporte, no debe degradarse, colapsar, o cambiar
de fase o estructura a la temperatura típica de reacción
M. C. Manuel Román Aguirre

Estabilidad química
El catalizador, no debe deteriorarse con el medio reaccionante (arrastrarse en la reaccion, contaminarse (envenenarse), cambiar su
composicion quimica, etc.)
M. C. Manuel Román Aguirre

Estabilidad química
El catalizador, no debe deteriorarse con el medio reaccionante (arrastrarse en la reaccion, contaminarse (envenenarse), cambiar su
composicion quimica, etc.)
M. C. Manuel Román Aguirre

Estabilidad química
El catalizador, no debe deteriorarse con el medio reaccionante (arrastrarse en la reaccion, contaminarse (envenenarse), cambiar su
composicion quimica, etc.)
M. C. Manuel Román Aguirre

Actividad, selectividad y estabilidad
cantidad de reactivo convertido
(unidad de tiempo)·(cantidad de catalizador)
Actividad: es una medida de la velocidad de la reacción
en relación al catalizador utilizado:
M. C. Manuel Román Aguirre

Selectividad: es el cociente entre los moles de producto
deseado obtenidos y los moles de reactivo
consumidos
Actividad, selectividad y estabilidadM. C. Manuel Román Aguirre
A + B C
A + B D
A: REACTIVO LIMITANTE
C: PRODUCTO DESEADO
NA0: MOLES INICIALES DE A
NA: MOLES REMANENTES DE A
NC: MOLES PRODUCIDAS DE C
S = NC
NA0-NA

Estabilidad: es la medida de la capacidad de un
catalizador para convertir reactivos en productos
durante su “tiempo de vida”:
cantidad de reactivo convertido
cantidad de catalizador
Actividad, selectividad y estabilidadM. C. Manuel Román Aguirre

Ventajas y desventajas de la catálisis heterogénea
Cat.Homogénea
Cat. Heterogénea
Condiciones de reacción Suaves Severas
Separación de productos y cat. Difícil Fácil
Recuperación del catalizador Caro No Requiere
Estabilidad térmica catalizador Baja Alta
Tiempo de vida del catalizador Variable Alto
Actividad Alta Variable
Selectividad Alta Media-baja
Sensibilidad al envenenamiento Baja Alta
Determinación de propiedades estéricas y electrónicas del catalizador
Viable Muy Difícil
Determinación del mecanismo Frecuente Muy Difícil
Problemas de difusión Bajo Importantes
M. C. Manuel Román Aguirre

Clasificación de los catalizadores heterogéneos
Tipo de fase activa
Procesos industriales Ejemplos
Metales Hidrogenación, deshidrogenacion, combustión total, metanación, oxidación
Ni, Pd, Pt, Ag
Óxidos metálicos semiconductores
Oxidación, deshidrogenación, hidrodealquilación, desproporción de olefinas, polimerización, hidrogenación
Cr2O3, V2O5, MoO3
Sales metálicas Hidrodesulfuración, oxicloración CoS, NIS, CuCl2
Óxidos metálicos aisladores (ácidos y bases)
Isomerización, deshidratación, desintegración catalítica, alquilación, hidratación
Al2O3, SiO2-Al2O3, MgO
Bifuncionales Reformación Pt/Al2O3
M. C. Manuel Román Aguirre
•J. Blanco, R. Linarte, Catálisis: fundamentos y aplicaciones industriales. 1ra Ed. Trillas, México, 1976

CRUDO DESTILACION
ATMOSFERICA
DESTILACION
AL VACIO
COQUIZACION
HID
RO
TR
AT
AM
IEN
TO
TAME MTBE
FCC
RECUPERACIONY ENDULZAMIENTODE GAS SATURADO
REFORMACIONDE GAS
RECUPERACION DE AZUFRE
REFORMACION
C5/C6
ISOMERIZACION
ENDULZ. Y RECUP.DE LIGEROS DE
GAS NO SATURADO
ALQUILACIONC3’s - C4’s
n C4
ISOMERIZACION
C3/C4 A LPGH2
AZUFRE
H2S
H2
GASOLINA
DIESEL
GAS COMBUSTIBLE
LPGC3
=
nC4
H2COMBUSTOLEO
ACL
ACEITE DECANTADO
METANOLDESTILADOS
COQUE
C5=‘s C4=‘s
H2S
H2
Catalizadores en la industria química (petroquímica básica)
M. C. Manuel Román Aguirre

Catalizadores en la industria química (petroquímica básica)
M. C. Manuel Román Aguirre

Catalizadores en la industria química (agricultura)
Proceso de producción de amoniaco (NH3)
M. C. Manuel Román Aguirre

Catalizadores en la industria química (agricultura)
Planta de producción de amoniaco (NH3)
M. C. Manuel Román Aguirre

COOH
CH3
iPr
Ibuprofen 8000 Tm/año
- H2O CN
CH3
iPr
H2O- NH3
HC
CH3
iPr
NOH
CHO
CH3
iPr NH2OHCH3
iPr
O CO2Et
(CH3CO)2O AlCl3
O
CH3
iPr
ClCH2CO2Et NaEtO
iPr
- H2O
NaEtO/EtOHHCl/H2O
- HCOOEt - NaCl
- NaCl
- CH3COOH
Ruta Boots
O
CH3
iPr
(CH3CO)2O HF
H2
Pd/C
CH3
iPr
OH CO
PdCl2(PPh3)2 HCl
Ruta Hoescht
Catalizadores en la industria química (fármacos)
M. C. Manuel Román Aguirre

Catalizadores en energías alternativas (Celdas de combustible)
M. C. Manuel Román Aguirre

CH4 + H2O CO + 3H2
CO + H2O CO2 + H2
CnHm + n H2O nCO + (n + m/2) H2
Catalizadores en energías alternativas (producción de hidrógeno)
M. C. Manuel Román Aguirre

Catalizadores en energías alternativas (producción de hidrógeno)
M. C. Manuel Román Aguirre

Catalizadores en energías alternativas (producción de hidrógeno)
M. C. Manuel Román Aguirre

Catalizadores en energías alternativas M. C. Manuel Román Aguirre
Proyecto CUTE(Clean Urban Tranport for Europe)

Eg
foton UV> 348 nm
O2
O2-
Cr(VI)
Cr(III)
H2O
orgánicos
CO2 + H2O
H+ + [HO]·
banda de valencia
banda de conducción
Fotocatálisis sobre TiO2
Catalizadores: Contaminación ambiental
M. C. Manuel Román Aguirre

Catálisis: Investigación
0
10000
20000
30000
40000
50000
60000
70000#
de
Art
icu
los
1950 1974 1980 1988 1993 1997 2001
Año
M. C. Manuel Román Aguirre

Catálisis: Investigación
Lineas de investigacion en CIMAV• Materiales catalíticos nanoestructurados• Catalizadores para celdas de combustible• Producción de hidrogeno• Fotocatálisis (control de contaminantes)• Petroquímica (desulfuración, crackeo)• Química fina (obtención de materiales para la
industria farmacéutica y cosmética)

Catálisis: Investigación
Buscando solución a problemas de:
• Contaminación ambiental
• Fuentes alternas de energía
• Mejora en el desempeño de procesos petroquímicos
• Aprovechamiento de recursos regionales