Epilepsia del lóbulo temporal y papel de la Enfermería
Transcript of Epilepsia del lóbulo temporal y papel de la Enfermería

Epilepsia del lóbulo temporal y papel de la Enfermería
TEMPORAL LOBE EPILEPSY AND NURSING ROLE
Autor: Javier Peña Ceballos
Tutora: María José Noriega Borge
CURSO ACADÉMICO 2014-2015
UNIVERSIDAD DE CANTABRIA
ESCUELA UNIVERSITARIA “CASA DE SALUD VALDECILLA”
GRADO EN ENFERMERÍA

ÍNDICE
1. RESUMEN Y PALABRAS CLAVE……………………………….……………………………….... 1
2. INTRODUCCIÓN………………………………………………………………………………………… 2
2.1. Objetivos generales y específicos…………………………………………………….. 2
2.2. Metodología……………………………………………………………………………………. 3
2.3. Descripción de los apartados de la monografía……………………………….. 3
2.4. Epidemiología………………………………………………………………………………….. 4
2.5. Terminología según la International League Against Epilepsy (ILAE)… 4
2.6. Clasificación de epilepsias según la ILAE………………………………………….. 5
3. BASES CELULARES DE LA EPILEPSIA..………………………………………………….…….. 7
3.1. Señales eléctricas……………………………………………………………………………. 7
3.2. Canales iónicos……………………………………………………………………………….. 8
3.2.1. Canales iónicos despolarizantes dependientes de voltaje………… 8
3.2.2. Canales iónicos hiperpolarizantes dependientes de voltaje……… 9
3.3. Neurotransmisores…………………………………………………………………………. 9
3.4. Estudio electrofisiológico de la epilepsia…………………………………………. 10
4. EPILEPSIA DEL LÓBULO TEMPORAL…………………………..……………………………… 12
4.1. Epidemiología…………………………………………………………………………………. 12
4.2. Etiología………………………………………………………………………………………….. 12
4.3. Manifestaciones clínicas…………………………………………………………………. 14
4.4. Diagnóstico de la epilepsia del lóbulo temporal……………………………… 14
4.4.1. Historia clínica………………………………………………………………………….. 15
4.4.2. Electroencefalograma (EEG)/Videoelectroecefalograma (VEEG). 15
4.4.3. Resonancia magnética……………………………………………………………… 17
4.4.4. Tomografía de emisión de fotón simple (SPECT)………………………. 18
4.4.5. Tomografía por emisión de positrones (PET)……………………………. 19
4.4.6. Substraction Ictal SPECT Co-registered to MRI (SISCOM)…………. 19
4.4.7. Electrodos intracraneales………………………………………………………… 19
4.4.8. Test neuropsicológicos…………………………………………………………….. 20

4.5. Tratamiento…………………………………………………………………………………….. 21
4.5.1. Tratamiento preventivo……………………………………………………………. 21
4.5.2. Tratamiento médico…………………………………………………………………. 21
4.5.3. Tratamiento quirúrgico…………………………………………………………….. 22
4.5.3.1. Técnicas resectivas…………………………………………………………….. 23
4.5.3.2. Técnicas no resectivas……………………………………………………….. 24
4.6. Otras alternativas: Dieta cetogénica (DC)………………………………………… 24
5. CUIDADOS DE ENFERMERÍA …………………………………………………………………….. 26
5.1. Papel de la Enfermería en la educación sanitaria de pacientes epilépticos y
familiares………………………………………………………………………………………………. 26
5.2. Cuidados de enfermería en pruebas diagnósticas……………………………. 26
5.2.1. Cuidados de Enfermería en la Resonancia Magnética (RM)………. 26
5.2.2. Cuidados de enfermería en el Electroencefalograma (EEG)………. 26
5.2.3. Cuidados de Enfermería en el PET y SPECT………………………….……. 27
5.3. Papel de la Enfermería en el tratamiento quirúrgico de la epilepsia: Funciones
de la/el enfermera/o circulante e instrumentista.……………………………….. 27
6. CONCLUSIONES……………………………………..……………………………………………….. 28
7. BIBLIOGRAFÍA………………………………………..……………………………………………….. 29
8. ANEXOS………………………………………………………………………………………………….. 36

1
1. RESUMEN Y PALABRAS CLAVE/ABSTRACT AND KEYWORDS.
Resumen y palabras clave.
La epilepsia es una enfermedad neurológica que afecta al Sistema Nervioso Central (SNC), siendo la segunda enfermedad neurológica más prevalente, que se manifiesta por crisis convulsivas. Las crisis epilépticas se producen por un desequilibrio entre los mecanismos excitatorios e inhibitorios neuronales mediados por los neurotransmisores glutamato y ácido γ−aminobutírico (GABA), respectivamente. Estas crisis epilépticas pueden ser generalizadas o focales.
La epilepsia del lóbulo temporal (ELT) es la más frecuente dentro de las focales. Esta patología puede localizarse unilateral o bilateralmente en los lóbulos temporales siendo la esclerosis del hipocampo (EH) el hallazgo fisiopatológico más relevante. El foco epileptógeno puede localizarse en la zona mesial o en la zona neocortical, dando lugar a diferentes signos y síntomas. La ELT se caracteriza por ser resistente a fármacos antiepilépticos (FAE) entre el 25-40% de los casos siendo el tratamiento quirúrgico el método de elección.
El papel del personal de Enfermería es fundamental para el diagnóstico y tratamiento de los pacientes con esta patología. El/la enfermero/a participa en las pruebas diagnósticas, en la educación sanitaria que conforma el tratamiento preventivo y en el tratamiento quirúrgico desarrollando diferentes funciones por mediación de los enfermeros circulantes e instrumentistas.
Palabas clave: Epilepsia; Crisis; Lóbulo temporal; Enfermería.
Abstract and keywords.
Epilepsy is a neurological disease that affects the Central Nervous System (CNS), being the second most prevalent neurological disease; it is manifested by convulsive seizures that are produced by an imbalance between neural excitatory and inhibitory mechanisms mediated by the neurotransmitters glutamate and γ-aminobutyric acid (GABA), respectively. These epileptic seizures can be generalized or focal.
Temporal lobe epilepsy (TLE) is the most common within focal seizures. This pathology can be located unilaterally or bilaterally in temporal lobes, the hippocampal sclerosis being the most usual pathological finding. Epileptogenic focus can be found in the mesial or neocortical structures producing different signs and symptoms. TLE is characterized by resistance to antiepileptic drugs, between 25-40% of the cases, the surgical treatment being the best choice.
Nursing role is essential for the diagnosis and treatment of epileptic patients. Nurses take part in the diagnostic tests, in the health education that forms the preventive treatment and in the surgical treatment carrying out different functions as either circulating nurses or instrumentalist nurses.
Keywords: Epilepsy; Seizures; Temporal lobe; Nursing.

2
2. INTRODUCCIÓN.
La epilepsia ha sido una enfermedad común al ser humano desde hace varios miles de años. Esta enfermedad neurológica ha sido conocida con múltiples denominaciones: morbus sacer, morbus maior, morbus comicialis, etc, y la mayoría de ellas haciendo referencia a su origen divino. Ya en la antigua Mesopotamia (500 a. C) se encontraron documentos en los que se consideraba a los epilépticos como lunáticos y castigados por Dios, e incluso el Código de Hammurabi, por ejemplo, autorizaba devolver a los esclavos epilépticos.
Por el contrario, en esa misma época, Hipócrates (400 a. C) defendió el origen natural de la epilepsia y negaba las teorías iniciales. Areteo de Capadocia, médico griego, criticó a quienes vinculaban la epilepsia con un origen divino y demoniaco.
Ámbitos como la literatura, el cine o la televisión, han contribuido a la divulgación de la enfermedad y, a su vez también, han generado falsas creencias y estereotipos en la sociedad. Dostoievski, Edgar Allan Poe y Vicent Van Gogh, son algunos de los ejemplos de personalidades mundialmente conocidas que padecieron epilepsia (Collado-Vázquez & Carrillo, 2012).
La epilepsia es una enfermedad neurológica, que afecta al Sistema Nervioso Central (SNC), causada por descargas eléctricas descontroladas de neuronas. Esta patología se manifiesta por convulsiones corporales parciales o generalizadas. La epilepsia ha sido motivo de exclusión y estigmatización de personas en todo el mundo y durante largos períodos de tiempo. Actualmente, aún es patente la discriminación que la enfermedad provoca en epilépticos y en sus familias en algunas partes del mundo.
Esta enfermedad es la causante de gran cantidad de incapacitaciones laborales y también, cabe destacar el elevado coste sanitario que generan las pruebas diagnósticas, tratamientos, estancias hospitalarias, cuidados, etc. (Organización Mundial de la Salud, 2015).
2.1. Objetivos generales y específicos.
Esta monografía persigue los siguientes objetivos generales y específicos:
Objetivo general
- Describir la alteración neurofisiológica que desencadena la epilepsia del lóbulo temporal con sus características clínicas y tratamientos; y desarrollar el papel que tiene el personal de Enfermería en la atención a estos enfermos.
Objetivos específicos
- Plasmar datos epidemiológicos, mostrar el proceso de clasificación de los diferentes tipos de epilepsia y definir conceptos básicos para conocer la enfermedad.
- Describir qué son y qué función tienen las señales eléctricas, los canales iónicos y los neurotransmisores, en la producción de crisis epilépticas.
- Explicar los tipos de epilepsia del lóbulo temporal que se pueden presentar, datos epidemiológicos y etiológicos, y explicar las manifestaciones clínicas que son características de esta patología.
- Desarrollar las diferentes pruebas diagnósticas y el tratamiento (preventivo, médico y quirúrgico) de la epilepsia del lóbulo temporal.

3
- Dar a conocer el papel de la Enfermería en las pruebas diagnósticas, y en el tratamiento preventivo y quirúrgico en esta patología.
2.2. Metodología.
Para la realización de esta monografía, se han consultado múltiples bases de datos. Entre ellas PubMed (Medline), Google Académico, CUIDENplus, Índice Médico Español (IME), entre otras. Por último, se ha utilizado la base de datos UpToDate, accesible desde el Hospital Universitario Marqués de Valdecilla (HUMV).
Para la obtención de varios artículos ha sido necesaria la subscripción a algunas páginas web como Enfermería21.com o Neurología.com, teniendo libre acceso a su base de datos.
Otra fuente de consulta ha sido Biblioteca de Ciencias de la Salud de la Universidad de Cantabria.
Una parte de los artículos han sido obtenidos de páginas web especializadas en salud, centrándose en neurología, como la Sociedad Española de Neurología (SEN), la Sociedad Española de Neurocirugía (SENEC), la Organización Mundial de la Salud (OMS), Sociedad Española de Enfermería Neurológica (SEDENE), la Sociedad Española de Neurofisiología Clínica (SENFC) y la International League Against the Epilepsy (ILAE).
La mayoría de los artículos están datados a partir del año 2000, utilizando aquéllos con información contrastada y válida actualmente. Se han desechado artículos experimentales desarrollados en animales.
Los términos DeCS y MeSH utilizados para la búsqueda bibliográfica han sido las siguientes:
- Epilepsia [Epilepsy] - Crisis [Seizures] - Lóbulo temporal [Temporal lobe] - Enfermería [Nursing]
2.3. Descripción de los apartados de la monografía.
A continuación se hará una descripción de los apartados que conforman esta monografía:
La monografía comienza con una breve introducción de la enfermedad y la perspectiva inicial que tenía sociedad sobre la enfermedad, así como el cambio de enfoque que ha ido experimentando en los últimos años.
El apartado 3, como su título indica, se centra en las bases celulares de la epilepsia las cuales son imprescindibles para comprender la alteración neurofisiológica que desencadena las crisis epilépticas. En este apartado se estudian los canales iónicos y neurotransmisores implicados en la generación de crisis epilépticas. Además se desarrollan los diferentes tipos de señales eléctricas y se hace un estudio del efecto epileptógeno.
En el apartado 4 se hace un desarrollo de la epilepsia del lóbulo temporal. Los dos primeros subapartados aportan datos epidemiológicos y etiológicos de la patología, respectivamente. En el tercer subapartado se explican las manifestaciones clínicas de la

4
patología, mientras que en el cuarto se exponen las diferentes pruebas diagnósticas necesarias, y hallazgos frecuentes, para diagnosticar esta patología. En los dos últimos subapartados se explican los diferentes tipos de tratamientos y alternativas para el tratamiento de la epilepsia del lóbulo temporal.
En el apartado 5 se exponen los cuidados de Enfermería. A través de los diferentes subapartados, se describe la atención en diferentes pruebas diagnósticas; las recomendaciones sanitarias que el personal de Enfermería debe dar a los pacientes epilépticos y a sus familiares. En este apartado se evidencia la importancia de la Enfermería en el aspecto de educación sanitaria y prevención de los factores desencadenantes de la epilepsia. Y se explican las funciones que realizan los enfermeros instrumentistas y circulantes dentro del quirófano. Esta monografía finaliza con las conclusiones, referencias bibliográficas y anexos para completar la información.
2.4. Epidemiología.
Dentro de las enfermedades neurológicas más frecuentes, la epilepsia ocupa la segunda posición, detrás del ictus, afectando aproximadamente al 1-2 % de la población (López & Pomposo-Gaztelu, 2010). Actualmente, la Organización Mundial de la Salud (OMS) estima que alrededor de 50 millones de personas padecen epilepsia en el mundo. Cerca del 80 % de los pacientes proceden de regiones en desarrollo. Según datos de la misma organización, la morbilidad de la epilepsia se establece en un 0,75 % (OMS, 2015).
En España se estiman 50 nuevos casos por 100.000 habitantes cada año, por lo que se estima aproximadamente 20.000 casos cada año. El número total de epilépticos en la población española se cifra entre 180.000 y 360.000 (Guía Ápice, 2011).
2.5. Terminología según la International League Against Epilepsy (ILAE).
Uno de los problemas principales dentro del estudio de esta enfermedad ha sido la falta de homogeneidad entre los especialistas respecto a la terminología.
La Liga Internacional contra la Epilepsia o International League Against Epilepsy (ILAE), fundada en 1909, tiene múltiples objetivos como: fomentar la investigación, docencia y formación en epilepsia; desarrollar la calidad de los servicios (diagnóstico, tratamiento, etcétera) y la atención a los pacientes; mejorar en aspectos relacionados con la prevención de la enfermedad; y, contribuir a la difusión del conocimiento sobre la epilepsia (International League Against Epilepy, 2015).
Por ello, uno de los aspectos más importantes desarrollados por la ILAE consiste en consensuar la terminología adecuada. A continuación se presentan definiciones de los conceptos necesarios para el conocimiento de la epilepsia:
- Epilepsia: Es un trastorno cerebral caracterizado por una predisposición persistente para producir crisis epilépticas con las repercusiones que genera a nivel cognitivo, psicológico y social. Para definir la epilepsia es necesario la aparición de una crisis epiléptica como mínimo (Fisher et al., 2005).
- Crisis epiléptica: Es la presencia temporal de signos y síntomas causados por una función defectuosa y sincrónica del cerebro (Fisher et al., 2005).
- Crisis epilépticas generalizadas: Tienen lugar a nivel cortical y subcortical sin incluir necesariamente la totalidad de la corteza cerebral. El comienzo de una crisis puede ser un punto focalizado, sin embargo, la lateralización y localización no es consistente con

5
relación a otra crisis. Estas crisis pueden ser asimétricas (Berg et al., 2010; Berg & Scheffer, 2011).
- Crisis epilépticas focales (Sustituye al término parciales): Son aquéllas que tienen comienzo en zonas limitadas de un hemisferio del cerebro. La localización tiene una amplitud variable. El inicio de la crisis puede ser a nivel subcortical. La propagación de la crisis puede influir sobre el hemisferio cerebral contralateral (Berg et al., 2010; Berg & Scheffer, 2011). En la actualidad estas definiciones tan básicas aún no han sido aceptadas por la totalidad de especialistas en la materia, generándose aún continuos debates.
2.6. Clasificación de las epilepsias según la ILAE.
La clasificación de los diferentes tipos de epilepsias y crisis epilépticas ha supuesto un problema, sujeto a debate, desde finales del siglo XX. En la primera reunión de la ILAE, que tuvo lugar en Kioto en 1981, se realizó la primera clasificación de crisis epilépticas. En esta primera clasificación, basada en datos electrofisiológicos, anatómicos y clínicos, se diferenciaron las crisis epilépticas en: generalizadas, parciales (actualmente conocidas como focales) e inclasificables.
Ocho años más tarde, en la reunión de la ILAE celebrada en Nueva Delhi, se realizó una nueva clasificación focalizada en epilepsias y síndromes epilépticos. En esta última clasificación se categorizan las epilepsias y síndromes epilépticos en: idiopáticas, sintomáticas y criptogénicas.
En 2001 se celebró en Buenos Aires el XXIV Congreso Internacional de la ILAE, en el cual Engel propuso un nuevo planteamiento para la clasificación de los diferentes tipos de epilepsias. Engel estableció cinco ejes para el correcto abordaje de la epilepsia y ocho grupos en los que se clasificaban los diferentes síndromes epilépticos. Es importante destacar que eliminó algunos términos como “criptogénico” para cambiarlo por “probable o presumiblemente sintomático”. Además añadió el síndrome epiléptico benigno, como aquel de fácil abordaje o que no requiere ser tratado. La clasificación de Engel, al igual que las anteriores, ha sido puesta en duda y criticada por otros autores y miembros de la ILAE.
Berg en representación de la Comisión de Clasificación y Terminología de la ILAE planteó, en 2010, la última clasificación con el objetivo de reorganizar y unificar conceptos (Tabla 1). Esta clasificación incluía cambios muy radicales, por lo que fue duramente criticada desde su publicación. Por ejemplo suprimía los términos “epilepsia focal” y “epilepsia generalizada”, pero mantenía los términos “crisis epiléptica generalizada” y “crisis epiléptica focalizada”. Esta nueva clasificación, suprime los términos etiológicos “idiopáticos”, “sintomáticos” y “presumiblemente sintomáticos” por una nueva diferenciación etiológica: epilepsia genética, epilepsia de origen estructural/metabólico y epilepsia de causa desconocida. Por último, Berg definió diferentes tipos de síndromes electroclínicos, constelaciones distintivas y otros tipos de epilepsia (Casas-Fernández, 2012).

6
Tabla 1: Clasificación de las epilepsias.
Clasificación de las crisis epilépticas
Tonicoclónicas Ausencias
Típicas Atípicas Con características especiales Ausencias mioclónicas
Crisis epilépticas generalizadas Mioclonías palpebrales Mioclónicas
Mioclónicas Mioclonicoatónicas Mioclonicotónicas
Clónicas Tónicas Atónicas
Crisis epiléticas focales
Crisis desconocidas
Espasmos epilépticos
Tabla modificada de Casas-Fernández, C. (2012).

7
3. BASES CELULARES DE LA EPILEPSIA.
Las crisis epilépticas pueden ser entendidas, de una manera simple, como un desequilibrio entre los mecanismos excitatorios e inhibitorios dentro de los circuitos neuronales (Stafstrom & Rho, 2014).
Para entender la fisiopatología de la epilepsia es importante conocer el sistema nervioso, así como los canales iónicos y los neurotransmisores implicados en la formación de las crisis epilépticas.
El sistema nervioso se divide en el sistema nervioso central (SNC) y el sistema nervioso periférico (SNP). El primero está compuesto por encéfalo y medula espinal o raquídea, mientras que el segundo se compone de neuronas sensitivas o aferentes y neuronas eferentes.
A nivel celular el sistema nervioso se compone de neuronas y células gliales, glía o neuroglia, también se conocen como células de sostén pese a realizar otras funciones dentro del sistema. Las neuronas, unidades funcionales del sistema nervioso, están formadas por un cuerpo celular o soma, del cual nacen unas prolongaciones encargadas de recibir las señales de entrada, conocidas como dendritas, y otra prolongación, axón, que se encarga de transportar la información una vez elaborada (Silverthorn, 2014).
3.1. Señales eléctricas.
Tanto las células del sistema nervioso como las células del tejido muscular se consideran excitables. Este fenómeno consiste en la generación y transmisión de señales eléctricas, de manera rápida, en respuesta a un estímulo. La base de las señales eléctricas reside en la asimetría de la distribución iónica intracelular y extracelular, Na+, Cl- y Ca++ se encuentran más concentrados a nivel extracelular que intracelular. Mientras que el K+ se encuentra en el líquido intracelular más concentrado que en el extracelular.
Las fluctuaciones en el voltaje que sufre la membrana pueden ser clasificadas en dos tipos de señales eléctricas: potenciales locales y potenciales de acción. El potencial local es una señal eléctrica cuya intensidad fluctúa, viaja distancias cortas y pierde intensidad cuando viaja por la célula. Cuando la intensidad del potencial local es suficiente para alcanzar una zona integradora de la neurona, desencadena un potencial de acción. Los potenciales locales pueden ser excitatorios o inhibitorios, si producen despolarización o hiperpolarización, respectivamente. El potencial de acción es una despolarización breve e intensa que al viajar largas distancias a lo largo de una neurona mantiene íntegro su voltaje.
Las neuronas tienen un potencial de membrana en reposo, aproximadamente, de -70mV. Cuando se produce un potencial de acción este valor alcanza +20 o +30 mV. La generación de un potencial de acción tiene lugar en la zona gatillo. Esta zona gatillo es el cono axónico o parte inicial del axón, también denominada como segmento inicial.
La zona gatillo se caracteriza por una gran concentración de canales de Na+ dependientes de voltaje. Cuando los potenciales locales que llegan a la zona gatillo consiguen la despolarización de la membrana hasta el potencial umbral, aproximadamente -55mV, estos canales de Na+ dependientes de voltaje se abren, la membrana se vuelve más permeable para el Na+ y este ión fluye hacia el interior de la célula despolarizándola. Posteriormente, cuando el potencial de acción alcanza los 30mV, punto máximo del mismo, se produce el cierre de los canales de Na+ y los canales de K+ se abren. Entonces

8
comienza la salida de K+ intracelular, la membrana aumenta su permeabilidad hacia este ión, volviendo a su potencial de reposo, -70mV. Si la permeabilidad hacia el K+ continúa se puede llegar al potencial de equilibrio del K+ (EK) que son aproximadamente -90mV. Este fenómeno se conoce como posthiperpolarización. Al final, los canales de K+ dependientes de voltaje se cierran y se detiene la salida de este ión, lo que unido a la expulsión de Na+, hace que la célula recupere su potencial de membrana de reposo de -70mV y la permeabilidad iónica de reposo (Silverthorn, 2014).
3.2. Canales iónicos.
Para el desarrollo de movimiento o flujo de iones a través de la membrana se utilizan los denominados canales iónicos. Los canales iónicos son una clase amplia y heterogénea de proteínas de membrana que tienen la función de generar y mediar señales en las membranas celulares excitables. Se clasifican en función de la permeabilidad y selectividad para los iones (ej: Canales de Na+, Cl-, Ca++, K+) y también según su respuesta a cambios en el potencial de membrana, a ligandos extracelulares o a segundos mensajeros (Ashcroft, 2000; Armijo, De las Cuevas & Adín, 2000).
Los canales iónicos dependientes de voltaje son activados por cambios en el potencial de membrana que alteran el estado de conformación del canal, lo cual permite el paso selectivo de iones. Los canales iónicos de Na+ y Ca++ dependientes de voltaje, son “excitadores”, despolarizan la membrana celular hacia el potencial de acción. Los canales iónicos de K+ dependientes de voltaje, son “inhibidores”, funcionan hiperpolarizando la membrana celular alejando la posibilidad de generar un potencial de acción (Stafstrom & Rho, 2014).
3.2.1. Canales iónicos despolarizantes dependientes de voltaje.
Los canales de Na+ son complejos formados por subunidades de polipéptidos, en los que se puede encontrar una subunidad α y una o más subunidades β, las cuales son más pequeñas que la anterior e influyen en las propiedades cinéticas de la subunidad α. El tipo de potencial de acción producido en cada célula excitable, está determinado por los tipos de subunidad α y β presentes en la proteína de canal (Catterall, Goldin & Waxman, 2005). Alteraciones genéticas en la estructura del canal de Na+ pueden inducir a la epilepsia generalizada con crisis febriles, síndrome de Dravet, la epilepsia mioclónica severa de la infancia así como otros síndromes epilépticos (Lossin, 2009). El canal de Na+ es el lugar de acción de la mayoría de antiepilépticos que inhibiendo este canal estabilizan la membrana (Armijo et al., 2000). Algunos de estos ejemplos son la fenitoína, carbamazepina y lacosamida (Stafstrom & Rho, 2014).
La activación de los canales de Ca++ tiene como consecuencia un aumento de Ca++ intracelular. La entrada de Ca++ en las neuronas presinápticas facilita la liberación de neurotransmisores, mientras que a nivel postsináptico produce la despolarización mantenida (Herranz, 2002). Hay diferentes subtipos de canales de Ca++ que a su vez tienen diferentes propiedades electrofisiológicas, perfiles farmacológicos, estructura molecular y localización celular (Catterall, Striessnig, Snutch & Pérez, 2003).

9
3.2.2. Canales iónicos hiperpolarizantes dependientes de voltaje.
Los canales iónicos de K+ representan la familia más grande de canales iónicos dependientes de voltaje (Stafstrom & Rho, 2014) y participan en la repolarización e hiperpolarización de la membrana y sus alteraciones pueden inducir una hiperexcitabilidad que facilita las crisis epilépticas (Armijo et al., 2000). El prototipo de canal de K+ dependiente de voltaje está compuesto por 4 subunidades α que atraviesan la membrana y 4 subunidades β que conforman un complejo octamérico que forma un poro iónico selectivo. Parte de las propiedades de anticonvulsivos como topiramato o levetiracetam incluye la acción sobre los canales de K+ (Stafstrom & Rho, 2014). El anticonvulsivo retigabina actúa abriendo y activando los canales de K+ dependientes de voltaje (Stephen & Brodie, 2011).
Estos canales juegan un papel relevante en el desarrollo de las crisis epilépticas.
3.3. Neurotransmisores.
Los neurotransmisores son moléculas que participan en una sinapsis y provocan una respuesta en la célula receptora de los mismos. Atendiendo a su estructura química se agrupan en siete tipos: acetilcolina, aminas, aminoácidos, purinas, péptidos, lípidos y gases (Silverthorn, 2014). De todos ellos, los que tienen más relevancia en el proceso epiléptico son los aminoácidos glutamato y ácido γ-aminobutírico (GABA). A continuación se estudiarán ambos aminoácidos:
1. El aminoácido glutamato es el principal neurotransmisor excitatorio del sistema nervioso central. Las sinapsis glutamatérgicas están extendidas a lo largo del cerebro y su actividad excitatoria es imprescindible para un correcto desarrollo cerebral (Simeone, Sanchez, & Rho, 2004).
Dentro de los receptores glutamatérgicos se pueden encontrar dos clases: receptores ionotrópicos (1.1) y metabotrópicos (1.2) (Herranz, 2002).
1.1. Dentro de los receptores ionotrópicos se pueden diferenciar dos tipos: a) Receptores NMDA que se activan por N-metil-D-aspartato y glutamato.
Muestran permeabilidad al Na+ y K+, y se bloquean por el Mg+ (Herranz, 2002). Aparte de tener una zona de unión para el glutamato o NMDA, posee un sitio para el reconocimiento de diferentes moduladores como glicina, zinc o poliaminas. Cuando la membrana se despolariza, los receptores NMDA para los iones de Mg+ se cierran, y como consecuencia los receptores NMDA se activan y hay afluencia de iones de Ca++ y Na+ que generan un potencial postsináptico excitatorio (PEPS) lento y duradero (Stafstrom & Rho, 2014).
b) Receptores No-NMDA divididos en dos subtipos: ácido α-amino-3-hidroxi-5-metil-4-isoxazolpropiónico o AMPA y los receptores KA. Los receptores AMPA se activan por amino-hidroxi-5-metil-isoxazol-propionil y glutamato, mientras que los receptores KA se activan por kainato, domoato y glutamato. Ambos tipos de receptores No-NMDA son permeables al Na+ y K+, y presentan escasa permeabilidad al Ca++ (Herranz, 2002).
1.2. Los receptores glutamatérgicos metabotrópicos que no forman canales iónicos representan una extensa familia de receptores asociados a proteínas G. Estas proteínas activan varios mecanismos de transducción y son moduladores de los canales iónicos de Ca++ y K+ dependientes de voltaje y canales catiónicos no selectivos (Conn, 2003).

10
2. El ácido γ-aminobutírico (GABA) es el neurotransmisor inhibitorio más extendido en el sistema nervioso central encontrándose en un 30% de las sinapsis del mismo sistema (Pereno, 2010). Después de la liberación de los terminales axónicos, el GABA se une a una de las dos clases de receptores, GABA-A y GABA-B, encontrados en la mayoría de los receptores corticales. Los receptores GABA-A también han sido encontrados en la glía aunque su función no es totalmente conocida. Se debe destacar que los circuitos hipocampales inhibitorios utilizan este aminoácido (Stafstrom & Rho, 2014). - Los receptores GABA-A consisten en un complejo macromolecular que forma
un canal iónico que tiene un lugar para la unión de agonistas y moduladores alostéricos como barbitúricos o benzodiacepinas que afectan a las propiedades cinéticas de los receptores (Sigel & Steinmann, 2012).
- Los GABA-B se encuentran en la membrana postsináptica y en los terminales presinápticos. Actúan controlando los canales de Ca++ y K+ utilizando segundos mensajeros unidos a proteínas-GTP (Simeone, Donevan & Rho, 2003).
3.4. Estudio electrofisiológico de la epilepsia.
El estudio de las señales eléctricas en el SNC es una de las bases fundamentales en el estudio de la epilepsia. La despolarización paroxística (PDS; paroxysmal depolarization shift) es el signo electrofisiológico característico de las descargas epileptógenas interictales (DEI) (Pastor, Menéndez de la Prida, Hernando & Sola, 2006). El PDS es un hallazgo electrofisiológico que ocurre en una única neurona (Fig. 1A). Las DEI son la actividad sincrónica de varios millones de neuronas despolarizándose paroxísticamente (Fig. 1B.). Se requieren aproximadamente, como mínimo, 6 cm2 de la corteza cerebral para que ocurra este evento (Stafstrom & Rho, 2014).
El PDS consiste en una despolarización de alto voltaje sobre la que se observan ráfagas de potenciales de acción de gran frecuencia, seguida de una intensa y prolongada hiperpolarización (Dichter & Ayala, 1987; Kandel, Schwartz & Jessell, 2000). La duración de la despolarización paroxística es de varios cientos de milisegundos (Stafstrom & Rho, 2014). Este fenómeno ocurre de manera sincrónica en un gran número de neuronas dando lugar a las descargas epileptógenas interictales (DEI) (Dichter & Ayala, 1987; Kandel et al., 2000).
Figura 1: Señales eléctricas características de la epilepsia. A) Despolarización paroxística. B) Descargas epileptógenas interictales (DEI). Schiller, Y. (2002).

11
La despolarización inicial está mediada por la acción del glutamato sobre los receptores AMPA mientras que la fase de despolarización sostenida depende de la activación de los receptores NMDA. La despolarización paroxística termina con un período prolongado de hiperpolarización mediado principalmente por corrientes inhibitorias de K+ y Cl-, iones que se mueven a través de canales de K+ dependientes de voltaje y de receptores GABA respectivamente (Stafstrom & Rho, 2014).
El fenómeno epileptogénico se fundamenta en tres pilares comunes (Herranz & Forcadas, 2012):
- Capacidad de determinados grupos neuronales para sufrir cambios paroxísticos de despolarización (PDS, paroxysmal depolarization shift).
- Incremento de la función excitadora glutamatérgica. - Disminución de la función inhibidora gabaérgica, lo cual produce una desinhibición.

12
4. EPILEPSIA DEL LÓBULO TEMPORAL.
Entre las diferentes presentaciones de epilepsias conocidas, las crisis focales representan el 50% de los casos, aproximadamente (Thom, Sisodiya & Najm, 2008). La epilepsia del lóbulo temporal (ELT) es el tipo más frecuente de epilepsias desarrolladas (Benbadis, 2014) (Figs. 2 y 3). En 1986, Schwartzkroin postuló que “El lóbulo temporal es la región más epileptogénica del cerebro humano”. De todas las regiones descritas dentro del lóbulo temporal solo se aceptan, en la actualidad, dos áreas epileptógenas: el área temporal mesial y temporal neocortical (Bercovici, Kumar & Mirsattari, 2012).
4.1. Epidemiología.
Dentro de los tipos de epilepsia temporal, la epilepsia del lóbulo temporal mesial tiene una frecuencia del 90% frente al 10% restante de la epilepsia del lóbulo temporal neocortical (Téllez-Zenteno & Ladino, 2013). Cabe destacar que existen pocos datos bien fundamentados referentes a la epidemiologia de la epilepsia del lóbulo temporal.
Diferentes artículos relatan que aproximadamente el 80% de los pacientes que acudían a centro de cirugía de la epilepsia presentaban ELT, siendo el 20% restante epilepsias extratemporales. Dentro del grupo de las epilepsias extratemporales, la epilepsia del lóbulo frontal es la más común (Téllez-Zenteno, Wiebe & López-Méndez, 2010).
4.2. Etiología.
El origen de la epilepsia del lóbulo temporal puede ser esporádico o familiar. Las diferentes causas descritas que pueden provocar la ELT son la esclerosis hipcocampal (EH), lesiones glióticas secundarias a infecciones o traumatismos, malformaciones congénitas y vasculares y, tumores en estadio inicial (Cendes, 2005).
La esclerosis hipocampal (EH), puede recibir el nombre de esclerosis mesial temporal (EMT), es el hallazgo más comúnmente encontrado en la ELT. Los estudios revelan una
Figura 3: Vista sagital del encéfalo. López, J.E. (2008).
Figura 2: Vista lateral externa del lóbulo temporal derecho. Cairós, M. (s.f.)

13
pérdida neuronal en el hipocampo, predominantemente en las áreas CA1, CA3 y CA4 del cuerpo o asta de Ammon y giro dentado, siendo relativamente escasa la pérdida en la región CA2 (Figs. 4 y 5). En la mayor parte de los casos la esclerosis hipocampal es unilateral, siendo posible la afectación bilateral aunque en menor porcentaje (Benbadis, 2014). El desarrollo de la esclerosis del hipocampo se ha asociado en múltiples casos a crisis febriles en el nacimiento y en la infancia (Monge-Galindo et al., 2010). Cuando se prolongan las crisis febriles se puede producir un edema hipocampal que acabe produciéndo una esclerosis del hipocampo (Tatum, 2012).
La ILAE realizó una clasificación sobre los diferentes suptipos de EH (Benbadis, 2014):
- Esclerosis hipocampal Tipo 1: Se caracteriza por una severa pérdida neuronal y gliosis en las áreas CA1 y CA4. El área CA1 es el más afectado con una pérdida neuronal >80%. Las otras áreas también muestran hallazgos patológicos. Entre el 60-80 % de los pacientes sometidos a resección quirúrgica se incluyen en este subtipo.
- Esclerosis hipocampal Tipo 2: Se caracteriza por una severa pérdida celular en el área CA1 con escasa población neuronal en las áreas CA2, CA3 y CA4.
- Esclerosis hipocampal Tipo 3: Se caracteriza por una pérdida neuronal >50 % en el área CA1 sin escasa pérdida en las otras regiones.
En algunas ocasiones se ha detectado que el hipocampo no sufre esclerosis y lo único apreciable es la gliosis y la pérdida neuronal (Blümcke et al., 2013).
Las malformaciones vasculares que se han asociado con mayor frecuencia a la epilepsia han sido los angiomas cavernosos y las malformaciones arteriovenosas (Téllez-Zenteno & Ladino, 2013).
En 1988 Daumas-Duport y otros describen los tumores neuroepiteliales disembroblásticos. Dichos tumores, están relacionados con crisis focales, muestran preferencia por el lóbulo temporal pero no son exclusivos de éste. Es un tumor que la OMS clasifica de bajo grado o grado 1 pero que puede evolucionar de estadio. Los gangliomas son los tumores más frecuentes en la ELT. Este tumor puede ir asociado a patología dual como es la esclerosis del hipocampo. Al igual que en el caso de los tumores neuroepiteliales disembroblásticos, los gangliomas son tumores grado 1 según la OMS pese a que se han encontrado casos de grado 3 (López & Pomposo-Gaztelu, 2010).
Figura 5: Cuerno de Ammon. Department of Pathology, University of Oklahoma Health Sciences Center. (s.f.)
Figura 4: Hipocampo. Claro Mader, E. (2015).

14
Las lesiones glióticas es posible que se desarrollen posteriormente episodios de hipoxia neonatal y en pacientes que tengan historia previa de cirugía cerebral, traumatismo o infección (Téllez-Zenteno & Ladino, 2013).
4.3. Manifestaciones clínicas.
Dentro de las manifestaciones clínicas que se presentan en la epilepsia del lóbulo temporal mesial y neocortical, existen diferencias de las cuales las más relevantes serán estudiadas a continuación (Anexo I).
La epilepsia del lóbulo temporal mesial afecta al hipocampo, amígdala y al giro parahipocampal (Benbadis, 2014). Las manifestaciones clínicas, por lo general, se presentan de una manera clara en los pacientes. Las auras aparecen en el 80% de los pacientes con esta patología siendo las viscerosensoriales las más comunes. Las auras viscerosensoriales se acompañan de sensación de miedo, ansiedad y déjà vu. A estas manifestaciones se le suma una sensación epigástrica indescriptible, y automatismos orales y manuales acompañados de una afectación de la conciencia durante 30-60 segundos (Tatum, 2012). Se conoce como “aura” al evento, de la crisis epiléptica, que ocurre previo de la pérdida de conciencia y que se recuerda después (Fernández-Torre, 2002). El malestar epigástrico forma parte de las auras autonómicas y puede ser un malestar estático en la región epigástrica, ascender a la región torácica y de la garganta, o descender a la región hipogástrica (Thompson, Duncan & Smith, 2000). Otras manifestaciones frecuentes en este tipo de epilepsia son la midriasis, piloerección y taquicardia (Tatum, 2012).
Por otro lado, la epilepsia del lóbulo temporal neocortical está asociada a anormalidades en el neocortex de la región temporal que pueden estar causadas por malformaciones vasculares o daños traumáticos cerebrales (Benbadis, 2014). Con respecto al tipo anterior, en la epilepsia del lóbulo temporal neocortical los pacientes manifiestan el aura en el 60% de los casos aproximadamente. Los auras son de típico auditivo, somatosensorial y psíquico, continuada con la interrupción de la actividad motriz, mirada fija y ausencia de respuesta y posterior actividad contralateral. Las auras psíquicas, originadas en el neocortex de la región temporal, más habituales son las percepciones de jamais vu o déjà vu. En este tipo de epilepsia, la generalización secundaria de la crisis es habitual a diferencia de la epilepsia del lóbulo temporal mesial (Téllez-Zenteno & Ladino, 2013).
Otras manifestaciones clínicas diferenciadoras de los dos tipos de epilepsia del lóbulo temporal, y de otros tipos de epilepsias, permite la clasificación diagnóstica en esta patología (Anexo II).
4.4. Diagnóstico de la epilepsia del lóbulo temporal.
Para realizar un diagnóstico certero de la epilepsia se debe efectuar en primer lugar una anamnesis. Elaborar una historia clínica es fundamental para organizar cada caso de estudio, así como para la obtención de pruebas diagnósticas y elección del tratamiento más adecuado. Los errores principales en el diagnóstico de la epilepsia son la confusión de la epilepsia con otro episodio paroxístico, o viceversa, y la clasificación errónea del tipo de epilepsia (Piña-Astete et al., 2011).

15
4.4.1. Historia clínica
La historia clínica (HC) es el documento médico-legal que surge de la relación establecida entre el médico y el paciente y en el que se recoge la información necesaria para el correcto desarrollo de la labor asistencial. Cuando nos enfrentamos a enfermedades que se manifiestan con episodios paroxísticos, la HC es el instrumento inicial que debe establecer el diagnóstico diferencial (DD) y guiar el proceso diagnóstico (Casas Fernández & Serrano Castro, 2012). Muchas veces en este tipo de enfermedad neurológica no es suficiente con una entrevista al paciente si no que es necesario interrogar a testigos que expliquen cómo ha sido la crisis, graben un vídeo o incluso hagan una simulación de la misma. Reconocer las características clínicas del paciente es imprescindible para la selección de estudios diagnósticos que permitan la localización de la lesión en pacientes candidatos a tratamiento quirúrgico (Jan & Girvin, 2008).
A continuación se muestran los pilares centrales que ha de tener una correcta historia clínica (Casas-Fernández & Serrano Castro, 2012):
o Anamnesis. o Antecedentes personales. o Antecedentes familiares. o Enfermedad actual.
Las pruebas complementarias para el diagnóstico de la epilepsia son las siguientes (Mercadé Cerdá, Mauri Llerda & López González, 2012):
- Analítica general en sangre, orina y líquido cefalorraquídeo (LCR): son útiles a la hora de establecer un diagnóstico diferencial con otro tipo de enfermedades, por ejemplo metabólicas.
- Electrocardiograma (ECG): se realiza para descartar enfermedad de origen cardíaco. - Test genéticos: debido a que se han detectado epilepsias, parciales y generalizadas,
de origen genético. - Electroencefalograma/Vídeoelectroencefalograma. - Neuroimagen craneal. - Test neuropsicológico: evaluación de alteraciones cognitivas en áreas como el
lenguaje y la memoria.
Destacar que para el diagnóstico de la ELT es necesario aún de más estudios complementarios que serán desarrollados a continuación.
4.4.2. Electroencefalograma (EEG)/Videoelectroencefalograma (VEEG).
El psiquiatra alemán Hans Berger (1929) desarrolló (1873-1941) la electroencefalografía que ha sido de vital importancia para el diagnóstico y tratamiento de la epilepsia. Para ello se sitúan los electrodos de registro en el cuero cabelludo siguiendo una organización consensuada (Fig.6). Los estudios de Gibbs, Davis y Lennox (1935) detectaron la presencia de complejos de punta-onda interictales durante las crisis de ausencia. En estudios posteriores se afirmó la presencia de puntas epileptógenas en las epilepsias focales (Gibbs, Lennox & Gibbs, 1936; Jasper, 1936).
A todos los pacientes con ELT se les debe realizar un EEG despiertos y con privación del sueño (Foldvary et al., 2001). En algunos casos el EEG puede ser normal, por lo que el uso del videoelectroencefalograma se realizará en todos los pacientes con ELT candidatos a cirugía (Binnie et al., 1981) y cuando sea necesario corroborar el diagnóstico de ELT (Chen, Mitchell, Horton & Snead, 1995).

16
Figura 6: Sistema de colocación de electrodos según versión europea.
Barea, R. (s.f.)
Las puntas u ondas agudas temporales anteriores con voltaje máximo F7/F8 es la anormalidad interictal más reconocido en pacientes con epilepsia del lóbulo temporal mesial, estando presente en el 94% de los casos. Si el foco es neocortical, las puntas son visibles en T3/T4 (zona mediotemporal) y T5/T6 (zona temporal posterior). Las puntas interictales tienen un valor predictivo del foco epileptógeno superior al 95%, y hasta un 30% de los pacientes pueden presentar descargas bitemporales interictales independientes. La presencia de descargas epileptógenas interictales es más frecuente en pacientes con epilepsia del lóbulo temporal que en pacientes con epilepsias extratemporales. En el EEG se han encontrado anormalidades interictales que hacen sospechar de ELT, como la actividad delta arrítmica presente en el 66% de estos pacientes; este hallazgo tiene un valor localizador similar al que tienen las puntas temporales. Por otro lado la actividad delta rítmica temporal intermitente es, si cabe, más específico encontrándose en el 80% de los casos asociado a epilepsia, dicha actividad involucra estructuras mesiales temporales siendo un hallazgo fiable (Téllez-Zenteno & Ladino, 2013) (Figs. 7 y 8).
En los pacientes con epilepsias extratemporales predominan frecuencias rápidas en los rangos beta y alfa de la actividad rítmica, mientras que en los pacientes con ELT son más comunes las frecuencias delta y theta. La sensibilidad de esta prueba es generalmente del 91% en pacientes con ELT, por otro lado, es de 72% en pacientes con epilepsias extratemporales (Foldvary et al., 2001). En la epilepsia temporal mesial se ha observado actividad rítmica de 5-10 Hz y en la epilepsia neocortical 2-5 Hz (Jan, Sadler & Rahey, 2010).

17
Figura 7: Electroencefalograma basal. Saiz Díaz, R.S. (2012).
Figura 8: EEG que muestra actividad epiléptica en región temporal izquierda tipo onda aguda-onda lenta. Sánchez, J., Centanaro, M., Solís, J., Valle, C. (2009).
4.4.3. Resonancia magnética (RM).
La resonancia magnética es una prueba de gran trascendencia para el estudio de pacientes con diagnóstico de ELT, y especialmente, aquellos potenciales de ser tratados mediante cirugía (Spencer, 2002) (Fig. 9). En ocasiones los resultados de la prueba son negativos pero tras la resección del lóbulo temporal, entre un 40-50% de los pacientes no vuelven a sufrir crisis (Cohen et al., 2006).

18
Figura 9: Imagen de resonancia magnética de un paciente con epilepsia del lóbulo temporal. Krauss, G.L. (2013).
La RM es una prueba muy sensible en la localización de la esclerosis del hipocampo, además es importante el estudio de la zona mesial, la zona parahipocampal y la amígdala (Woermann & Volmar, 2009).
Los descubrimientos más importantes son: atrofia del hipocampo (95%), hiperintensidad hipocampal en T2 (85%) y FLAIR. Otros hallazgos que se deben valorar son las pérdidas superficiales y en la estructura interna (60-95%), hipointensidades en la secuencia T1 (10-95%) (Wieser, 2004).
Los especialistas en esta técnica señalan que se debe prestar atención a las secuencias T2 y FLAIR (Woermann & Volmar, 2009).
4.4.4. Tomografía de emisión de fotón simple (SPECT).
Esta prueba es utilizada para encontrar el foco epileptogénico detectando el flujo sanguíneo cerebral (Fig. 10).
Figura 10. SPECT del encéfalo de un paciente con epilepsia del lóbulo temporal durante fase ictal. Rohit Bakshi, M.D. (2006).
La prueba se realiza en la fase ictal o posctical comparándose con la SPECT en fase interictal. La inyección de los elementos específicos, radioisótopos Tecnecio-99-HMPAO y Tecnecio-99-ECD (Van Paesschen, Dupont, Sunaert, Goffin & Van Laere, 2007), en el SPECT ictal se realiza cuando comienza la crisis epiléptica y las imágenes gammagráficas se obtienen cuando ésta finaliza (Setoain et al., 2012). Esta prueba es utilizada fundamentalmente en la valoración quirúrgica (Van Paesschen et al., 2007).

19
Se trata de una prueba de alto coste y no muy disponible. Para su realización requiere la hospitalización del paciente y la suspensión del tratamiento de fármacos antiepilépticos, así como vigilancia ante la aparición de crisis (Reis, 2008).
4.4.5. Tomografía por emisión de positrones (PET).
La utilidad de esta prueba reside en identificar áreas de hipometabolismo (de la zona epileptógena) en fase interictal (Fig. 11). El radioligando más utilizado es el 18-fluorodesoxiglucosa.
Figura 11: PET normal (izquierda) y PET anormal (derecha) con hipometabolismo temporal bilateral. Inan Akman, Cigdem. (s.f.).
La indicación de esta prueba es en aquellos casos de epilepsia focalizada sin lesiones o sin concordancias. Esta prueba, como ocurre con la prueba SPECT, tiene un uso de carácter adicional, no definitivo, en pacientes candidatos a cirugía. En pacientes con una RM normal, la prueba PET alcanza una precisión para localizar el foco del 80%. (Téllez-Zenteno & Ladino, 2013). Dentro de las pruebas de imagen funcional para la ELT, la PET es la más aconsejable, debido a que no requiere de ingreso en hospital ni retirar la medicación (Álvarez-Linera, Bargalló & Setoain, 2012). La sensibilidad diagnóstica de la prueba para los casos de ELT es del 86% y de un 67% para los casos de epilepsia extratemporal (Casse, Rowe, Newton, Berlangieri & Scott, 2002).
4.4.6. Substraction Ictal SPECT Co-registered to MRI (SISCOM).
Esta técnica consiste en combinar las pruebas diagnósticas SPECT y RM, y es útil tanto en casos de epilepsia temporal como de extratemporal. Diferentes estudios han revelado, además, la efectividad del uso de la prueba SISCOM en pacientes con epilepsia no lesional o no concordante (Téllez-Zenteno & Ladino, 2013).
4.4.7. Electrodos intracraneales.
Este procedimiento está indicado cuando existe incongruencia entre los resultados de las imágenes obtenidas con las pruebas descritas y el EEG. Dentro de este método diagnóstico se pueden encontrar dos variedades dependiendo de su colocación: los electrodos subdurales y los electrodos profundos. Los electrodos subdurales, implantados quirúrgicamente a través de un orificio en el cráneo, realizan un registro del córtex cerebral. El otro tipo de electrodos intracraneales, los electrodos profundos,

20
tienen la capacidad de registrar zonas que no cubren los electrodos subdurales como son la amígdala, la ínsula, el hipocampo, la corteza entorrinal, el polo occipital, la unión occipitotemporal y la unión parietotemporal.
Los resultados obtenidos en estudios que comparaban los electrodos subdurales y los electrodos profundos no han mostrado una ventaja de uno sobre otro, por lo que la elección depende de cada centro. Ambos métodos detectan cambios eléctricos que tienen lugar a escasos milímetros de su colocación mientras que los electrodos superficiales del EEG detectan cambios en amplias regiones del córtex.
El uso de electrodos posee unas ventajas como la oportunidad de realizar una estimulación de la corteza cerebral con el objetivo de mapear el lenguaje, conseguir una mejor resolución espacial y la reducción de artefactos en el electroencefalograma. Sin embargo, la posibilidad de no detectar el foco epileptógeno, limitado muestro del córtex y otras complicaciones, son algunas de las desventajas de estos métodos (Téllez-Zenteno & Ladino, 2013).
La utilidad de los electrodos incraneales puede tener provecho en los siguientes casos clínicos (Téllez-Zenteno & Ladino, 2013):
- Cuando la lesión se halle en un lóbulo temporal pero las crisis epilépticas y las descargas se detecten en el lóbulo temporal contralateral a la lesión.
- Escenarios clínicos en los que el VEEG muestre actividad epileptiforme en ambos lóbulos temporales. En estos casos se busca localizar el lado dominante para el inicio de la crisis epiléptica y en caso afirmativo se lleva a cabo la resección de la zona, y en el caso opuesto se desecharía la opción de la cirugía resectiva.
- Pacientes con epilepsias multifocales y cuyo inicio crítico sea de origen dubitativo. - En casos donde se aplique la técnica resectiva y se deba mantener intacta la región
del lenguaje. - Casos en los que únicamente sea necesaria la resección hipocampal manteniendo
intacta las zonas neocorticales. - Casos en los que el procedimiento sea una lesionectomía.
Se estima que este procedimiento es innecesario en el 60-85% de los casos de ELT candidatos a tratamiento quirúrgico (Holmes, Miles, Dodrill, Ojemann & Wilensky, 2003).
4.4.8. Test neuropsicológicos.
La evaluación neuropsicológica es una ayuda para descubrir la localización y lateralización de áreas cerebrales dañadas y que pueden guardar relación con el inicio de las crisis epilépticas. El resultado de la prueba no va enfocado al diagnóstico de la epilepsia, si no a conocer la alteración o no de las capacidades cognitivas del paciente (Maestú, Martin, Gil-Nagel, Franch & Sola, 2000).
En los casos de ELT dominante, los pacientes presentan alteración en la memoria verbal, mientras que en los casos de ELT no dominante la alteración es más notable en la memoria visuoespacial. Contribuye para conocer la dominancia del lenguaje, pese a que en la actualidad se esté utilizando más la resonancia magnética funcional (RMf) ya que puede lateralizar el lenguaje y otras áreas del córtex (Téllez-Zenteno & Ladino, 2013).
Un elemento útil para lateralizar el lenguaje y examinar la cognición del paciente prequirúrgico y postquirúrgico es el test de Wada. Esta prueba es una técnica invasiva por lo que hay que tener en cuenta posibles complicaciones y posibles riesgos para el paciente (Sharan, Ooi, Langfitt & Sperling, 2011). El test de Wada es útil en aquellos

21
pacientes con ELT, hipocampo no atrófico y sin déficits de memoria (Carreño & Serratosa, 2012).
4.5. Tratamiento.
Los dos objetivos principales del tratamiento de un paciente epiléptico son las siguientes: prevenir los desencadenantes de las crisis epilépticas y eliminar las mismas mediante un tratamiento médico o quirúrgico.
4.5.1. Tratamiento preventivo.
Para realizar esta prevención de factores desencadenantes de crisis epilépticas, Albert Molins Albanell (2013) postula las siguientes pautas:
Intentar mantener un descanso nocturno diario de 7-8 horas de forma regular. Evitar el abandono del tratamiento antiepiléptico. Evitar el olvido de dosis del tratamiento antiepiléptico. Evitar el consumo de drogas excitantes (anfetaminas, cocaína, etcétera). Evitar el consumo excesivo de alcohol. Evitar situaciones de intenso estrés emocional. Evitar aquellos estímulos luminosos intermitentes, como la televisión o las
discotecas, en los que se haya detectado fotosensibilidad en electroencefalograma.
4.5.2. Tratamiento médico.
El abordaje farmacológico de la epilepsia y de las crisis epilépticas se basa en las propiedades farmacológicas, mecanismo de acción y farmacocinética, de los fármacos antiepilépticos (FAE) (Herranz & Forcadas, 2012). Es necesario destacar que el 40% de los casos de epilepsia focal muestran un efecto refractario al tratamiento farmacológico y serán, en potencia, candidatos a intervención quirúrgica (Kwan & Sander, 2004).
Al igual que para tratar otro tipo de epilepsias, es preferible la monoterapia. El objetivo principal del tratamiento farmacológico contra la epilepsia es suprimir las crisis. En caso de que un fármaco antiepiléptico no sea eficaz, se podrá recurrir a la politerapia. La respuesta del paciente ante el primer antiepiléptico sirve para predecir la respuesta al tratamiento farmacológico (Kwan & Brodie, 2000).
El mecanismo de acción de los fármacos antiepilépticos son los siguientes (Herranz & Forcadas, 2012):
• Inhibir o bloquear los canales de Na+. • Inhibir o bloquear los canales de Ca++. • Inhibir los receptores glutamatérgicos (NMDA, AMPA y kainato). • Potenciar los canales de K+. • Potenciar los receptores gabaérgicos de clase GABA-A y GABA-B.
Los FAE se pueden clasificar en: FAE de 1º, 2º y 3º generación (Tabla 2):

22
Tabla 2: Clasificación de los fármacos antiepilépticos (FAE).
FAE de 1º generación FAE de 2º generación FAE de 3º de generación
- Carbamacepina - Clobazam - Clonazepam - Etosuximida - Fenitoína - Fenobarbital - Primidona - Valproato
- Gabapentina - Levetiracetam - Lamotrigina - Oxcarbazepina - Pregabalina - Tiagabina - Topiramato - Zonisamida
- Lacosamida - Retigabina - Eslicarbazepina - Rufinamida
Tabla modificada de Herranz, J.L., Forcadas, M.I. (2012).
A nivel farmacocinético, los antiepilépticos ideales se caracterizan por una absorción rápida por vía oral, nula o escasa asociación con proteínas plasmáticas, no se produce una metabolización hepática, ausencia de interacciones con otros fármacos y ausencia de metabolitos activos, cinética lineal, vida media de eliminación prolongada y eliminación vía renal. Siguiendo estas premisas farmacocinéticas de un FAE ideal, los fármacos de primera generación serían los más desaconsejados. Los FAE de 2º y 3º generación, son los que menos interacciones tienen con respecto a otros antiepilépticos, siendo los FAE de 1º generación los que más interacciones presentan (Herranz & Forcadas, 2012).
4.5.3. Tratamiento quirúrgico.
La cirugía de la epilepsia tiene como objetivo eliminar o disminuir el número de crisis epilépticas que sufre el paciente. La cirugía resectiva curativa consiste en eliminar el foco epileptógeno, y por consiguiente las crisis epilépticas, sin causar daños o déficits al paciente. Cuando la cirugía resectiva curativa no es viable, existen otras opciones como la cirugía resectiva paliativa, la estimulación vagal o estimulación cerebral profunda (Carreño & Serratosa, 2012). Cuando la cirugía se realiza de forma exitosa, la calidad de vida del paciente aumenta y se reducen los gastos en FAEs y estancia hospitalaria (Unwonge, Wehner & Foldvary-Schaefer, 2010). La cirugía se aplica en casos de epilepsias temporales y epilepsias extratemporales, pese a que son más exitosas las primeras (López & Pomposo-Gaztelu, 2010). Dentro de las crisis focales, el caso más dificultoso de tratar es la ELT mesial, ya que solo se controla con tratamiento médico un 25-40% de los casos (Spencer, 2002).
Para realizar el tratamiento quirúrgico de la epilepsia se deben cumplir las siguientes premisas (Carreño & Serratosa, 2012):
- Epilepsia refractaria al tratamiento o farmacorresistente. - Epilepsia abordable quirúrgicamente.
La ILAE definió la epilepsia refractaria o resistente a fármacos antiepilépticos como “aquella en la cual se ha producido el fracaso a dos ensayos de FAE, en monoterapia o en combinación, tolerados, apropiadamente elegidos y empleados de forma adecuada, para conseguir la ausencia mantenida de crisis”. Lo que supone que el paciente no presente crisis epilépticas en un período de 12 meses (Kwan et al., 2010).

23
También se ha de valorar cómo interfieren las crisis epilépticas en la vida del paciente, así como los efectos secundarios que los FAE producen. Además, la evolución de la enfermedad debe ser de al menos dos años, en caso de que haya amenaza para la vida o sean casos de niños, el período será inferior a dos años (Sánchez-Álvarez, Serrano Castro & Cañadillas Hidalgo, 2002).
El Dr. José Ignacio López y el Dr. Iñigo Pomposo-Gaztelu (2010) postulan que las causas de la epilepsia refractaria son las siguientes: esclerosis del hipocampo, displasias corticales, patología dual (esclerosis del hipocampo y displasia cortical), diferentes tipos de neoplasias (tumor neuroepitelial disembroblástico, ganglioglioma, astrocitomas, etcétera), malformaciones vasculares, hamartomas y encefalitis de Rasmussen.
4.5.3.1. Técnicas resectivas.
Las técnicas quirúrgicas resectivas pueden ser la cirugía curativa y la cirugía paliativa. El primer tipo tiene como objetivo la eliminación de las crisis epilépticas. La cirugía paliativa, a diferencia, tiene como objetivo mejorar las crisis epilépticas (Carreño & Serratosa, 2012).
Los síndromes epilépticos que pueden ser abordados mediante cirugía curativa son los siguientes:
- Epilepsia del lóbulo temporal medial secundaria a esclerosis del hipocampo. En este caso, la intervención precisa es la amigdalohipocampectomía acompañándose de la lobectomía temporal anterior. Posterior a la intervención quirúrgica, dos tercios de los pacientes, aproximadamente, quedan libres de crisis epilépticas.
- Epilepsia neocortical con una única lesión circunscrita. La intervención quirúrgica recibe el nombre de lesionectomía, y es guiada por RM, lo cual es suficiente para localizar la zona epileptógena. La zona epileptógena comúnmente se sitúa en la proximidad de la lesión. Cuando la lesión se sitúa a nivel temporal, el porcentaje de pacientes que quedan libres de crisis después de la cirugía es similar al caso anterior. Sin embargo, este porcentaje es menor a lesionectomía extratemporal (Devaux et al., 2008).
- Síndromes de epilepsia hemisféricos (hemimegalencefalia, síndrome de Sturge-Weber, síndrome de Rasmussen y otras epilepsias unilaterales). Se aplica la técnica hemisferectomía funcional o hemisferotomía. Dependiendo de la patología, se alcanzan unos resultados exitosos comprendidos entre el 60-80% de pacientes libres de crisis.
- Epilepsias neocorticales sin lesión única circunscrita, las cuales tienen peor resultado tras la intervención quirúrgica. Dicha cirugía se realiza en casos de patología dual, lesiones mal circunscritas en el neocortex y en casos de epilepsia no lesional (no se observa lesión en las pruebas de neuroimagen). En el caso de la epilepsia no lesional, se utilizan como guía las pruebas de neuroimagen funcional para la posterior colocación de electrodos intracraneales que servirán para localizar la zona epileptógena. Tiene mejor pronóstico postquirúrgico esta cirugía en los casos de epilepsia temporal que extratemporal alcanzándose un 60% de pacientes libres de crisis contra un 35%, respectivamente.
Como se desarrolla con anterioridad, en ocasiones no es posible llevar a cabo la cirugía curativa, y se debe desarrollar la cirugía paliativa cuyo objetivo es mejorar las crisis epilépticas (Carreño & Serratosa, 2012):
- Resección subpial múltiple: indicada en algunos casos como el síndrome de Landau-Kleffner. Buscando los mejores resultados y tras un seguimiento de 4 años, un 55% de los pacientes quedaban libres de crisis y un 4% de déficits continuos (Sociedad Española de Neurocirugía, 2009).

24
- Callostomía: consiste en seccionar de manera parcial o total el cuerpo calloso. Es una intervención posible en aquellos pacientes que sufren crisis epilépticas y caídas, con una mejora del 70% de los pacientes (SENEC, 2009).
4.5.3.2. Técnicas no resectivas.
A parte de las técnicas resectivas existen otras como son la radiocirugía gamma, la estimulación cerebral profunda y la estimulación del nervio vago que serán descritas a continuación:
- Radiocirugía gamma: Esta técnica de radiocirugía estereotáxica tiene como objetivo el tratamiento de pequeñas lesiones intracraneales mediante la emisión de radiaciones ionizantes. Actualmente se utilizan radiaciones de cobalto que emiten una radiación gamma. Otra de las características de esta técnica es que no se daña el tejido circundante sano, ya que solo se emite en la zona intracraneal lesionada (Calcerrada & Sábes, 2005). Con esta técnica, realizada en una sesión única, se busca evitar los riesgos de las intervenciones quirúrgicas en epilepsias del lóbulo temporal medial, hamartomas hipotalámicos y cavernomas. Los resultados de éxito son similares a los que se obtienen tras la cirugía resectiva, sin embargo, la eficacia es visible después de varios meses (Carreño & Serratosa, 2012).
- Estimulación cerebral profunda (ECP): En la epilepsia hay varios estudios que demuestran que tras las repetidas crisis epilépticas se forman reorganizaciones corticales y subcorticales. Estructuras del córtex pueden mantener cambios metabólicos anormales, posterior a la resección quirúrgica, por la formación de conexiones neuronales formadas previamente a la intervención. La ECP es una modalidad terapéutica utilizada para regular estos circuitos anormales con el objetivo de controlar las crisis epilépticas, y en plazo más amplio eliminarlas (Lega, Halpem, Jaggi & Baltuch, 2010). Las dianas utilizadas son el cerebelo, núcleos talámicos, subtalámicos e hipotalámico, caudado y sustancia negra (Fisher et al., 2010).
- Estimulación del nervio vago: Este tratamiento es utilizado, generalmente, en pacientes con crisis focales, que no son candidatos a cirugía por diferentes motivos y que presentan una epilepsia refractaria. La respuesta a este procedimiento terapéutico es considerada como paliativa, debido a la dificultad de conseguir un control total de las crisis epilépticas (Téllez-Zenteno & Ladino, 2013). El mecanismo de acción de esta terapia es a nivel del nervio vago izquierdo, a nivel cervical, produciendo una estimulación en el tálamo y amígdala, y diferentes conexiones en el córtex cerebral. La razón de su colocación en la región izquierda, y no en la región derecha, es la de evitar complicaciones y alteraciones en la conducción cardíaca. Este generador se coloca quirúrgicamente (Carreño & Serratosa, 2012). El dispositivo puede ser activado, mediante un magneto, por el paciente cuando esté sintiendo el aura y así genera una estimulación eléctrica (Cramer, Ben Menachem & French, 2001).
4.6. Otras alternativas: Dieta cetogénica (DC).
A principios de la década de 1920 se empezó a utilizar la dieta cetogénica (DC) como terapia anticonvulsiva. Sin embargo, con la aparición de los primeros FAE el uso de DC descendió. No obstante, su uso como tratamiento antiepiléptico ha vuelto a incrementarse en las últimas dos décadas.

25
La DC consiste en una dieta con niveles altos de lípidos, una cantidad adecuada de proteínas y una baja cantidad de hidratos de carbono, lo cual induce la cetosis, minimizando los posibles efectos secundarios relacionados con el crecimiento.
Actualmente puede considerarse un tratamiento antiepiléptico de primera línea en crisis mioclónicas, esclerosis tuberosa, epilepsia mioclónica-astática (síndrome de Doose), síndrome de Dravet, síndrome de Lennox-Gastaut, etcétera. Sin embargo diferentes estudios destacaron que la DC, aplicada en las crisis epilépticas temporales, no conseguía resultados tan beneficiosos en contraste con los resultados obtenidos en crisis epilépticas generalizadas (Lambruschini & Pineda, 2012).

26
5. CUIDADOS DE ENFERMERÍA EN EL PACIENTE EPILÉTICO.
A continuación se presentan los cuidados de enfermería aplicados al paciente epiléptico en todos los ámbitos, abarcando tanto la prevención como el procedimiento a realizar en diferentes pruebas utilizadas para el diagnóstico de la ELT (Segura, Gómez, Campaña, Gómez & Gómez, 2013) y su tratamiento.
5.1. Papel de la Enfermería en la educación sanitaria de pacientes epilépticos y familiares.
El profesional de Enfermería, además, de cubrir las necesidades básicas de las personas con demandas de salud con el objetivo de que recuperen su independencia o suplir su autonomía, si es necesario, tiene otros campos de actuación que la consolidan como una ciencia del cuidado. Estos pilares que conforman a la Enfermería como ciencia son la función administradora y gestora de los cuidados, la investigación para seguir desarrollando cuidados de salud de calidad y la función docente sobre futuros profesionales, así como de personas con necesidades de salud y sus familias (Bellido, Ríos & Fernández, 2010). Como se ha plasmado anteriormente en el apartado sobre el tratamiento preventivo de la epilepsia, ésta es una enfermedad neurológica que se caracteriza por la aparición de crisis epilépticas en los pacientes. En ocasiones, estas crisis surgen por una mala prevención de los factores desencadenantes. Tanto el personal facultativo como el personal de Enfermería deben participar en la educación de la persona epiléptica y de su familia (Anexo III).
5.2. Cuidados de enfermería en las pruebas diagnósticas.
Dentro de las diferentes pruebas diagnósticas, se ha de procurar proporcionar la mayor información solicitada por el paciente con objeto de mantenerle en el estado de mayor tranquilidad posible. Así en cada una de las pruebas debe existir una información previa y también durante todo el desarrollo de las mismas.
5.2.1. Cuidados de enfermería en la Resonancia Magnética (RM)
La RM es una prueba no invasiva pero que puede resultar traumática para los pacientes. Aquí emerge la figura del personal de Enfermería para tranquilizar al paciente explicándole el procedimiento de la prueba y entregándole el consentimiento informado (Anexo III).
5.2.2. Cuidados de enfermería en el Electroencefalograma (EEG)
El electroencefalograma es una prueba desconocida para muchos pacientes llegando a generar incertidumbre por lo que el profesional de Enfermería es imprescindible para tranquilizar al paciente, explicarle el procedimiento a seguir y enseñarle a realizar movimientos de hiperventilación. Es función de Enfermería entregar al paciente el consentimiento informado y encargarse de registrar movimientos que puedan causar artefactos como el parpadeo, deglución y habla. El personal de Enfermería deberá de informar al paciente sobre diferentes requisitos de la prueba (Anexo III).

27
5.2.3. Cuidados de enfermería en el PET y SPECT
El PET y el SPECT, al igual que el EEG, son pruebas desconocidas para muchos pacientes epilépticos generando inseguridad. Entre las funciones de Enfermería en esta prueba se encuentra el entregar el consentimiento informado y tranquilizar al paciente de cara a la realización de la prueba (Anexo III).
5.3. Papel de la Enfermería en el tratamiento quirúrgico de la epilepsia: Funciones de la/el enfermera/o circulante e instrumentista.
En este apartado se estudiarán las funciones del profesional de Enfermería en la cirugía de la epilepsia en el proceso intraoperatorio. Dentro del quirófano de Neurocirugía se encuentra el/la enfermero/a circulante y el/la enfermero/a instrumentista. El/la enfermero/a circulante desarrolla las siguientes funciones (Sánchez Fernández et al., 2013) (Anexo III).

28
6. CONCLUSIONES.
1. La epilepsia es la segunda enfermedad neurológica más prevalente. Según datos de la OMS, sigue aumentando la prevalencia y los datos de mortalidad y morbilidad también lo están haciendo. Además, el prejuicio que tiene esta enfermedad a día de hoy, produce un rechazo hacia las personas epilépticas en las sociedades de algunos países.
2. La epilepsia fue en sus orígenes una enfermedad muy desconocida. El avance de la medicina permitió conocer que esta enfermedad estaba causada por un desequilibrio neurofisiológico a nivel del sistema nervioso central.
3. Esta enfermedad genera altos costes a nivel económico derivados del alto precio de las pruebas diagnósticas, estancias hospitalarias, tratamientos farmacológicos, tratamientos quirúrgicos, etc. Aparte de este impacto, se encuentra el daño que la enfermedad causa en pacientes epilépticos y en sus familias, siendo una enfermedad muy incapacitante.
4. La epilepsia del lóbulo temporal es la más común dentro de las focales. Además es una epilepsia de difícil control mediante fármacos siendo candidatos a tratamiento quirúrgico aquellos pacientes que presenten una epilepsia refractaria.
5. El personal de Enfermería es clave en el manejo de los pacientes con epilepsia. En primer lugar, destaca el papel de la Enfermería en el tratamiento preventivo de factores desencadenantes de epilepsia. También es imprescindible la figura de estos profesionales en las pruebas diagnósticas. Por último, es importante disponer de profesionales de Enfermería cualificados en el área quirúrgica.

29
7. BIBLIOGRAFÍA
Abad, F., Bellido, G., Camino, R., Cañadillas, F., Fernández, L., Martínez, C., et al. (2011). Crisis epilépticas y epilepsia. En Guía ÁPICE de epilepsia algunos la padecen, entre todos la tratamos (p. 18). Sevilla: ÁPICE, Asociación Andaluza de Epilepsia (ed). Recuperado de: http://www.asadeepilepsia.com/guia-apice/guia-apice.pdf
Álvarez-Linera, J., Bargalló, N., Xetoain, X. (2012). Métodos diagnósticos en epilepsia: Neuroimagen. En J.M. Mercadé Cerdá, J. Sancho Rieger, J.A. Mauri Llerda, F.J. López González y X. Salas Puig (ed.). Guías diagnósticas y terapéuticas de la Sociedad Española de Neurología 2012. 1. Guía oficial de práctica clínica en epilepsia (pp. 58-64). Madrid: Luzán 5 S.A.
Armijo, J.A., De las Cuevas, I., Adín, J. (2000). Canales iónicos y epilepsia. Rev Neurol, 30 (supl 1), S25-41.
Ashcroft, F.M. (2000). Ion channels and disease. Academic Press, 481.
Barea, R. (s.f.). Tema 5: Electroencefalografía. En Ingeniería en Electrónica. Instrumentación Biomédica. Universidad de Alcalá, Departamento de Electrónica. Recuperado de: http://www.bioingenieria.edu.ar/academica/catedras/bioingenieria2/archivos/apuntes/tema%205%20-%20electroencefalografia.pdf
Bellido, J.C., Ríos, Á., Fernández, S. (2010). Modelo de cuidados de Virginia Henderson. En J.C. Bellido y J.F. Lendínez (Coords.). Proceso Enfermero desde el modelo de cuidados de Virginia Henderson y los Lenguajes NNN. Jaén: Ilustre Colegio Oficial de Enfermería de Jaén.
Benbadis, S.R. (2015). Localization-related (focal) epilepsy: Causes and clinical features. UpToDate. Recuperado de: http://www.uptodate.com/contents/localization-related-focal-epilepsy-causes-and-clinical-features
Bercovici, E., Kumar, B.S., Mirsattari, S.M. (2012). Neocortical temporal lobe epilepsy. Epilepsy Res Treat, 103160, 1-15.
Berg, A.T., Berkovic, S.F., Brodie, M., Bruchhalter, J., Cross, J.H., Van Emde Voas, W., et al. (2010). Revised terminology and concepts for organization of seizures and epilepsies: report of the ILAE Commission on Classification and Terminology. Epilepsia, 51 (4), 676-685.
Berg, A.T., Scheffer, I.E. (2011). New concepts in classification of the epilepsies: entering the 21st century. Epilepsia, 52, 1058-1062.
Berger, H. (1929). Uber das Electrenkephalogram des Menschen. Arch Psychiatr Nervenkr, 87, 527-570.
Binnie, C.D., Rowan, A.J., Overweg, J., Meinardi, H., Wisman, T., Kamp, A. et al. (1981). Telemetric EEG and videomonitoring in epilepsy. Neurology, 31, 298-303.
Blümcke, I., Thom, M., Aronica, E., Armstrong, D.D., Bartolomei, F., Bernasconi, A., et al. (2013). International consensus classification of hippocampal sclerosis in temporal lobe epilepsy: A Task Force report from the ILAE Commission on Diagnostic Methods. Epilepsia, 54 (7), 1315-1329.

30
Cairós, M. (s.f.). Epilepsia del Lóbulo Temporal. En Cerebro Inquieto. Aprendiendo sobre la epilepsia. Recuperado de: http://www.cerebroinquieto.com/epilepsia-del-lobulo-temporal.html
Calcerrada, N., Sabés, R. (2005). Concepto de radiocirugía y Sistemas de radiocirugía estereotáxica (SRS). En, Efectividad, seguridad y estimación de costes del sistema de radio cirugía Cyberknyfe (pp. 7-11). Madrid: Unidad de Evaluación de Tecnologías Sanitarias (UETS), Agencia Laín Entralgo.
Cano Sánchez, M.C. (2012). Actualización del cuidado enfermero del paciente con epilepsia. Metas de Enferm, 15 (8), 15-20.
Carreño Martínez, M., Serratosa Fernández, J. (2012). Cirugía de la epilepsia. En J.M. Mercadé Cerdá, J. Sancho Rieger, J.A. Mauri Llerda, F.J. López González y X. Salas Puig (ed.). Guías diagnósticas y terapéuticas de la Sociedad Española de Neurología 2012. 1. Guía oficial de práctica clínica en epilepsia (pp. 194-201). Madrid: Luzán 5 S.A.
Casas-Fernández, C. (2012). Análisis crítico de la nueva clasificación de las epilepsias y crisis epilépticas de la Liga Internacional contra la Epilepsia. Rev Neurol, 54 (Supl 3), S7-18.
Casas Fernández, C., Serrano Castro, P.J. (2012). La historia clínica en epilepsia. Diagnóstico diferencial de la epilepsia en las distintas edades. En J.M. Mercadé Cerdá, J. Sancho Rieger, J.A. Mauri Llerda, F.J. López González y X. Salas Puig (ed.). Guías diagnósticas y terapéuticas de la Sociedad Española de Neurología 2012. 1. Guía oficial de práctica clínica en epilepsia (pp. 29-38). Madrid: Luzán 5 S.A.
Casse, R., Rowe, C.C., Newton, M., Berlangieri, S.U., Scott, A.M. (2002). Positron emission tomography and epilepsy. Mol Imaging Biol, 4, 408-414.
Catterall, W.A., Goldin, A.L., Waxman, S.G. (2005). International Union of Pharmacology. XLVII. Nomenclature and structure-function relationships of voltage-gated sodium channels. Pharmacol Rev, 57 (4), 397-409.
Catterall, W.A., Striessnig, J., Snutch, T.P., Pérez-Reyes, E. (2003). International Union of Pharmacology. XL. Compendium of voltaje-gated ion channels: calcium channels. Pharmacol Rev, 55 (4), 579-581.
Cendes, F. (2005). Mesial temporal lobe epilepsy syndrome: an updated overview. J Epilepsy Clin Neurophysiol, 11, 141-144.
Chen, L.S., Mitchell, W.G., Horton, E.J., Snead, O.C. (1995). Clinical utility of video-EEG monitoring. Pediatr Neurol, 12, 220-224.
Claro Mader, E. (2015). What are the differences between CA1, CA2, CA3, and CA4?. Quora. Recuperado de: https://www.quora.com/What-are-the-differences-between-CA1-CA2-CA3-and-CA4
Cohen-Gadol, A.A., Wilhelmi, B.G., Collignon, F., White, J.B., Britton, J.W., Cambier, D.M., et al. (2006). Long-term outcome of epilepsy surgery among 399 patients with nonlesional seizure foci including mesial temporal lobe sclerosis. J Neurosurg, 104, 513-524.
Collado-Vázquez, S., Carrillo, J.M. (2012). La epilepsia en la literatura, el cine y la televisión. Rev Neurol, 55, 431-442.

31
Conn, P.J. (2003). Physiological roles and therapeutic potential of metabotropic glutamate receptors. Ann N Y Acad Sci, 1003, 12-21.
Cramer, J.A., Ben Menachem, E., French, J. (2001). Review of treatment options for refractory epilepsy: nre medications and vagal nerve stimulation. Epilepsy Res, 47, 17-25.
Department of Pathology, University of Oklahoma Health Sciences Center. NeuroTest Question. Recuperado de: http://moon.ouhsc.edu/kfung/jty1/NeuroTest/R01-Ans.htm
Devaux, B., Chassoux, F., Guenot, M., Haegelen, C., Bartolomei, F., Rougier, A., et al. (2008). Epilepsy surgery in France. Neurochirurgie, 54, 453-465.
Dichter, M.A., Ayala, G.F. (1987). Cellular mechanism of epilepsy: a status report. Science, 237, 157-164.
Fernández-Torre, J.L. (2002). Auras epilépticas: clasificación, fisiopatología, utilidad práctica, diagnóstico diferencial y controversias. Rev Neurol, 34, 977-983.
Fisher, R.S., Van Emde Voas, W., Blume, W., Elger, C., Genton, P., Lee, P., et al. (2005). Epileptic seizures and epilepsy: definitions proposed by the International League Against Epilepsy (ILAE) and the International Bureau for Epilepsy (IBE). Epilepsia, 46, 470-472.
Fisher, R., Salanova, V., Witt, T., Worth, R., Henry, T., Gross, R., et al. (2010). Electrical stimulation of the anterior nucleus of thalamus for treatment of refractory epilepsy. Epilepsia, 51, 899-908.
Foldvary, N., Klem, G., Hammel, J., Bingaman, W., Najm, I., Luders, H. (2001). The localizing value of ictal EEG in focal epilepsy. Neurology, 57, 2022-2028.
Gibbs, F.A., Davis, H., Lennox, W.G. (1935). The EEG in epilepsy and in the impaired states of consciousness. Arch Neurol Psychiatry, 34, 1133.
Gibbs, F.A., Lennox, W.G., Gibbs, E.L. (1936). The electroencephalogram in diagnosis and in localization of epileptic seizures. Arch Neurol Psychiatry, 36, 1225-1235.
Grupo de Cirugía Funcional de la Sociedad Española de Neurocirugía (SENEC). (2009). Guías clínicas para la cirugía de la Epilepsia y de los Trastornos del Movimiento. Neurocirugía, 20, 329-334.
Herranz, J.L. (2002). Canalopatías: un nuevo concepto en la etiología de las epilepsias. Boletín de la Sociedad de Pedriatría de Asturias, Cantabria y Castilla y León, 42 (179), 20-28.
Herranz, J.L., Forcadas, M.I. (2012). Principio farmacológicos del tratamiento antiepiléptico. En J.M. Mercadé Cerdá, J. Sancho Rieger, J.A. Mauri Llerda, F.J. López González y X. Salas Puig (ed.). Guías diagnósticas y terapéuticas de la Sociedad Española de Neurología 2012. 1. Guía oficial de práctica clínica en epilepsia (pp. 75-84). Madrid: Luzán 5 S.A.
Holmes, M.D., Miles, A.N., Dodrill, C.B., Ojemann, G.A., Wilensky, A.J. (2003). Identifying potential surgical candidates in patients with evidence of bitemporal epilepsy. Epilepsia, 44, 1075-1079.
Inan Akman, Cigdem. (s.f.). PET cerebral en la infancia. Neuropediatría Ilustrada, 287. Recuperado de: http://media.axon.es/pdf/88944_4.pdf
International League Against Epilepsy. Strategic plan-June 2009. (2015). Recuperado de: http://www.ilae.org/Visitors/Documents/StrategicPlan-FinalJuly-09.pdf

32
Jan, M.M., Girvin, J.P. (2008). Seizure semiology: value in identifying seizure origin. Can J Neurol Sci, 35, 22-30.
Jan, M.M., Sadler, M., Rahey, S.R. (2010). Electroencephalographic features of temporal loce epilepsy. Can J Neurol Sci, 37, 439-448.
Jasper, H.H. (1936). Localized analyses of the function of the human brain by the electro-encephalogram. Arch Neurol Psychiatry, 36, 1131.
Kandel, E.R., Schwartz, J.H., Jessell, T.M. (2000). Principles of neural science. McGraw-Hill.
Krauss, G.L. (2013). Chosing the Right Medical Regimen for Seizures Disorders. Medscape Education Neurology & Neurosurgery. Recuperado de: http://www.medscape.org/viewarticle/782779_transcript
Kwan, P., Arzimanoglou, A., Berg, A.T., Brodie, M.J., Allen Hauser, W., Mathern, G., et al, (2010). Definition of drug resistant epilepsy: consensus proposal by the ad hoc Task Force of the ILAE Commission on Therapeutic Strategies. Epilepsia, 51, 1069-1077.
Kwan, P., Brodie, M.J. (2000). Early identification of refractory epilepsy. N Engl J Med, 342, 314-319.
Kwan, P., Sander, J.W. (2004). The natural history of epilepsy: an epidemiological view. J Neurol Neurosurg Psychiatry, 75, 1376-1381.
Lambruschini Ferri, A., Pineda Marfa, M. (2012). Introducción y Fisiopatología del efecto antiepileptógeno. En N. Lambruschini y A. Gutiérrez (Coords.). Dieta cetogénica. Apectos clínicos. Aplicación dietética (pp. 13-21). Barcelona: Servei Neurología, Hospital Sant Joan de Dèu. Universitat de Barcelona.
Lega, B.C., Halpem, C.H., Jaggi, J.L., Baltuch, G.H. (2010). Deep brain stimulation in the treatment of refractory epilepsy: update on current data and future directions. Neurobiology of Disease, 38 (3), 354-360.
López, J.E. (2008). Amigdala: Síndrome de Klüver-Bucy. Universidad de Valencia. Recuperado de: http://mural.uv.es/locen/Diseno%20de%20trabajos%20cientificos.html
López, J.I., Pomposo-Gaztelu, I. (2010). Patología quirúrgica de la epilepsia. Rev Neurol, 50, 616-622.
Lossin, C. (2009). A catalog of SCN1A variants. Brain Dev, 31, 114.
Maestú, F., Martin, P., Gil-Nagel, A., Franch, O., Sola, R.G. (2000). Evaluación en la cirugía de la epilepsia. Rev Neurol, 30 (5), 477-482.
Mercadé Cerdá, J.M., Mauri Llerda, J.A., López González, F.J. (2012). Métodos diagnósticos en epilepsia. En J.M. Mercadé Cerdá, J. Sancho Rieger, J.A. Mauri Llerda, F.J. López González y X. Salas Puig (ed.). Guías diagnósticas y terapéuticas de la Sociedad Española de Neurología 2012. 1. Guía oficial de práctica clínica en epilepsia (pp. 39-46). Madrid: Luzán 5 S.A.
Molins, A. (2013). Epilepsia; clínica y tratamiento. En M. Aguilar, M.L. Alcaraz, A. Arpa, F.J. Arpa, J. García, A.B. Castillo, et al. Tratado de Enfermería Neurológica. La persona, la enfermedad y los cuidados (3ª ed., pp. 103-110). Barcelona: Elsevier España S.L.

33
Monge, L., Pérez, R., López, J., Lafuente, M., Ruiz del Olmo, I., Peña, J.L. (2010). Esclerosis mesial temporal en pediatría: espectro clínico. Nuestra experiencia de 19 años. Rev Neurol, 50, 341-348.
Organización Mundial de la Salud. (2015). Epilepsia. Recuperado de: http://www.who.int/mediacentre/factsheets/fs999/es/
Pastor, J., Menéndez de la Prida, I., Hernando, V., Sola, R.G. (2006). Voltage sources in mesial temporal lobe epilepsy recorded with foramen ovale electrodes. Clin Neurophysiol, 117, 2604-2614.
Pastor, J., Sola, R.G., Vega-Zelaya L., Garnés, O., Ortega, G.J. (2014). Conectividad funcional y redes complejas en el estudio de la epilepsia focal. Implicaciones fisiopatológicas y terapeúticas. Rev Neurol, 58, 411-419.
Pereno, G.L. (2010). Fisiopatología de la Epilepsia del Lóbulo Temporal: Revisión del Proceso de Muerte Neuronal a la Neuroplasticidad. Revista Argentina de Ciencias del Comportamiento (RACC), 2 (1), 46-57.
Piña-Astete, L., Leonel, M., Gómez, M.P., Campos, E., García-Morales, I., Toledano, R. (2011). Eficacia de la monitorización videoelectroencefalográfica prolongada con protocolo específico de activación cerebral en el diagnóstico diferencial de la epilepsia. Revista Científica de la Sociedad Española de Enfermería Neurológica, 33 (1), 5-9.
Reis, J. (2008). Eloquent cortex and tracts: overview and noninvasive evaluation methods. En H.O. Luders (ed), Textbook of epilepsy surgery (pp. 871-880). London: Informa Healthcare.
Rohit Bakshi, M.D. (2006). Neuroimaging and Diagnosis Highlights. Medscape. Recuperado de: http://www.medscape.org/viewarticle/506103
Saiz Díaz, R.S. (2012). Rendimiento diagnóstico del EEG. En Módulo 3: Diagnóstico. Neurodidacta. Recuperado de: http://www.neurodidacta.es/es/comunidades-tematicas/epilepsia/epilepsia/cuestiones-relativas-diagnostico/rendimiento-diagnostico-del-eeg
Saiz, R.S., Sancho, J. (2012). Terminología de las crisis epilépticas y epilepsia. Semiología de las crisis epilépticas. En J.M. Mercadé Cerdá, J. Sancho Rieger, J.A. Mauri Llerda, F.J. López González y X. Salas Puig (ed.). Guías diagnósticas y terapéuticas de la Sociedad Española de Neurología 2012. 1. Guía oficial de práctica clínica en epilepsia (pp. 18-19). Madrid: Luzán 5 S.A.
Sánchez-Álvarez, J.C., Serrano Castro, P., Cañadillas Hidalgo, F. (2002). Refractory epilepsy in adults. Rev Neurol, 35, 931-953.
Sánchez, J., Centanaro, M., Solís, J., Valle, C. (2009). Estudio de 20 pacientes con epilepsia del lóbulo temporal medial con esclerosis del hipocampo. Revista ecuatoriana de Neurología, 18 (1-2). Recuperado de: http://www.medicosecuador.com/revecuatneurol/vol18_No1-2_2009/articulos_originales/estudio_20_pacientes_con_epilepsia.htm
Sánchez Fernández, F.M., Sánchez Cánovas, M.D., Solano García, M., Sánchez Ruiz, G., Flores Martín, J.A., Gilabert Murcia, J., et al. (2013). Funciones de la Enfermera Circulante y

34
Funciones de la Enfermera Instrumentista. En. Manual de Acogida y Funcionamiento del Servicio de Quirófano para Profesionales de Nueva Incorporación (pp. 14-17). Murcia: Consejería de Sanidad. Servicio Murciano de Salud.
Schiller, Y. (2002). Inter-Ictal- and Ictal-Like Epileptic Discharges in the Dendritic Tree of Neocortical Pyramidal Neurons. Journal of Neurophysiology, 88 (6), 2954-2962. Recuperado de: http://jn.physiology.org/content/88/6/2954
Segura, T., Gómez, A., Campaña, L., Gómez, I., Gómez, M. (2013). Diagnóstico de las enfermedades neurológicas y neuroimagen. En M. Aguilar, M.L. Alcaraz, A. Arpa, F.J. Arpa, J. García, A.B. Castillo, et al. Tratado de Enfermería Neurológica. La persona, la enfermedad y los cuidados (3ª ed., pp. 17-22). Barcelona: Elsevier España S.L.
Setoain, X., Pavía, J., Seres, E., García, R., Carreño, M.M., Donaire, A., et al. (2012). Validation of an automatic dose injection system for ictal SPECT in epilepsy. J Nuci Med, 53, 324-329.
Sharan, A., Ooi, Y.C., Langfitt, J., Sperling, M.R. (2011). Intracarotid amobarbital procedure for epilepsy surgery. Epilepsy Behav, 20, 209-213.
Sigel, E., Steinmann, M.E. (2012). Structure, function, and modulation of GABA (A) receptors. J Biol Chem, 287 (48), 40224-31.
Silverthorn, D. (2014). Propiedades de las neuronas y de las redes neuronales. En Fisiología Humana. Un enfoque integrado (6ª ed., pp. 239-281). Buenos Aires: Editorial Médica Panamericana.
Simeone, T.A., Donevan, S.D., Rho, J.M. (2003). Molecular biology and ontogeny of gamma-aminobutyric acid (GABA) receptors in the mammalian central nervous system. J Child Neurol, 18 (1), 39-48.
Simeone, T.A., Sanchez, R.M., Rho, J.M. (2004). Molecular biology and ontogeny of glutamate receptors in the mammalian central nervous system. J Child Neurol, 19 (5), 343-360.
Spencer, S. (2002). When should temporal-lobe epilepsy be treated surgically?. Lancet Neurol, 1 (6), 375-382.
Stafstrom, C.E., Rho, J.M. (2014). Pathophysiology of seizures and epilepsy. UpToDate. Recuperado de: http://www.uptodate.com/contents/pathophysiology-of-seizures-and-epilepsy
Stephen, L.J., Brodie, M.J. (2011). Pharmacotherapy of epilepsy: newly approved and developmental agents. CNS Drugs, 25 (2), 89-107. DOI: 10.2165/11584860-000000000-00000.
Schwartzkroin, P.A. (1986). Hippocampal slices in experimental and human epilepsy. Adv Neurol, 44, 991-1010.
Tatum, W.O. (2012). Mesial Temporal Lobe Epilepsy. Journal of Clinical Neurophysiology, 29 (5), 356-365.
Téllez-Zenteno, J.F., Ladino, L.D. (2013). Epilepsia temporal: aspectos clínicos, diagnósticos y de tratamiento. Rev Neurol, 56, 229-242.
Téllez-Zenteno, J.F., Wiebe, S., López-Méndez, Y. (2010). Epilepsia extratemporal. Aspectos clínicos, diagnósticos y de tratamiento. Rev Neurol, 51, 85-94.

35
Thom, M., Sisodiya, S., Najm, I. (2008). Neuropathology of epilepsy. Greenfield’s neuropathology, 1, 833-887.
Thompson, S.A., Duncan, J.S., Smith, S.J. (2000). Partial seizures presenting as panic attacks. BMJ, 321, 1002-1003.
Unwonge, K., Wehner, K., Foldvary-Schaefer, N. (2010). Selecting patients for epilepsy surgery. Curr Neurol Neurosci Rep, 10, 299-307.
Van Paesschen, W., Dupont, P., Sunaert, S., Goffin, K., Van Laere, K. (2007). The use of SPECT and PET in routine clinical practice in epilepsy. Curr Opin Neurol, 20, 194-202.
Wieser, H.G., ILAE Commission on Neurosurgery of epilepsy. (2004). ILAE commission report. Mesial temporal lobe epilepsy with hippocampal sclerosis. Epilepsia, 45, 695-714.
Woermann, F.G., Volmar, C. (2009). Clinical MRI in children and adults with focal epilepsy: a critical review. Epilepsy Behav, 17, 161-164.

36
8. ANEXOS.
Anexo I: Características de la epilepsia mesial y de la epilepsia neocortical.
Características de la epilepsia mesial y de la epilepsia neocortical
Epilepsia mesial Epilepsia neocortical
Prevalencia 90% 10%
Factores de riesgo Convulsiones febriles, TCE,
No conocidos infecciones SNC, lesiones perinatales
Edad de presentación Adolescencia 5-10 años más tarde
Aura Abdominal, olfatoria Psíquica, auditiva gustatoria, miedo y vertiginosa, visual
estados de ensoñación y cefálica
Alteración de la conciencia Tardía
Temprana, usualmente asociada a afectación de la actividad motora
Automatismos Tempranos, ocurren en Tardíos o ausentes, rara vez los primeros 20s de la crisis son la manifestación inicial
Manifestaciones motoras
Automatismos ipsilaterales Postura distónica contralateral
seguidos de postura distónica temprana, no precedida por contralateral. Movimiento de automatismos. Más frecuentes
piernas frecuente movimientos clónicos, rara vez movimiento de piernas
Generalización secundaria Infrecuente Más frecuente y temprana
Otras características Mayor hiperventilación, Mayor afectación motora con
Semiológicas suspiros, tos postictal, giro ictal mirada fija inicial. Más
y actividad de búsqueda presencia de lenguaje ictal
Duración de la crisis > 1 minuto < 1 minuto
Electroencefalograma
Ondas agudas rítmicas de Ondas con frecuencia de 2-5Hz, 5-10 Hz, con activación con menor estabilidad en
Ictal esfenoidal y de la región frecuencia y amplitud. A veces temporomesial anterior se evidencia actividad temporal
Bilateral
Resonancia magnética La mayoría de los casos son Usualmente no lesionales o con
lesionales y se evidencia EH lesiones tumorales, MAV o MDC
EH: epilepsia hipocampal; MAV: malformaciones arteriovenosas; SNC: sist. Nervioso central; MDC: malformaciones del desarrollo cortical; TCE: traumatismo craneoencefálico
Fuente: Téllez-Zenteno, J.F., Ladino, L.D. (2013). Epilepsia temporal: aspectos clínicos, diagnósticos y de tratamiento. Rev Neurol, 56, 229-242.

37
Anexo II: Tipos de síntomas, localización y lateralización de los mismos.
Semiología, signos localizadores y lateralizadores
Localización Lateralización
Auras
Abdominal Temporal No tiene valor Psíquica Temporal neocortical No tiene valor Olfatoria Temporal y orbitofrontal No tiene valor Visual compleja Temporal anteromesial Contralateral Auditiva Temporal No tiene valor Gustativa Temporal No tiene valor Orgásmica Temporal No dominante
Automatismos
Automatismo oral Temporal (hipocampo) No tiene valor Automatismo manual Temporal Ipsilateral Automatismo con la
Temporal No dominante conciencia preservada Automatismos bipedales Un 5% temporal No tiene valor Automatismos seguidos
Temporal neocortical Ipsilateral de crisis clónicas Automatismos seguidos de
Temporal mesial Ipsilateral postura distónica de la mano Otras manifestaciones ictales Parpadeo ictal unilateral Temporal Ipsilateral Escupitajo ictal Temporal No dominante Beber durante la crisis Temporal No dominante Emesis ictal Temporal No dominante Urgencia urinaria ictal Temporal No dominante Piloerección Temporal Ipsilateral Taquicardia ictal pura Temporal No tiene valor Cefalea periictal Temporal Ipsilateral Ataque de pánico ictal Temporal No dominante
Lenguaje
Afectación del lenguaje ictal Temporal Dominante Lenguaje ictal Temporal No dominante Disfasia postictal Temporal Dominante Asimetria facial
Temporal mesial Contralateral unilateral emocional
(Continúa)

38
Motor
Versión cefálica no Frontal o temporal Ipsilateral
forzada temprana Versión cefálica
Frontal o temporal Contralateral forzada tardía Versión cefálica no
Frontal o temporal Ipsilateral forzada tardía Postura distónica de la
Temporal o frontal Contralateral mano unilateral
Postural del 4 Un 70% temporal, Contralateral al brazo un 30% extratemporal extendido
Manifestaciones postictales
Nosewiping postictal Temporal Ipsilateral Tos postictal Temporal No dominante Desorientación postictal Temporal No dominante Alteración de la memoria
Temporal Dominante verbal postictal Alteración de la memoria
Temporal No dominante visual postictal
Fuente: Téllez-Zenteno, J.F., Ladino, L.D. (2013). Epilepsia temporal: aspectos clínicos, diagnósticos y de tratamiento. Rev Neurol, 56, 229-242.

39
Anexo III: Actuación enfermera en los procesos diagnósticos y de tratamiento en la epilepsia
Recomendaciones que el profesional de Enfermería ha de instruir al paciente epiléptico y su familia (Cano Sánchez, 2012):
- Incidir en la importancia que tiene el correcto cumplimiento del tratamiento médico, asegurándose de que no haya interrupciones.
- En caso de olvido de alguna dosis de FAE, deberá tomar la dosis correspondiente cuando sea consciente del olvido pero sin exceder la dosis diaria.
- En caso de que el paciente vomite después de la ingesta del FAE, y no hayan transcurrido 30 minutos, se debe repetir la ingesta de la dosis.
- Ingerir los FAE con las comidas. No tomar ácido valproico con bebidas carbonatadas ya que disminuye su absorción.
- Destacar la transcendencia de los controles analíticos, de una manera periódica, para conocer los niveles séricos ya que estos varían dependiendo de la capacidad de absorción que tiene cada paciente.
- Controlar la frecuencia con la que aparecen las crisis epilépticas. Es de vital importancia su conocimiento por el facultativo especialista debido a que puede clasificar la epilepsia como refractaria.
- Destacar la importancia que tiene el conocimiento de la enfermedad por parte del círculo cercano de la persona. Evitar que adopten posiciones de sobreprotección.
- En caso de crisis epiléptica, tratar la situación de una manera discreta. - Considerar la terapia psicológica o los grupos de autoayuda. - Transcendencia de llevar a cabo un control de la dieta. - Evitar consumo de sustancias tóxicas (tabaco, drogas, alcohol…) y estimulantes (café,
productos con cafeína…). - Mantener un patrón de horas y calidad de sueño adecuado para evitar la aparición de
las crisis epilépticas. - Algunos fármacos como la fenitoína pueden provocar hiperplasia gingival por lo que se
ha de asegurar una correcta higiene bucal. - Saber reconocer los efectos adversos de los FAE prescritos. - No conducir si se ha sufrido una crisis epiléptica en un período menor a 12 meses. Llevar
a cabo las pautas desarrolladas en el R.D. 818/2009 del 8 de mayo. - Después de una crisis, es importante observar el color de la orina ya que una lesión
muscular podía desencadenar la coloración de la misma. - En caso de mujeres con deseos de embarazo, consultar con su neurólogo para que elija
FAE y ajuste dosis. Determinados FAE tienen un elevado índice teratogénico. - Algunos FAE pueden ser transportados en la leche materna y provocar somnolencia en
el lactante, el cual deberá ser sometido a vigilancia. - Solicitar información y sistemas de apoyo si va a ser sometido a tratamiento quirúrgico. - Evitar los deportes de riesgo y tener especial cuidado con la natación (temperatura del
agua y profundidad del medio). - Participar en deportes colectivos que no requieran un excesivo esfuerzo físico.

40
Resonancia magnética:
Electroencefalografía:
- Se trata de una prueba indolora. - Ayuna previa de 6 horas, por si es necesario la inyección de contraste intravenoso. - La RM puede causar daños en relojes y tarjetas de crédito. Asegurar que el paciente se
desprende de estos materiales así como de cualquier objeto metálico (joyas, etcétera) antes de comenzar la prueba.
- En caso de ser preciso administrar contraste intravenoso, hay que explicar al paciente que puede tener la sensación de calor, rubor, gusto salado o metálico. En caso de que sea necesaria la inyección de contraste, el personal de Enfermería responsable le canalizará una vía periférica al paciente. Si existe pauta médica, el personal de Enfermería responsable inyectará una sedación al paciente.
- La RM puede causar sensación de claustrofobia por lo que se le pedirá al paciente permanecer quieto durante su realización. El personal de Enfermería responsable debe asegurarse que el paciente se encuentra en posición de decúbito supino durante la prueba.
- La máquina emite un tipo de ruidos del cual no debe preocuparse. En caso de que el paciente lo precise, el personal de Enfermería responsable le dará tapones para los oídos al paciente.
- Existe la posibilidad de comunicarse entre el paciente y el personal encargado de realizar la RM mediante un micrófono.
- Posibles dudas sobre la prueba. - No debe fumar y tampoco tomar refrescos de cola, café o té la mañana en la que se realizará
la prueba debido a su efecto estimulante. - La noche previa a la realización del EEG, se deberá lavar la cabeza sin utilizar lociones
capilares o lacas. Será el personal de Enfermería el encargado de colocar los electrodos en el cuero cabelludo utilizando pasta que facilite la conducción.
- Aconsejar dormir menos la noche antes, en caso de existir orden médica, para la realización del EEG en privación de sueño.
- La prueba requiere de cooperación, siendo fundamental que el paciente se mantiene quiero y con los ojos cerrados.
- Cómo realizar movimientos de hiperventilación, por si fuera preciso para la realización de la prueba.
- La utilización de fotoestimulación con el objetivo de examinar la respuesta cerebral ante este estímulo.
- No se debe suspender los tratamientos farmacológicos salvo excepción médica. - La duración de la prueba oscila entre 30 y 45 minutos aproximadamente. - Por lo general el procedimiento es grabado en vídeo. - En ocasiones se inyecta alguna sustancia intravenosa durante la prueba. Si existe pauta
médica, el personal de Enfermería responsable inyectará una determinada sustancia al paciente.

41
PET y SPECT:
- La prueba es indolora. - Posibles dudas derivadas de la prueba. - Si existe pauta médica del facultativo de Medicina Nuclear, el personal de Enfermería
responsable administrará una determinada sustancia intravenosa por la vía periférica. - Será introducido en una gammacámara, siendo el profesional de Enfermería el
responsable de que el paciente se encuentre correctamente colocado para la realización de la prueba.

42
Funciones de la/el enfermera/o circulante:
- Tener conocimiento sobre la intervención quirúrgica que va a llevar a realizar. - Tener conocimiento sobre el instrumental y aparataje que se va a requerir, así como
su localización. Tener la capacidad de acceder a ellos rápidamente en caso de necesidad y por consiguiente, disminuir complicaciones.
- Conocer el uso y conservación del instrumental y aparataje. - Comprobar que se dispone de todo el material necesario para llevar a cabo la
intervención quirúrgica. - Preparación del instrumental y material que va a ser necesario durante la intervención
quirúrgica. - Revisión del correcto funcionamiento del aparataje con ayuda de el/la enfermero/a
instrumentista y de la/el auxiliar de Enfermería. - Control y coordinación de todas las actividades e incidencias que ocurran dentro del
quirófano. - Controlar las necesidades requeridas por el paciente. - Evitar cualquier tipo de movimiento prescindible durante la intervención quirúrgica. - Asegurarse de la identidad del paciente y comprobar que se le ha realizado con éxito
la preparación quirúrgica y acogida. - Colaborar a trasladar al paciente a la mesa quirúrgica y a su correcta colocación. - Asegurarse de que el paciente mantenga una temperatura corporal caliente. - Preparación del paciente para intervención quirúrgica: posición quirúrgica, lavado de
la zona, etc. - Disminuir al mínimo posible las complicaciones potenciales, por lo que se ha de
asegurar de que se respete el espacio con respecto al campo quirúrgico (mínimo 50 cm), asegurarse de que las personas que acceden al quirófano están correctamente vestidas, etc.
- Manejar e identificar de manera correcta las muestras biológicas recogidas. - Ayudar en el acondicionamiento de la mesa quirúrgica. Mantener la higiene y el orden
del quirófano durante la intervención quirúrgica. - Suministrar el instrumental y materiales requeridos a la/el enfermera/o
instrumentista. Evitar el acercamiento excesivo al campo estéril. Anticiparse a las necesidades de material e instrumental. En la apertura del material se precisa una asepsia estricta.
- Recuento inicial, junto con la/el enfermera/o instrumentista, de gasas, compresas, agujas, etc, y su posterior registro.
- Recuento final, junto con la/el enfermera/o instrumentista, antes del cierre de la piel y las cavidades que hayan sido abiertas. Se debe repetir el recuento para asegurarse que no hay material y/o instrumental en el interior del paciente. En caso de incongruencia en el recuento se debe hacer una radiografía de la zona que ha sido intervenida. Asegurarse que no salen bolsas de basura del quirófano hasta que el recuento sea correcto.
- Control del balance de líquidos utilizados y recogidos durante la intervención. - Hacer el registro en la hoja de circulante. - Cuando finalice la intervención, debe retirar el instrumental y aparataje utilizado.
Avisar al celador para el traslado del paciente. Avisar a los servicios de limpieza y notificar que instrumentos y/o aparatos requieren una limpieza especial según protocolo.
- Preparación y reposición del quirófano para la siguiente intervención quirúrgica.

43
Funciones de la/el enfermera/o instrumentista:
- Realizar una revisión del quirófano para cerciorarse de que está en condiciones de ser
utilizado. - Tener conocimientos sobre la intervención quirúrgica que se va a realizar, técnica,
suturas y otros dispositivos que puedan ser utilizados. - Preparación del material para la intervención. - Asegurarse de que los paquetes estériles mantienen su integridad. - Llevar a cabo el lavado quirúrgico. - Colocarse la bata y los guantes siguiendo la técnica correcta. - Colocación de mesa quirúrgica. - Realización del recuento inicial de material con colaboración de la/el enfermera/o
circulante. El recuento se continúa durante la intervención quirúrgica. Recuento final antes del cierre de la piel y de la cavidad intervenida.
- Verificación del instrumental y material colocado en la mesa. - Control del campo quirúrgico y los tiempos de la operación. - Ayudar en la colocación del campo manteniendo extremando el cuidado en el manejo
de ropa estéril. - Ayudar a vestir la bata y los guantes a los cirujanos manteniendo una asepsia estricta. - Proporcionarle a los cirujanos el material e instrumental que precisen durante la
operación. - Comprobación del instrumental y material que se entrega al cirujano. - Mantener la mesa ordenada para que la entrega del material sea rápida y eficaz. - Seguir las medidas y protocolos con el objetivo de controlar la esterilidad del campo
quirúrgico. No dar la espalda al campo quirúrgico. Considerar no estéril todo lo que se encuentre inferior a la mesa y en caso de dudosa contaminación, considerar que si ha habido contaminación.
- Recuento de gasas, compresas y agujas utilizadas durante la intervención. Debe haber coincidencia entre el número inicial y final. A continuación se debe avisar al cirujano si hay coincidencia o no. En caso de no haber coincidencia, el cirujano revisará las cavidades y/o se realiza control mediante radiografía.
- Limpiar y desinfectar la herida quirúrgica, colocación de apósitos, colocación de reservorios de drenajes, etc.
- Retirar las mesas de instrumental y campo quirúrgico, asegurándose de que no hay - Asegurarse de que el paciente mantiene una temperatura corporal caliente hasta su
traspaso a la unidad de Reanimación, conservando su identidad. - Colocar instrumentos punzantes y agujas en su contenedor apropiado. - Colaborar en el traslado del paciente a la cama, asegurándose de su correcta colocación
en la cama y vigilar vías, drenajes, etc.

















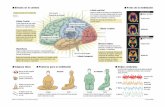

![[2]Bioinformatica Componente genético de Epilepsia en lóbulo temporal](https://static.fdocuments.es/doc/165x107/577d1cf31a28ab4e1e8b45c3/2bioinformatica-componente-genetico-de-epilepsia-en-lobulo-temporal.jpg)