FORMULACIÓN Y NOMENCLATURA INORGÁNICA (Apuntes Clase)
-
Upload
guillermo-fernandez -
Category
Documents
-
view
891 -
download
6
Transcript of FORMULACIÓN Y NOMENCLATURA INORGÁNICA (Apuntes Clase)

FORMULACIÓN Y NOMENCLATURA INORGÁNICA
COMBINACIONES BINARIAS1.- ÓXIDOS- Combinación de cualquier elemento de la tabla periódica con el oxígeno.
- Fórmula general: X2Ox (Excepto flúor)Ejemplos:
Fe2O3
Fe2O2 = FeO
- Nomenclatura: Óxido de ........... (...)Ejemplos:
Óxido de hierro (II) - FeODióxido de azufre - S2O4 =SO2
• Para nombrar un óxido de un metal seguiremos la siguiente regla: Óxido + Nombre del metal + (Valencia en números romanos).
• Para nombrar un óxido de un elemento no metálico nombraremos de derecha a izquierda y emplearemos prefijos como mono, di, tri, tetra, etc.para indicar el número de átomos de cada elemento.
- Óxidos del cloro:Cl2O - Monóxido de dicloroCl2O3 - Trióxido de dicloroCl2O5 - Pentaóxido de dicloroCl2O7 - Heptaóxido de dicloro
2.- PERÓXIDOS- Combinaciones en las que normalmente un metal (en estado de oxidación bajo) se combina con el grupo peróxido (O2), con valencia 2.
- Fórmula general: X2(O2)x
Ejemplos:Li2(O2)1
Ca2(O2)2 = CaO2
- Nomenclatura. Se emplea la palabra peróxido más el nombre del metal, y si este tuviera varias valencias se indicará entre paréntesis con números romanos.
Li2O2 - Peróxido de litioCaO2 - Peróxido de CalcioCu2O2 - Peróxido de cobre (I)CuO2 - Peróxido de cobre (II)
3.- HIDRUROS- Combinación de cualquier elemento de la tabla periódica con el hidrógeno.
3.1.- Hidruros metálicos- Fórmula general: XHx
- Nomenclatura: Hidruro de + nombre del metal + (Valencia)FeH2 - Hidruro de hierro (II)FeH3 - Hidruro de hierro (III)
3.2.- Hidruros no metálicos• Grupos 16 y 17- Fórmula general: HxX- Se forma con la menor valencia.
HCl - Cloruro de hidrógeno (Ácido clorhídrico)H2S - Sulfuro de hidrógeno (Ácido sulfhídrico)
1

• Grupos 13, 14 y 15- Fórmula general: XHx
- Nomenclatura:B - BH3 - Borano (Trihidruro de boro)C - CH4 - Metano (Tetrahidruro de carbono)Si - SiH4 - Silano (Tetrahidruro de silicio)P - PH3 - Fosfina (Trihidruro de fósforo)As - AsH3 - Arsina (Trihidruro de arsénico)Sb - SbH3 - Estibina (Trihidruro de antimonio)NH3 – Amoníaco (Trihidruro de nitrógeno)
SALES BINARIAS- Combinaciones de un no metal con un metal.
- Fórmula general: MxXm
- Nomenclatura: De derecha a izquierda los elementos. El nombre del no metal llevara el sufijo –uro y a continuación de + nombre del metal +(si tiene valencia, entre paréntesis con numeros romanos).
COMPUESTOS TERNARIOS1.- HIDRÓXIDOS- Fórmula general: M(OH)m
- Nomenclatura: Hidróxido de + nombre del metal + (valencia en nos romanos)Ca(OH)2 – Hidróxido de calcio
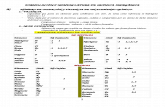
2.- ÁCIDOS OXOÁCIDOS- Fórmula general: HaXbOc
Nº oxidació
nFórmula Prefijo/sufijo
Fórmula
Nomenclatura tradicional Nomenclatura sistemática
1 HXO Ac. .hipo....oso HclO Ac. hipocloroso Monoxoclorato (I) de hidrógeno3 HXO2 Ac. ........oso HclO2 Ac. cloroso Dioxoclorato (III) de hidrógeno5 HXO3 Ac. ..........ico HclO3 Ac. clórico Trioxoclorato (V) de hidrógeno7 HXO4 Ac. per.....ico HclO4 Ac. perclórico Tetraoxoclorato (VII) de hidrógeno
Nº oxidació
nFórmula Prefijo/sufijo
Fórmula
Nomenclatura tradicional Nomenclatura sistemática
2 H2XO2 Ac. .hipo....oso H2SO2 Ac. hiposulfuroso Dioxosulfato (II) de hidrógeno4 H2XO3 Ac. ........oso H2SO3 Ac. sulfuroso Trioxosulfato (IV) de hidrógeno6 H2XO4 Ac. ..........ico H2SO4 Ac. sulfúrico Tetraoxosulfato (VI) de hidrógeno
S2O4 = SO2
SO2+H2O=H2SO3
Cl2O3+H2O=H2Cl2O4 =HCl2
Cuando el no metal tiene solo dos valencias diferentes, en la nomenclatura tradicional solamente será necesario utilizar los sufijos -oso, para la menor valencia, e -ico para la mayor.
H3PO4 – Ácido fosfóricoH3BO3 – Ácido bórico
2

SALES TERCIARIAS- Fórmula general: HXOM
→M (XO)m
Ejemplo: H 2 X O4M (III )→
M 2(MO4)3
- Nomenclatura:Hipo-........-ito.................-ito.................-atoPer-..........-ato
Ejemplos:HNO2Cu(II)
→Cu(NO2)2 – Dioxonitrato (II) de cobre / Nitrito de cobre
HNO3Cu(II )→
Cu(NO3)2 - Trioxonitrato (V) de cobre
HClONa→NaClO - Monoxoclorato (I) de sodio / Hipoclorito de sodio
HClO2Na→NaClO2 – Dioxoclorato (III) de sodio / Clorito de sodio
HClO3Na→NaClO3 - Trioxoclorato (V) de sodio / Clorato de sodio
HClO4 Na→NaClO4 - Tetraoxoclorato (VII) de sodio / Perclorato de sodio
SALES ÁCIDAS- N2CO3
→NaHCO3 - Hidrógenotrioxocarbonato (IV) de sodio / Bicarbonato de sodio
- H 2PO4→H 2 PO4 - Dihidrógeno tetraoxofosfato (V) de sodio
Na2HPO4
RADIACTIVIDAD
Es el fenómeno por el cual los núcleos de los átomos de ciertos elementos son capaces deemitir, de manera espontánea, radiaciones que les hacen transformarse en otros elementos.
Bi83209 – { 83 protones83 electrones
126neutrones}• Tipos de radiactividad1.- Partículas α (alfa) Ξ He2
4
X102244
→He24 + Y100
240
2.- Partículas β (beta) Ξ e−10
n01
→p11 + e−1
0
3.- Radiación γ (gamma)
- Vida mediaTiempo necesario para que se desintegren la mitad de los núcleos presentes en una muestra de un isótopo radiactivo.
3

Guillermo Fernández Gonzalo4º E.S.O. B – I.E.S. Fco. Grande Covián
4