Guía Química - Propiedades de la Materia
-
Upload
diana-carolina-benitez-monsalve -
Category
Documents
-
view
21 -
download
0
description
Transcript of Guía Química - Propiedades de la Materia

1 INSTITUCIÓN EDUCATIVA TÉCNICA SAGRADO CORAZÓN QUÍMICA 5°
Aprobada según Resolución No. 8758000490 – NIT 8000029113 – DANE 108758000490SOLEDAD – ATLÁNTICO
NOMBRE GRADO:DIRECCIÓN: CEL. EMAIL: TEL.
“CUANDO ENTIENDO EN QUÉ ESTOY FALLANDO Y BUSCO LA MANERA DE CORREGIRLO EMPIEZO A SER EXCELENTE”
GUÍA QUÍMICAGRADO 5°

2 INSTITUCIÓN EDUCATIVA TÉCNICA SAGRADO CORAZÓN QUÍMICA 5°
MATRIZ DE CONTENIDO
SEGUNDO PERIODOTEMAS NIVELES DE DESEMPEÑO
PROPIEDAD DE LA MATERIA
Elementos y compuestos químicos Propiedades generales de la materia
La masaEl Volumen La temperatura
Propiedades específicas de la materia Densidad SolubilidadDilatación Punto de ebulliciónPunto de fusión Conductividad Eléctrica Conductividad térmica
Identifica las propiedades generales y específicas de la materia.
Distingue los estados de la materia Diferencia las clases detransformación
de la materia. Establece diferencias entre elementos y
compuestos químicos.
ACTIVIDADES
1. Solución de talleres2. Elaboración e interpretación de gráficos3. Ejercicios sobre densidad, volumen y masa4. Elaboración de cuadros sinópticos y comparativos5. Elaboración de dibujos6. Consultas
“CUANDO ENTIENDO EN QUÉ ESTOY FALLANDO Y BUSCO LA MANERA DE CORREGIRLO EMPIEZO A SER EXCELENTE”

3 INSTITUCIÓN EDUCATIVA TÉCNICA SAGRADO CORAZÓN QUÍMICA 5°
LOS ELEMENTOS Y COMPUESTOS QUÍMICOS
ÁTOMO
La palabra ÁTOMO proviene del griego y significa sin división.
Podemos decir que el átomo es la partícula más pequeña de cualquier elemento.
Los átomos están constituidos por tres tipos de partículas muy singulares: PROTONES, NEUTRONES y ELECTRONES.
Con estas tres partículas subatómicas se puede construir cualquier tipo de átomo.
Un átomo está constituido por dos partes: el núcleo y la corteza. En el núcleo residen todos los protones y neutrones del átomo. Son partículas pesadas responsables de la mayor parte de la masa del átomo.
Tanto a los protones como a los neutrones se les denomina nucleones.
La carga de los electrones se toma como la unidad fundamental de carga eléctrica negativa. Entre los electrones y los protones, por ser partículas con carga, se establece una interacción eléctrica.
LA TABLA PERIÓDICA
“CUANDO ENTIENDO EN QUÉ ESTOY FALLANDO Y BUSCO LA MANERA DE CORREGIRLO EMPIEZO A SER EXCELENTE”

4 INSTITUCIÓN EDUCATIVA TÉCNICA SAGRADO CORAZÓN QUÍMICA 5°
Es la representación gráfica de los símbolos de los elementos químicos organizados número atómico y sus propiedades físico químicas.
ELEMENTOS: Sustancias puras formadas por un solo tipo de átomos.
COMPUESTOS: Sustancias puras, pero que están formadas por distintas clases de átomos (varios elementos)
INFORMACIÓN DE CADA ELEMENTO
Numero atómico: Es el total de protones que tiene un átomo.
Símbolo: Esta asociado al nombre de elemento y permite identificarlo.
Masa atómica: Conceptualmente, masa atómica (m. a.) es la masa de un átomo, y la masa de un átomo en particular es la suma de las masas de sus protones y neutrones.
Nombre del elemento: Es un tipo de materia constituida por átomos de la misma clase.
TALLER
“CUANDO ENTIENDO EN QUÉ ESTOY FALLANDO Y BUSCO LA MANERA DE CORREGIRLO EMPIEZO A SER EXCELENTE”

5 INSTITUCIÓN EDUCATIVA TÉCNICA SAGRADO CORAZÓN QUÍMICA 5°
1. En la tabla periódica señala cuales son los metales (azul), no metales (verde), metaloides (naranja) y gases nobles (amarillo), colorea.
2. Señala las partes de átomo.
3. Toma tu tabla periódica y busca en ella los elementos que se muestran a continuación. Completa el cuadro con la información que te suministra la tabla periódica.
Elemento Símbolo Grupo Periodo Numero atómico Masa atómicaCloroAluminioCalcio Oxígeno Hidrógeno BromoNeónPlata
“CUANDO ENTIENDO EN QUÉ ESTOY FALLANDO Y BUSCO LA MANERA DE CORREGIRLO EMPIEZO A SER EXCELENTE”

6 INSTITUCIÓN EDUCATIVA TÉCNICA SAGRADO CORAZÓN QUÍMICA 5°
4. Observa tu tabla y responde: ¿Qué elementó tendrá propiedades más parecidas al carbono? ¿El boro, el nitrógeno, el fósforo o el silicio? Explica tu respuesta. ____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
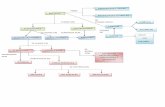
5. Completa el mapa conceptual
6.
Elige la respuesta correcta.
La material se encuentra formada por:
a) Átomos b) Moléculasc) Compuestos d) Elementos
Los seres vivos y los seres inertes se encuentra constituidos por:
b) Elementos b) Compuestos d) Materia d) Aire
4. Responde:
a) De las sustancias que forman parte de tu entorno, ¿Cuáles son elementos?b) ¿Qué es la tabla periódica?c) ¿Cómo se organizan los elementos en la tabla periódica?
5. Identifica la información la información que proporciona la tabla periódica por elemento.
“CUANDO ENTIENDO EN QUÉ ESTOY FALLANDO Y BUSCO LA MANERA DE CORREGIRLO EMPIEZO A SER EXCELENTE”

7 INSTITUCIÓN EDUCATIVA TÉCNICA SAGRADO CORAZÓN QUÍMICA 5°
6. Escribe el símbolo químico de los siguientes elementos.
Carbono _________ Radón _________ Potasio _________ Yodo ________Antimonio _________ Talio _________ Cobalto _________Manganeso _________ Cesio ________ Fósforo _________
7. Crucigrama Horizontales Verticales 1. Su símbolo es He 1. Símbolo químico del germanio 2. Grupo IIIA, periodo 6 2. Símbolo químico Níquel3. Elemento fundamental para vivir 3. Grupo IA, periodo 24. Su número atómico es 31 4. Su símbolo es O5. Símbolo químico del Hierro 5. Su símbolo es Li6. Segundo elemento del grupo de los
Gases nobles.
8. Observa la tabla periódica de los elementos. Identifica, en ella, los grupos y los periodos. Elabora un alista con los nombres de los elementos de los grupos representativos y escribe al frente de cada nombre, el símbolo correspondiente.
“CUANDO ENTIENDO EN QUÉ ESTOY FALLANDO Y BUSCO LA MANERA DE CORREGIRLO EMPIEZO A SER EXCELENTE”
5 3
↓ ↓
1 → 4
↓
1 2 →
↓ ↓
3 →
4 →
5 →
6 →

8 INSTITUCIÓN EDUCATIVA TÉCNICA SAGRADO CORAZÓN QUÍMICA 5°
9. Selecciona un término científico del recuadro para completar correctamente las oraciones. Escríbelas completas en el cuaderno.
a) La ____________ es la medida de la cantidad de materia que tiene un cuerpo.b) La partícula subatómica con carga negativa es el _________________.c) Los tres estados fundamentales de la materia son _______________, _______________ y
__________________.d) La unión de varias moléculas constituyen un __________________e) En el centro de átomo se encuentra el ________________ el cual contiene los
________________ y los _________________.
10. Los compuestos se representan por medio de fórmulas químicas. Éstas nos indican los elementos que las forman.
Observa las siguientes fórmulas y con ayuda de la tabla periódica identifica los elementos que hacen parte de cada compuesto.
CompuestoElemento
Símbolo Nombre
H2SO4
AgNO3
KCL
FeBr3
11. En tu cuaderno, clasifica las sustancias del recuadro en elementos y compuestos.Elabora una tabla con tu resultado.
“CUANDO ENTIENDO EN QUÉ ESTOY FALLANDO Y BUSCO LA MANERA DE CORREGIRLO EMPIEZO A SER EXCELENTE”
MASA – LIQUIDO – COMPUESTO – NÚCLEO – ELECTRÓN – NEUTRONES – SOLIDO – GASEOSO – PROTONES.

9 INSTITUCIÓN EDUCATIVA TÉCNICA SAGRADO CORAZÓN QUÍMICA 5°
Lectura Los Beneficios de la Aspirina
Motivado por encontrar un remedio para aliviar los dolores reumáticos que sufría su padre, en 1897, el químico Alemán Felix Hoffman descubrió la fórmula del compuesto ácido acetil salicílico, un componente natural que se encuentra en la corteza de árboles como el sauce. Con toda seguridad, el químico, no sospechó las dimensiones que con el tiempo iba a alcanzar su descubrimiento de lo que se conoce como aspirina.
Un siglo después de su descubrimiento, ese analgésico concebido inicialmente para combatir el dolor de cabeza y las fiebres gripales, es el medicamento más conocido y usado en el planeta.
Según datos de la casa comercial propietaria de la patente, actualmente se consumen 216 millones de comprimidos al día en todo el mundo.
Además de un remedio contra la jaqueca y la fiebre, la popular pastilla se ha revelado igualmente como un medicamento eficaz para la prevención primaria y secundaria del infarto de miocardio, del infarto cerebral, y de otras enfermedades.
Diversos estudios han demostrado que puede ser eficaz en la prevención del cáncer, las cataratas y las complicaciones en la diabetes. También puede ser utilizado con éxito en la recuperación en el deporte.
La aspirina continua asombrando a los científicos, en la medida en que sus virtudes como medicamento se amplían cada vez más.
Adaptado de El Tiempo, marzo 3 de 1997, página F-2. 16.
a) ¿Por qué te parecen importantes los estudios que se han hecho con la aspirina?b) Si tu fueras un científico que elabora un medicamento, ¿Qué crees que tendrías que hacer paraprobarlo? c) ¿Qué opinas de las personas que se automedican? Argumenta tu respuesta y discútela con el grupo. e) ¿Qué características presentan los cuerpos que nos rodean?
Exploración de ideas previas
“CUANDO ENTIENDO EN QUÉ ESTOY FALLANDO Y BUSCO LA MANERA DE CORREGIRLO EMPIEZO A SER EXCELENTE”
Sal de cocina, agua, aluminio, magnesio, dióxido de carbono

10 INSTITUCIÓN EDUCATIVA TÉCNICA SAGRADO CORAZÓN QUÍMICA 5°
Juanita quería preparar galletas, y encontró una receta deliciosa. Como no tenía recipientes ni instrumentos graduados para medir las porciones de los ingredientes, preparó las galletas tratando de calcular las cantidades. Le quedaron tan duras, que nadie se las pudo comer.
¿Cuáles errores crees que cometió Juanita? ___________________________________________
_________________________________________________________________________________ ¿Por qué crees que las galletas de Juanita quedaron tan duras?
____________________________________________________________________________________________________________
“CUANDO ENTIENDO EN QUÉ ESTOY FALLANDO Y BUSCO LA MANERA DE CORREGIRLO EMPIEZO A SER EXCELENTE”

11 INSTITUCIÓN EDUCATIVA TÉCNICA SAGRADO CORAZÓN QUÍMICA 5°
PROPIEDADES DE LA MATERIA
Como ya sabes el sol, las estrellas, el agua, el aire, las rocas y los seres vivos, entre otros, están formados por materia. Sin embargo, aunque todos los cuerpos están hechos de materia, se pueden diferencias unos de otros, por las propiedades de la materia que presentan cada uno.
La materia posee dos tipos de propiedades: las generales y las específicas.
Las propiedades generales nos sirven para identificar la sustancia de la que está compuesta la materia en cambio las propiedades especificas nos permite determinar la sustancia de la naturaleza que estudiamos.
Propiedades Generales de la Materia
Las propiedades generales de la materia son aquellas que son comunes a todos los cuerpos, por esta razón, aunque aportan información sobre el tipo de sustancia, no nos permiten identificarla ni diferenciarla de otra. Por ejemplo, si nos dicen que una sustancia tiene un volumen de 1 litro, con este dato no podemos saber de qué clase de sustancia se trata.
Algunas de las propiedades de generales son: la masa, latemperaturay el volumen.
“CUANDO ENTIENDO EN QUÉ ESTOY FALLANDO Y BUSCO LA MANERA DE CORREGIRLO EMPIEZO A SER EXCELENTE”

12 INSTITUCIÓN EDUCATIVA TÉCNICA SAGRADO CORAZÓN QUÍMICA 5°
La masa
La masa de un cuerpo es la cantidad de materia que posee dicho cuerpo. Por ejemplo, como un clavo es más grande que un alfiler, decimos que el clavo tiene más masa que el alfiler; es decir, que la masa del clavo es mayor que la del alfiler.
El instrumento que se usa para medir la masa es la balanza., y las unidades en las que se expresa son el gramo(g) y el kilogramo (kg).
Para medir la masa de un cuerpo en estado sólido y otro en estado líquido, se procede de forma diferente. Veamos.
- Para medir la masa de un cuerpo en estado sólido, se pone el cuerpo en la balanza y luego se registra e valor en la unidad respectiva. Es importante recordar que 1 kg equivale a 1.000 g.
- Para medir la masa de un cuerpo es estadolíquido, primero se mide la masa del líquido con su recipiente. Luego se mide la masa del recipiente vacío, finalmente se resta el valor de la masa del envase vació al valor de la masa del líquido en su envase. Esta diferencia corresponde, entonces, al valor de la masa del líquido.
Representa gráficamente en tu libreta. Inventa un ejemplo.
Peso
Fuerza que ejerce la tierra sobre los cuerpos por la atracción de la gravedad
El volumen
“CUANDO ENTIENDO EN QUÉ ESTOY FALLANDO Y BUSCO LA MANERA DE CORREGIRLO EMPIEZO A SER EXCELENTE”

13 INSTITUCIÓN EDUCATIVA TÉCNICA SAGRADO CORAZÓN QUÍMICA 5°
El volumen es la cantidad de espacio que ocupa un cuerpo. Por ejemplo, un balón de futbol ocupa más especio que una canica; por eso decimos que el volumen del balón es mayor al de la canica.
Los instrumentos empleados para medir el volumen varían según la forma y el estado en que se encuentre la materia. Por ejemplo si la materia está en estado sólido y tiene forma definida, se usa la regla, y si se encuentra en un estado líquido, se usa a probeta o la pipeta.
Las unidades de medida para expresar el volumen son: el milímetro (ml), el centímetro cúbico (cm3 o cc) y el litro (L), que corresponde a 1.000 ml.
¿Cómo se determina el volumen?
Si un objeto tiene forma geométrica regular, hallar su volumen se reduce a tomar unas pocas medidas y a realizar algunos cálculos. Por ejemplo para saber cuánto espacio ocupa un libro, debes medir ancho, largo y grosor. Luego realiza la multiplicación de estos números: el resultado es el volumen.
Observa la grafica
“CUANDO ENTIENDO EN QUÉ ESTOY FALLANDO Y BUSCO LA MANERA DE CORREGIRLO EMPIEZO A SER EXCELENTE”

14 INSTITUCIÓN EDUCATIVA TÉCNICA SAGRADO CORAZÓN QUÍMICA 5°
¿Si el objeto no tiene forma geométrica regular? Es muy sencillo. Te lo explicare con un ejemplo. Lee con atención.
Al sumergir un sólido en un recipiente con agua, la adición del volumen del sólido al volumen inicial de agua, hará que el nivel del agua aumente. La reta del volumen inicial del agua con su volumen final dará como resultado el volumen del objeto agregado al recipiente.
Observa con detenimiento la gráfica y analízala
La Temperatura
La Temperatura es una propiedad de la materia que está relacionada con la sensación de calor o frío que se siente en contacto con ella. Cuando tocamos un cuerpo que está a menos temperatura que el nuestro sentimos una sensación de frío, y al revés de calor. Sin embargo, aunque tengan una estrecha relación, no debemos confundir la temperatura con el calor.
Cuando dos cuerpos, que se encuentran a distinta temperatura, se ponen en contacto, se produce una transferencia de energía, en forma de calor, desde el cuerpo caliente al frío, esto ocurre hasta que las temperaturas de ambos cuerpos se igualan. En este sentido, la temperatura es un indicador de la dirección que toma la energía en su tránsito de unos cuerpos a otros.
Formas de medida
“CUANDO ENTIENDO EN QUÉ ESTOY FALLANDO Y BUSCO LA MANERA DE CORREGIRLO EMPIEZO A SER EXCELENTE”

15 INSTITUCIÓN EDUCATIVA TÉCNICA SAGRADO CORAZÓN QUÍMICA 5°
El termómetro: Es el instrumento utilizado habitualmente para medir la temperatura. La unidad en la que se mide la temperatura es el grado centígrado (ºC).
Diferencias entre calor y temperatura
Todos sabemos que cuando calentamos un objeto su temperatura aumenta. A menudo pensamos que calor y temperatura son lo mismo. Sin embargo, esto no es así. El calor y la temperatura están relacionadas entre sí, pero son conceptos diferentes.
Como ya dijimos, el calor es la energía total del movimiento molecular en un cuerpo, mientras que la temperatura es la medida de dicha energía. El calor depende de la velocidad de las partículas, de su número, de su tamaño y de su tipo. La temperatura no depende del tamaño, ni del número ni del tipo.
Por ejemplo, si hacemos hervir agua en dos recipientes de diferente tamaño, la temperatura alcanzada es la misma para los dos, 100° C, pero el que tiene más agua posee mayor cantidad de calor.
El calor es lo que hace que la temperatura aumente o disminuya. Si añadimos calor, la temperatura aumenta. Si quitamos calor, la temperatura disminuye.
La temperatura no es energía sino una medida de ella; sin embargo, el calor sí es energía.
Unidades de medida
TALLER EVALUATIVO
“CUANDO ENTIENDO EN QUÉ ESTOY FALLANDO Y BUSCO LA MANERA DE CORREGIRLO EMPIEZO A SER EXCELENTE”
1 kg equivale a 1.000 g. 1 kg equivale a 2 libras (Lb)
1 Lb equivale a 500 g1 litro equivale a 1000 ml o 1000 cm3
Kg= Kilogramo Lb= libraL= litro
Ml= mililitro cm3= centímetro cúbico
Misma temperatura, distinta cantidad de calor.

16 INSTITUCIÓN EDUCATIVA TÉCNICA SAGRADO CORAZÓN QUÍMICA 5°
1. Escribe la masa aproximada de tres objetos:
1. ________________ su masa aproximada es ___________ kg.2. ________________ su masa aproximada es ___________ kg.3. ________________ su masa aproximada es ___________ kg.
2. ¿Qué es masa?__________________________________________________________________________________________________________________________________________________________________
3. Diferencia entre masa y volumen?___________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
4. ¿Cuáles son las unidades utilizadas para medir la masa? Escribe al frente la abreviatura. ______________________ ____________________________ ____________________________ ______
5. ¿Qué es el volumen?__________________________________________________________________________________________________________________________________________________________________
6. ¿Qué es la temperatura? __________________________________________________________________________________________________________________________________________________________________
7. Escriba debajo de cada instrumento, que propiedad general de la materia se puede medir con él.
Termómetro____________
“CUANDO ENTIENDO EN QUÉ ESTOY FALLANDO Y BUSCO LA MANERA DE CORREGIRLO EMPIEZO A SER EXCELENTE”

17 INSTITUCIÓN EDUCATIVA TÉCNICA SAGRADO CORAZÓN QUÍMICA 5°
8. Lee el siguiente texto y responde las preguntas. La señora Martha compró en el supermercado los siguientes artículos: 3 libras de harina, 1 kilo de azúcar, 4 libras de mantequilla, 2 litros de leche, 2000 cm3 de aceite, 500 gramos de sal, 5 librad de chocolate, 3 litros de yogur, 2 libras de café, 3 litros de helado y 5 kilos de arroz.
a) En el siguiente cuadro clasifica los artículos teniendo en cuenta sus unidades de medida marcando con unaX
Artículo Unidades de masa Unidades de volumen Harina AzúcarMantequilla Leche Aceite Sal Chocolate Yogur CaféHelado Arroz
b) Analiza de nuevo la situación junto con la equivalencia de las unidades y responde las preguntas:
1. La cantidad de gramos de harina que compró la señora Martha, es de: a) 1 000 g b) 1 500 g c) 2 000 g d) 1 200 g
2. La cantidad de mililitros de helado es de: a) 1 500 ml b) 2 000 ml c) 3 000 ml d) 5 000 ml
3. La cantidad de centímetros cúbicos de yogur es: a) 2 000 cm3 b) 3 000 cm3 c) 1 000 cm3 d) 2 500 cm3
4. Los 5 kilos de arroz que compro la señora Martha , equivalen a: a) 2 libras b) 10 libras c) 3 libras d) 9 libras
5. 2 000 cm3 de aceite equivalen a: a) 1 litro b) 2 litros c) 2 000 litros d) 20 litros
6. 4 libras de mantequilla equivalen a:
“CUANDO ENTIENDO EN QUÉ ESTOY FALLANDO Y BUSCO LA MANERA DE CORREGIRLO EMPIEZO A SER EXCELENTE”

18 INSTITUCIÓN EDUCATIVA TÉCNICA SAGRADO CORAZÓN QUÍMICA 5°
a) 2 kilos b) 8 kilos c) 4 kilos d) 7 kilos
PROPIEDADES ESPECÍFICAS DE LA MATERIA
Las propiedades específicas o particulares de la materia son aquellas que nos permite diferenciar a un cuerpo de otro, es decir, caracterizan a cada clase de materia. Por ejemplo, a una manzana la podemos diferenciar de una naranja, por el color, el olor, el sabor, la dureza y la forma.
Otras propiedades específicas de la materia son:
Densidad Solubilidad Dilatación Punto de ebullición Punto de fusión Conductividad Eléctrica Conductividad térmica
Densidad: La densidad es una propiedad específica de la materia que nos permite diferenciar unos materiales de otros. Mide, en cierto modo, lo concentrada que esta la masa de un cuerpo. Por ejemplo, el plomo tiene la densidad mayor que la madera, es decir, está más compacta.
Una de las propiedades de los sólidos, así como de los líquidos e incluso de los gases es la medida del grado de compactación de un material: su densidad
La densidad es una medida de cuánto material se encuentra comprimido en un espacio determinado; es la cantidad de masa por unidad de volumen.
Los cuerpos sólidos suelen tener mayor densidad que los líquidos y éstos tienen mayor densidad que los gases.
“CUANDO ENTIENDO EN QUÉ ESTOY FALLANDO Y BUSCO LA MANERA DE CORREGIRLO EMPIEZO A SER EXCELENTE”

19 INSTITUCIÓN EDUCATIVA TÉCNICA SAGRADO CORAZÓN QUÍMICA 5°
Lo anterior está dado por el hecho de que en un gas las partículas que lo componen están menos cohesionadas, en términos vulgares esto significa que están más separados. En los líquidos hay mayor cohesión y en los sólidos la cohesión es mayor aún.
La densidad de los cuerpos se suele expresar en gramos (g) por milímetros (mL). Por ejemplo, 1 g de agua ocupa exactamente un volumen de 1 mL; por eso decimos que la densidad del agua es 1 gramo por mililitro (1 g/mL)
¿Cómo hallar el valor de la densidad de un cuerpo?
Es sencillo, simplemente dividimos la masa del cuerpo por su volumen
Masa Densidad = -------------------
Volumen Halla la densidad de un cuerpo que pesa 200 g y su volumen es 100 mL.
La solubilidad: es la capacidad que tiene una sustancia para disolverse en otras, a una determinada temperatura. Por ejemplo, en el agua se disuelven la sal y el azúcar, pero no el aceite. Con gasolina se pueden disolver aceites y pinturas, pero no sal ni azúcar.
La dilatación: es el aumento del volumen de un cuerpo por defecto de la temperatura. Por ejemplo, cuando un globo inflado se deja al sol, el aire que contiene se calienta, por lo que se dilata, es decir, su volumen aumenta y se puede reventar.
Pero no todos los cuerpos se dilatan de la misma manera; por ejemplo, los metales se dilatan más que la materia.
“CUANDO ENTIENDO EN QUÉ ESTOY FALLANDO Y BUSCO LA MANERA DE CORREGIRLO EMPIEZO A SER EXCELENTE”
El azúcar se disuelve más rápido en agua caliente que en agua fría.

20 INSTITUCIÓN EDUCATIVA TÉCNICA SAGRADO CORAZÓN QUÍMICA 5°
Punto de ebullición: La ebullición comienza cuando al calentar un líquido aparecen burbujas de gas en toda su masa. Esto ocurre a una temperatura fija para cada sustancia.
Llamamos Punto de ebullición de una sustancia a la temperatura a que se produce la ebullición de dicha sustancia. A nivel microscópico ocurre que casi todas las partículas tienen energía suficiente para escapar del líquido y liberarse en forma de gas.
Puto de fusión: Fusión es el proceso por el que una sustancia sólida al calentarse se convierte en líquido. Es el proceso inverso a la solidificación. Llamamos punto de fusión de una sustancia ala temperatura a la que se produce su fusión. Es una propiedad física característica de cada sustancia.
Conductividad eléctrica La conductividad eléctrica es la capacidad de un cuerpo de permitir el paso de la corriente eléctrica a través de sí.
Conductividad térmica La conductividad térmica es una propiedad física de los materiales que mide la capacidad de conducción de calor.
“CUANDO ENTIENDO EN QUÉ ESTOY FALLANDO Y BUSCO LA MANERA DE CORREGIRLO EMPIEZO A SER EXCELENTE”

21 INSTITUCIÓN EDUCATIVA TÉCNICA SAGRADO CORAZÓN QUÍMICA 5°
TALLER EVALUATIVO1. ¿Qué sucede al realizar las siguientes mezclas?
Agua + tinta: ______________________________________________________________________Agua + alcohol: ____________________________________________________________________Agua + arena: _____________________________________________________________________
2. Consulta en el diccionario los siguientes términos:
Solución: ___________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Soluto: _____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Solvente: ___________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
3. ¿Qué es la solubilidad? ___________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
4. Relaciona la propiedad de la materia con el caso correspondiente:
a. Para preparar un buen arroz es necesario que el agua este caliente. De lo contrario el arroz no se abre. ( ) Densidad
b. Una forma de ahorrar agua es introducir una botella u otroobjeto, en el tanque del inodoro. ( ) Dilatación
c. En un mismo supermercado, las manzanas, en igual cantidadpuedentener diferente precio. ( ) Masa
d. En las piscinas es común ver que los niños usan flotadores para su seguridad. ( ) Volumen
e. Si en la luna hubiera reinas de belleza, tendrían algunas característicasmuy diferentes que las de que tienen las ( ) Peso reinas de la tierra.
“CUANDO ENTIENDO EN QUÉ ESTOY FALLANDO Y BUSCO LA MANERA DE CORREGIRLO EMPIEZO A SER EXCELENTE”

22 INSTITUCIÓN EDUCATIVA TÉCNICA SAGRADO CORAZÓN QUÍMICA 5°
5. Resuelve:
¿Cuál es la densidad de una sustancia cuya masa es 200 g y su volumen de 40 cm3?
D = ___________ =
6. Para determinar el volumen de una piedra, ¿Cuál es el procedimiento más adecuado?
a) Medir el volumen inicial del agua y luego el volumen después de sumergido el cuerpo. Se procede a realizar una sustracción con los dos valores.
b) Medir la masa de la piedra y compararla con la masa de otro objeto.c) Medir la temperatura de la roca sumergida en el agua. d) Calentar la roca.
7. Con el fin de determinar que materiales flotan en el agua, se realiza una prueba con 4 tubos de igual volumen y de diferente material. Los resultados fueron los siguientes:
Material 1 0,85 g/cm3
Material 2 7,81 g/cm3
Material 3 1,17 g/cm3
Material 4 0,22 g/cm3
Si se realiza un viaje en un barco y el barco se hunde, el material más adecuado para utilizarcomo salvavidas es:
a) 1 b) 2 c) 3 d)4
8. Completa las afirmaciones utilizando las siguientes palabras:
a) La __________________ ocurre cuando los cuerpos aumentan su volumen al incrementar la temperatura.
b) Para medir la _____________________ debes utilizar la balanza.c) _____________________ es la capacidad que tiene una sustancia de disolverse en otra.d) El punto de _______________ hace referencia a la temperatura en la cual una sustancia
hierve.“CUANDO ENTIENDO EN QUÉ ESTOY FALLANDO Y BUSCO LA MANERA DE
CORREGIRLO EMPIEZO A SER EXCELENTE”
Volumen Masa Fusión
Temperatura Termómetro
Ebullición
Dilatación
Solubilidad
Solvente

23 INSTITUCIÓN EDUCATIVA TÉCNICA SAGRADO CORAZÓN QUÍMICA 5°
e) La sustancia que sirve para disolver a otra se llama ____________________f) A la medida de la fuerza de atracción que ejerce la Tierra sobre los cuerpos se le denomina
_________________g) A la temperatura en la cual una sustancia cambia de solidó a liquidó se le llama punto de
______________h) El __________________ lo utilizamos para medir la temperatura de los cuerpos.i) A la medida del calor de los cuerpos se le llama ____________________
9. Clasifica las siguientes propiedades de la materia como generales o específicas, escríbalas en la columna correspondiente.
10. Una caja de zapatos mide 30 cm de largo, 12cm de ancho y 10cm de alto. ¿Cuál esel volumen de la caja?
11.
12.
“CUANDO ENTIENDO EN QUÉ ESTOY FALLANDO Y BUSCO LA MANERA DE CORREGIRLO EMPIEZO A SER EXCELENTE”

24 INSTITUCIÓN EDUCATIVA TÉCNICA SAGRADO CORAZÓN QUÍMICA 5°
13.
“CUANDO ENTIENDO EN QUÉ ESTOY FALLANDO Y BUSCO LA MANERA DE CORREGIRLO EMPIEZO A SER EXCELENTE”

25 INSTITUCIÓN EDUCATIVA TÉCNICA SAGRADO CORAZÓN QUÍMICA 5°
Aplico la lógica conceptual:
“CUANDO ENTIENDO EN QUÉ ESTOY FALLANDO Y BUSCO LA MANERA DE CORREGIRLO EMPIEZO A SER EXCELENTE”