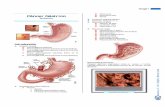
Her2 en cáncer gástrico
-
Upload
sandro-casavilca-zambrano -
Category
Health & Medicine
-
view
202 -
download
4
Transcript of Her2 en cáncer gástrico
PATOLOGOS ESPECIALIZADOS
Henry Guerra Mil lerCarlos Barrionuevo CornejoSandro Casavilca Zambrano
Mayo-2011
A pesar que en el mundo la incidencia de cáncer gástrico está disminuyendo, su frecuencia permanece en cuarto lugarOMS: reporta aprox 1 mil lón de nuevos casos al año
- Actualmente representa la segunda causa de muerte por cáncer, +/- 800.000 fallecidos al año (2008) - En la mayoría de los pacientes el diagnóstico se realiza en estadios avanzados de la enfermedad
Estadío cl inico
TNM % pacientes Sobrevida a los 5 años
IAIB
T1 N0 M0 T1 N1 M0 T2a/b N0 M0
20% 60-80%
II T1 N2 M0 T2a/b N1 M0 T3 N0 M0
15% 35%
IIIA
IIIB
T2a/b N2 M0 T3 N1 M0 T4 N0 M0 T3 N2 M0 65%
10-20%
IV T4 N1-3 M0 T1-3 N3 M0 T1-4 N1-3 M1
5%
Actualmente no existe un tratamiento estándar para el cáncer gástrico avanzado:Se uti l iza la quimioterapia tradicional con fluor pir imidinas (capecitabine, 5-FU) o a base de platino (cisplatino, axaliplatino) y eventualmente otros medicamentos (epirubicina o docetaxel)Sin embargo, la toxicidad es alta
Carcinoma primario Sobre-expresión de p185 HER-2
Mama 18-32%
Ovario 30-38%
Pulmón 27-50%
Sarcomas 30-35%
Estómago 12-50%
Vejiga 28-35%
Esófago 50-70%
Glándulas salivales 32-58%
Desde el inicio de los años 90, aparecieron trabajos de investigación que reportaban sobre-expresión de la proteína HER-2 en neoplasias originadas en diversos lugares anatómicos:
En estos últ imos años, en cáncer gástrico, se ha confirmado la sobre-expresión de la proteína p185c-erbB2, producida por el gen HER2 (miembro de la super-familia de los receptores del factor de crecimiento epidérmico), ubicado en el cromosoma 17 q12-q21
HER-2
100
100
100
44
82
33
36
59
24
48
79
28
Dominio ricoen cisteina
C-terminal
Dominio tirosina quinasa
erbB1HER-1EGF-R
erbB2HER-2
erbB3HER-3
erbB4HER-4
EGF, TGFα, HB-EGF.Amfiregulina, β-celul ina Heregulinas
NRG-2, NRG-3Heregulinas,
β-celulina
La proteína que encoda el gen HER-2 es una proteína tras-membrana de aproximadamente 185 kD, representa un receptor para la t irosina quinasa, se compone de una pequeña parte tras-membrana, de una porción extra-celular y de otra intracelular
HER-2 HER-3
Membranacelular
El vínculo con un l igando provoca homo o hetero dimerización de la parte extra-celular, iniciando la transducción de la señal para l legar a la fosfori lación de la t irosina quinasa
Por tanto, el gen HER-2 actúa como un oncogen, que a través de su producto proteico, modula la división celular, la apoptosis, la adhesión, la migración y la diferenciación celular
Proliferación, migración celular, diferenciación
Ligando
Ligando
Membranacelular
HER-2
HER-1HER-2HER-3HER-4
Señal intracelular
ADNADNTrascripción
génica
HER-2 HER-3
Membranacelular
La frecuencia de la sobre-expresión de la proteína HER-2 varía en relación al t ipo histológico del cáncer gástrico:
Tipo intestinal : 16-34% Tipo difuso: 02-07%
Referencia
Porcentaje de posit ividad para HER-2 Métod
oIntestinal Difuso Mixto
Tanner, 2005 21,5% 2% 5% CISH
Gravalos, 2007 16% 7% 14% IHQFISH
Lordic, 2007 34% 6% 20% IHQFISH
Bang, 2008 31,8% 6,2% 20,6% IHQFISH
HER-2 HER-3
Membranacelular
La frecuencia de la sobre-expresión de la proteína Her2 varía en relación a la localización anatómica de la neoplasia:
CA de la unión gastro-esofágica y fondo: 24-35 %CA del cuerpo y antro: 09-20%
ReferenciaPorcentaje de posit ividad para HER-2
Métodounión gastro-
esofágica Cuerpo, antro
Tanner, 2005 24% 12% CISH
Gravalos, 2007 25% 9,5% IHQFISH
Lordic, 2007 32% 18% IHQFISH
Bang, 2008 34,8% 19,8% IHQFISH
Brazil
Peru
Denmark
Great Britain
ItalyPortugal
Germany
Belgium
TurkeyFrance
Spain
Japan
Australia
China
Korea
Costa Rica
Mexico
Guatemala
Russia
South Africa
Panama India
Taiwan
Finland
Considerando la sobre-expresión de la proteína HER-2, se iniciaron investigaciones para averiguar la ut i l idad del uso de terapias biológicas específ icas con anticuerpos monoclonales contra la molécula HER-2, de manera similar a lo que ya se había estudiado con el cáncer de mama
EstudioToGA
0
20
40
60
80
100
Be
lgiu
m
De
nm
ark
Fin
lan
d
Fra
nce
Ge
rma
ny
UK
Au
str
alia
Po
rtu
ga
l
Me
xic
o
Ita
ly
Ind
ia
Sp
ain
Pa
na
ma
Co
sta
Ric
a
Ch
ina
Ru
ssia
Tu
rke
y
Pe
ru
Bra
zil
Gu
ate
ma
la
Ja
pa
n
Ko
rea
So
uth
Afr
ica
Ta
iwa
n
Cuerpo y antroUnión G-E
Bang YJ, et al. J Clin Oncol 2009; 27:Abstract 4556
Porcentaje
ToGA: Distr ibución de los diferentes casos en relación a los países participantes
0
5
10
15
20
25
30
35A
US
TR
ALIA
JA
PA
N
ITA
LY
DE
NM
AR
K
GR
EA
T B
RIT
AIN
FR
AN
CE
SO
UT
H A
FR
ICA
PA
NA
MA
BE
LG
IUM
PO
RT
UG
AL
GE
RM
AN
Y
KO
RE
A
CH
INA
ME
XIC
O
SP
AIN
RU
SS
IA
PE
RU
TU
RK
EY
GU
AT
EM
ALA
IND
IA
CO
ST
A R
ICA
BR
AZ
IL
FIN
LA
ND
TA
IWA
N
Países
En el estudio ToGA la posit ividad media global estuvo del 22,1%
35%
30%
25%
20%
15%
10%
5%
0%
22,1%
El estudio ToGA confirmó la diferente frecuencia de HER-2 en relación a la localización anatómica de la neoplasia
Ubicación de la neoplasiaUnión gastro-esofágica
Cuerpo y antro Metástasis
HER-2 posit ivo 34,8% 19,8% 16,3%HER-2 negativo
65,2% 80,2% 83,7%
Positividad total = 20,5%p< 0,002
Positividad total = 20,5%p< 0,002
Histotipo según clasif icación de Lauren
Intestinal Difuso Mixto
HER-2 posit ivo 31,8% 6,2% 20,6%
HER-2 negativo
68,2% 93,8% 79,4%
Positividad total = 22,9%p< 0,001
Positividad total = 22,9%p< 0,001
La frecuencia de la sobre-expresión de la proteína HER-2 en relación al t ipo histológico del cáncer gástrico reportada en el estudio ToGA se muestra similar a la anteriormente observada en otras investigaciones:
.
Debe considerarse también, el aspecto de la inmunotinción y/o la amplif icación génica, para diagnosticar como posit ivo para HER-2 El primer aspecto que se observó es que la inmuno-reacción no se presenta homogénea en todo el tumor, es heterogénea:
La expresión y/o la amplif icación génica de HER-2 se presenta también heterogénea dentro de la misma formación tubuloglandular
INMUNOHISTOQUIMICA POSITIVA PARA HER-2Tinción intensa lateral o baso-lateral en la membrana(por lo menos en el 10% de la células neoplásicas)
En el cáncer de células “en anil lo de sello” la membrana celular pudiera estar completamente coloreada
Si la inmunotinción lateral o basolateral de membrana es débil o moderada (en por lo menos el 10% de la células neoplásicas), se cataloga con “puntuación 2+” y el caso se considera DUDOSO
Si la puntuación es de 2+ deberá realizarse prueba molecular complementaria para determinar si existe o nó amplif icación génica o polisomía 17. Sólo así se podrá indicar la terapia específica
Amplif icación de HER-2 Polisomía del cromosoma 17
La puntuación 1+, interpretada como NEGATIVO, es cuando la inmunotinción lateral o basolateral de membrana es muy débil o apenas perceptible, en por lo menos el 10% de la células neoplásicasLa misma puntuación se atribuye si la membrana celular se colorea sólo parcialmente
La puntuación 0, interpretada como NEGATIVO, es cuando no hay inmunotinción lateral o baso-lateral de membrana, o si hubiese, ésta es menor del 10% de las células neoplásicas
Una reacción inmunohistoquímica intensa (puntuación 3+) se identif ica con faci l idad y usualmente no hay dudas en su interpretación
Si la inmunotinción se presenta débil o moderada (puntuación 2+), a veces no es fáci l diferenciarla de la que resulta muy débil o apenas perceptible (puntuación 1+)Las recomendaciones del Grupo de Estudio de HER-2 sugieren:Puntuación 2+, si el patrón de la inmunotinción no se discrimina a un aumento de 100X, pero si claramente a un aumento de 200XPuntuación 1+, si la inmunotinción puede valorarse recién con un aumento de 400X
Bang YJ, et al. J Clin Oncol 2009; 27:Abstract 4556.
En cáncer de mama, el diagnóstico de posit ividad para HER2 puede realizarse con inmunohistoquímica o biología molecular (FISH o CISH), en cáncer gástrico la HI t iene un valor preponderante:
IHQ 0 IHQ 1+ IHQ 2+ IHQ 3+ Total
FISH +N. casos
94 96 212 354 756
% 4.9 15.7 54.6 94.9 23
FISH -N. casos
1815 514 176 19 2524
% 95.1 84.3 45.4 5.1 77
TotalN. casos
1909 610 388 373 3280
% 100 100 100 100 100
5
IHQ3+/FISH+
0.2 0.4 0.6 1 2 3 4
Subgrupos
IHQ0/FISH+
IHQ1+/FISH+
IHQ2+/FISH+
IHQ3+/FISH-
IHQ 0 or 1+/FISH+
IHQ2+/FISH+ o IHQ3+
Proporciónde riesgo
Terapia favorable
Terapia desfavorable
En CA de mama, ambas metodologías tienen el mismo valor diagnóstico. En cáncer gástrico se demostró que los casos con puntuación 0 ó 1+ en HI pero con FISH posit ivo no responden a la terapia especif ica
Considerando que en la mayoría de pacientes, el cáncer gástrico se diagnostica en estadios avanzados, cuando ya es inoperable, es necesario averiguar la posibi l idad del uso de terapias biológicas que puedan adicionarse a la QT tradicional
En tal sentido, debemos resolver las siguientes interrogantes:1. ¿El diagnóstico de la expresión de HER-2 puede
realizarse en las biopsias endoscópicas? 2. ¿Cuál sería el número óptimo suficiente de biopsias?3. ¿Cómo evaluar la posit ividad en las biopsias?4. ¿Qué valor terapéutico tiene la posit ividad para HER2
en las biopsias?
En el estudio ToGA se evaluó también la sobre-expresión de la proteína HER2 en relación al t ipo de muestra:No se encontró diferencia estadistica signif icativa
Pieza quirúrgica Biopsia
HER-2 posit ivo 19,7% 22,7%
HER-2 negativo
80,3% 77,7%
Positividad total = 21,7%P = 0,13
Positividad total = 21,7%P = 0,13
El diagnóstico inmunohistoquímico de la expresión de HER2 puede realizarse en las biopsias gástricas
Como el CA gástrico es muy heterogéneo, será importante investigar una cantidad suficiente de tejido neoplásico (cantidad suficiente del material biópsico) El Grupo de Estudio de HER2 sugiere examinar de 6 a 8 biopsias , para reducir la probabil idad de falsos negativos
Para confirmar la validez del diagnóstico de la expresión de HER-2 en la biopsia endoscópica, se realizó un estudio clínico y otro patológico
El estudio clínico demostró que no existe diferencia de respuesta a la terapia biológica específica, evaluando la posit ividad para HER2 en la pieza quirúrgica o en la biopsia endoscópica
La investigación patológica, confirmó la correlación entre los resultados de la pieza quirúrgica y los de la biopsia endoscópica, a condición que la cantidad de tejido examinado sea suficiente
El diagnóstico inmunohistoquímico de HER2 puede realizarse en la biopsia gástr ica endoscópica
La interpretación inmunohistoquímica de HER2 en las biopsias gástricas endoscópicas se evalúa de manera diferente que en la pieza quirúrgica:
• Puntuación 3+ = posit ividad intensa, completa, baso lateral o lateral, en por lo menos un grupo de células cohesivas
• Puntuación 2+ = posit ividad moderada o débil, completa, baso lateral o lateral, en por lo menos un grupo de células cohesivas Debe realizarse prueba molecular complementaria (FISH, CISH)
• Puntuación 1+ = posit ividad muy débil o apenas perceptible lateral o baso-lateral o inmunotinción parcial de la membrana
• Puntuación 0 = ninguna inmunotinción