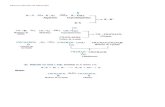
Reacciones Endotérmica y Exotérmica
-
Upload
ludwin-wilfredo-diaz-jimenez -
Category
Documents
-
view
7 -
download
0
Transcript of Reacciones Endotérmica y Exotérmica

REACCIONES ENDOTÉRMICA Y EXOTÉRMICA
PRÁCTICA
COMPETENCIA A DESARROLLAR:
Identifica reacciones químicas que absorben y liberan energía del medio.MATERIALES
Agitador de vidrio Bloque de madera pequeño Hule aislante Termómetro Vaso de Precipitados
SUSTANCIAS:
Agua destilada H 2S O 4
INTRODUCCIÓN
Las reacciones químicas suponen un proceso en el que se produce una reordenación de átomos, con ruptura de enlaces y formación de otros nuevos. Este es un aspecto parcial de la reacción, ya que el otro aspecto (tan importante como el anterior) lleva implícito un cambio energético entre los estados inicial y final. Algunas reacciones ocurren con desprendimiento de calor del sistema hacia el exterior; son las reacciones exotérmicas; en otras reacciones sucede el proceso inverso; y son las reacciones endotérmicas. Procesos exotérmicos espontáneos, tales como el arder del fuego o las corrientes de agua por las montañas, son muy conocidos y relativamente fáciles de explicar. Los procesos endotérmicos espontáneos, por lo contrario, no son tan comunes y son más difíciles de explicar. Se puede usar su existencia para recalcar la importancia de la ley universal que dice que: los sistemas tienden al caos.
¿Sabías que?
La vida sin energía es imposible. No hay ningún sistema viviente que pueda permanecer vivo por mucho tiempo sin algún tipo de combustible, es decir, el alimento que lo mantenga vivo. Así como el calor que desprenden algunos gases como el metano, etano, propano y butano, el cual se provecha para la calefacción en fábricas y hogares.

PREGUNTA GENERADORA:
¿El calor liberado por el combustible en las máquinas, será igual al calor liberado por el cuerpo humano? Fundamenta tu respuesta.
DESARROLLO EXPERIMENTAL:1.- Coloca 10 ml de agua destilada en un vaso de precipitado y mide su temperatura
2.- Añade 1 gramos de cloruro de amonio y agita hasta disolución total, mida su Temperatura: y su pH: ________________________________
Escribe tus observaciones:
¿A qué tipo de reacción corresponde?
DIBUJOS Y O ESQUEMAS
CUESTIONARIO:
1.- De acuerdo a la energía implicada ¿Cómo se clasifican las reacciones?

2.- ¿Cómo se logra que una reacción absorba o libere energía?
3.- ¿Cuáles son las aplicaciones de las reacciones endotérmicas y exotérmicas?
FUNDAMENTACIÓN DE RESULTADOS:
Vo. Bo. Del Profesor firma del alumno
Fecha