celula
-
Upload
masachuses -
Category
Education
-
view
233 -
download
2
Transcript of celula

Ideas Claves
• Todos los organismos vivos obedecen a las mismas leyes físicas y químicas
• La Vida es Compleja, Dinámica, Organizada y Automantenida.
• La Vida es Celular y basada en la información
• La Vida se adapta y evoluciona


CélulasCélulas

Mundo Vivo = Especies VivasMundo Vivo = Especies Vivas
Células procariotas o Células procariotas o Células eucariotasCélulas eucariotas

Procariotas Vs Eucariotas• Más numerosas y
abundantes: únicas 3800-1800 ma
• Carecen de núcleo y compartimientos delimitados por mem
• Proc. Unicels: Seres vivos más pqños -> ocupan cada nicho
• 2 Grupos: Bacterias y Arqueas
• Pared cel
• Núcleo verdadero delimitado x mem
• Gran compartimentación interna -> mayor complejidad estructural
• Especialización y cooperación intercelular
°C

Semejanzas Procariotas Vs Eucariotas
• Composición química semejante
• ADN o material genético: código universal





BACTERIAS• Diversas en hábitats y capacidades nutritivas:
Explotan diferentes fuentes de energía, nutrientes y entornos
∀ →Diversidad bioquímica• Bac que usan E luminosa ->CO2 > mols orgánicas• Bac productoras de enfermedades: tuberculosis, sífilis,
cólera, etc• La gran mayoría: fnes vitales en el mantenimiento de
la vida en la tierra: reciclaje de nutrientes como C, N, S. Ej. Rhizobium transforma nitrógeno (N2) en amoníaco (NH3)
• Interés industrial: producción antibióticos, yogur, quesos, etc.



ARQUEAS• 1977: C. Woese análisis de A.N• En algunos aspectos más cercanas a
eucariotas que bacterias Ej. Stma síntesis de proteínas
• Increible capacidad para ocupar cualquier nicho, Extremófilas: Temperaturas muy altas o muy bajas, concentraciones salinas elevadas, P elevada, etc. -> conocimiento singular sobre adaptaciones de la est. Biomolecular Ej.Extremozimas (enz que operan en condiciones nocivas)
• Utilidad en Biorreparación

EUCARIOTAS• Ppal diferencia: Presencia de Núcleo• Tamaño: ∼10 veces mayor, 10-30 µm• Volumen: ∼100 veces >, hepatocito 6000-10000 µm3
• Complejidad estructural: organelas especializadas -> compartimentación, eficiencia en fn -> respuesta, comunicación
• Multicelularidad: Cooperatividad y especialización -> stmas vivos ordenados que forman entidad coherente




MEMBRANAS BIOLÓGICAS






CITOESQUELETO






SISTEMA SISTEMA ENDOMEMBRANOSOENDOMEMBRANOSO
•Retículo endoplasmico liso y rugoso
•Aparato de Golgi
•Endosomas
•Lisosomas
•Vesículas y gránulos secretores
•Mitocondrios y Cloroplastos









AGUA

Propiedades del agua hacen posible la vida sobre la tierra

Propiedades Térmicas del H2O
• Agua es líquida a T ambiente, otras mol de peso mol similar no
• Puntos de fusión y ebullición son muy muy altos; Ej. H2S, f: -100 °C e: -91 °CH2O, f: 0 °C e: +100 °C
• Hielo: # máximo de enlaces de H• Líquida: continua formación y ruptura
enlaces de H

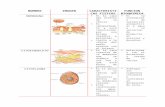
LA MOLÉCULA DE AGUACada molécula de agua está compuesta por un átomo de Oxígeno, unido a dos átomos de Hidrógeno (H2O), mediante enlaces covalentes.
La molécula de agua se comporta como un dipolo eléctrico con dos cargas parciales positivas (δ+) y dos negativas (δ- ).
δ+
δ+
δ-
δ-
La molécula es como un tetraedro asimétrico con sus dos H en los dos vértices hacia un lado y el O en el otro vértice.
El agua es una sustancia polar y su reactividad depende de esta característica.


ENLACE O PUENTE DE HIDRÓGENO
Es una atracción débil entre un átomo electronegativo en una mol y un átomo de H en otra molécula.
Carácter electrostático (iónico) y covalente


Los enlaces de H se hacen y deshacen permanentemente.
En el agua líquida, un enlace de hidrógeno dura en
promedio 10-11 s

En su estado sólido, el agua es
una estructura rígida, cristalina, y
muy ordenada.

A medida que aumentamos la temperatura, el agua pasa del
estado sólido al estado líquido.
Temperatura < 0°CEn el hielo, las
moléculas de agua están muy
organizadas y algo separadas

La estructura pierde su organización y aumenta la relación de molécula por
volumenA 4°C las
moléculas están mas próximas
que en el hielo, y se alcanza la
máxima densidad

En este proceso, la energía en
forma de calor, rompe los enlaces de hidrógeno.
Se sigue aumentando la temperatura...

En el vapor de agua, las
moléculas están mas separadas, y presentan pocos
enlaces de H

Facilita la disolución de sustancias iónicas.
Alta Constante Dieléctrica 80
Conduce calor y ayuda en la termorregulación, distribuyendo homogéneamente el calor de un medio.
Alta Conductividad Térmica O.6 J/s.m.K
Contribuye a la capilaridad en plantas, facilita intercambio de materiales en tejidos.
Alta Tensión Superficial 7.3 x 10-2 J/m2
Libera grandes cantidades de energía térmica, contribuye a mantener la temperatura corporal mediante sudoración.
Alto Calor de Evaporación 2260 J/g
Modera la temperatura en el ambiente (océanos) y en los organismos
Alto Calor Específico 4.18 J/g.K
IMPORTANCIAIMPORTANCIAPROPIEDADPROPIEDAD


• El enlace de H es responsable de los puntos de congelación y ebullición inusualmente elevados del agua
• Debido a que agua posee capacidad calorífica elevada puede absorber y liberar calor lentamente.
• El agua desempeña un papel importante en la regulación del calor en los seres vivos


PROPIEDADES DISOLVENTES DEL AGUA
Sustancias Hidrofílicas e Hidrofóbicas• Disolvente biológico ideal: mayoría
constituyentes seres vivos: Na+, K+, Cl-, azúcares, aa.
• No disuelve lípidos y algunos aa: est. Supramoleculares (ej. Membranas) y procesos bioquímicos como plegamiento proteíco.

Productos de ionización del agua son determinantes importantes en la estructura y propiedades de proteínas, ácidos nucleícos, membranas, ribosomas, etc.

PROPIEDADES DISOLVENTES DEL AGUA
Estructura dipolar del agua y su capacidad para formar enlaces de hidrógeno permite al agua disolver sustancias iónicas y polares


Cuando se disuelve en agua un compuesto iónico como el NaCl, sus iones se separan debido a que las moléculas polares del agua atraen a los iones más que éstos se atraen entre sí.









OSMOSISProceso espontáneo por el cual las moléculas del disolvente pasan a través de una mem semipermeable desde una solución de menor concentración de soluto a una disolución de mayor concentración de soluto.
PRESIÓN OSMÓTICAPresión requerida para detener el proceso de osmosis/ o flujo de agua a través de mem

Efecto de soluciones hipertónicas e hipotónicas sobre las cels animales
Disoluciones isotónicas no modifican el volumen cel
Disoluciones hipotónicas rompen las cels Ej hemólisis en eritrocitos en agua pura
Disoluciones hipertónicas arrugan las cels (crenación)

IONIZACIÓN DEL AGUA
Agua bajo grado de ionización: (a 25°C solamente 1 de 107 moléculas esta disociada):
H2O H+ + OH-
H2O + H2O = H3O+ + OH-
[H2O] = 55.5 M
La concentración Molar del agua pura → > que otros solutosDespejando tenemos:
[H+] x [OH-] = 1 x 10-14 M2
[H+] = [OH-] = 1 x 10-7 M
[H+][OH-]
Keq = _________ = 1.8 x 10-16
[H2O]Kw: Producto iónico del H2O
Kw = 1.8 x 10-16 x 55.5 M= [H+][OH-]

IONIZACIÓN DEL AGUA
• La concentración del H+ en agua pura es 1 x 10-7 M
• Cuando una disolución contiene cantidades [H+] = [OH-] → Neutra
• Cuando una sustancia iónica o polar se disuelve en H2O, puede cambiar el número relativo de [H+] y [OH-]
• Las disoluciones con exceso de [H+] → ACIDAS
• Las disoluciones con exceso de [OH-] → BASICAS
• La concentración de ión H+ varía en intervalo amplio: 100 y 10-14 lo cual proporciona la base de la escala de pH (pH = - log [H+] )


H2O OH- H++
1x10-7 M +1x10-14 M 1x10-7 M
0 1 2 3 4 5 6 7 8 9 10 11 12 13 14
100 10-1 10-2 10-3 10-4 10-5 10-6 10-7 10-8 10-9 10-10 10-11 10-12 10-13 10-14
HClJugos
GástricosJugo de Limón
Coca-ColaVinagre
CervezaTomate Agua
LechePlasmaSudor
Lágrimas
PanCafé
NegroBicarbonat
ode Soda
Detergentes
Amoníaco
Limpiadorde hornos
NaOH
NEU
TRO
Valor de pH
[H+](M)
AUMENTO DE ACIDEZ AUMENTO DE BASICIDAD
pH = -Log10 [H+]

H+
• Es muy importante en stmas biológicos• Su concentración afecta mayoría de
procesos cels y del organismo– Estructura, función de proteínas– Velocidad de rxs bioquímicas– Generación de E y endocitosis

BIOMOLÉCULAS ACIDAS O BÁSICAS
ACIDO : Donador de H+ Ej. HClBASE : Aceptor de H+ Ej. NaOH
• Los ácidos y bases FUERTES se ionizan casi completamente en H2O
• Los que NO se ionizan completamente se denominan Acidos débiles o Bases débiles

Acidos y Bases Débiles
Ionizan 1-5%HA ⇔ H+ + A-
Base conjugada de HA
La Fuerza de un ácido débil (su capacidad para liberar H+) se puede determinar:Donde K = cte de disociación del ácido
pKa = - log Ka < pKa → ácido + fuerte

Valores de constantes de disociación y los pKa de varios ácidos débiles comunes

AMORTIGUADORES
• Regulación de pH esencial en seres vivos• Ej. Sangre: 7.4 (7.35 – 7.45): acidosis, alcalosis
• Acidosis: como consecuencia de producción excesiva de ácidos en los tejidos, de pérdidas de bases en los líquidos corporales o de un fallo en los riñones para excretar metabolitos ácidos Ej. Diabetes mellitus, inanición; pH < 7.0 SNC ↓ y coma
• Alcalosis: causado por vómitos prolongados o por ingestión excesiva de fármacos alcalinos, sobreexcita SNC y músculos entran en estado de espasmo → convulsiones → paro respiratorio

AMORTIGUADORES
• Amortiguadores ayudan a mantener ∼ constante concentración de ión H+
• Amortiguadores más comunes son Acidos débiles y sus bases conjugadas
• S/n amortiguadora puede soportar cambios de pH debido a que entre componentes del amortiguador se establece un equilibrio
• Amortiguadores obedecen a ppio de Le Chatelier: si a un rx se le aplica una distorsión, el equilibrio se desplazará en la dirección que la contrarreste.

Amortiguador acetato: A. Acético + acetato sódico

Amortiguadores Fisiológicos• Fluidos extra e intracels contienen
pares conjugados acido-base los cuales actúan como Tampones al pH normal de dichos fluidos
• Amortiguadores más importantes: – Bicarbonato en sangre – Fosfato: – Proteína: Ej hemoglobina, albúmina
sérica, etc