Enlaces químicos II: Geometría molecular e hibridación de ... · Predicción de la geometría...
-
Upload
trinhnguyet -
Category
Documents
-
view
234 -
download
1
Transcript of Enlaces químicos II: Geometría molecular e hibridación de ... · Predicción de la geometría...

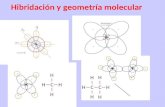
Enlaces químicos II:
Geometría molecular e hibridación Geometría molecular e hibridación
de orbitales atómicos

Modelo de repulsión de los pares electrónicos de la capa de valencia (RPECV):
Predicción de la geometría de las moléculas mediante la
repulsión electroestática de pares de electrones compartidos
y libres.
Clase
# de átomos
unidos al átomo
central
# de pares
libres en el
átomo centralArreglo de los pares
de electronesGeometría
molecular
AB2 2 0 lineal lineal
B B

Cl ClBe
2 átomos enlazados al átomo central
0 pares de electrones libres en el átomo central

AB2 2 0 lineal lineal
Clase
# de átomosunidos al
átomo central
# de pares
electrones
libres en el
átomo central
Geometría molecular
RPECV
AB3 3 0triangular
plana
triangular
plana
Arreglo de los pares de electrones


AB2 2 0 lineal lineal
Clase
# de átomosunidos al
átomo central
# de pares de
electrones libres
en el átomo
central
Geometría
molecular
RPECV
AB3 3 0triangular
plana
triangular
plana
Arreglo de
los pares de
electrones
AB4 4 0 tetrahédrica tetrahédrica

10.1

AB2 2 0 lineal lineal
Clase
# de átomosunidos al
átomo central
# de
electrones
libres en el
átomo central
Arreglo de los pares
de electrones
Geometría
molecular
RPECV
AB3 3 0triangular
plana
triangular
plana
AB4 4 0 tetrahédrico tetrahédrico
AB5 5 0triangular
bipiramidal
triangular
bipiramidal


AB2 2 0 lineal lineal
Clase
# de átomospegados al
átomo central
# de pares libres en el
átomo central
Arreglo de los pares de
electrones
Geometría
molecular
RPECV
AB3 3 0triangular
planotriangular
plano
10.1
AB4 4 0 tetrahédrico tetrahédrico
AB5 5 0triangular
bipiramidaltriangular
bipiramidal
AB6 6 0 octahédricooctahédrico



Comparación de la repulsión entre pares de electrones
pares compartidos vs.
pares compartidos pares libres vs.
pares librespares libres
vs. pares compartidos> >

Clase
# de átomospegados al
átomo central
# de pares libres en el
átomo central
Arreglo de los pares de
electrones
Geometría
molecular
RPECV
AB3 3 0triangular
plana
triangular
plana
AB2E 2 1 triangular
planadoblada
plana

Clase
# de átomospegados al
átomo central
# de pares libres en el
átomo central
Arreglo de los pares de
electrones
Geometría
molecular
RPECV
AB3E 3 1
AB4 4 0 tetrahédrica tetrahédrica
tetrahédrica triangular
piramidal

Clase
# de átomospegados al
átomo central
# de pares libres en el
átomo central
Arreglo de los pares de
electrones
Geometría
molecular
RPECV
AB4 4 0 tetrahédrico tetrahédrico
AB3E 3 1 tetrahédricotriangular
piramidalpiramidal
AB2E2 2 2 tetrahédrico doblada
H
O
H

Clase
# de átomospegados al
átomo central
# de pares libres en el
átomo central
Arreglo de los pares de
electrones
Geometría
molecular
RPECV
AB5 5 0 triangular
bipiramidal
triangular
bipiramidal
AB4E 4 1 triangular
bipiramidal
tetrahedro
deformadobipiramidal deformado

Clase
# de átomospegados al
átomo central
# de pares libres en el
átomo central
Arreglo de los pares de
electrones
Geometría
molecular
AB5 5 0triangular
bipiramidal
triangular
bipiramidal
AB4E 4 1triangular
bipiramidal
tetrahedro
deformado
RPECV
bipiramidal deformado
AB3E2 3 2triangular
bipiramidalForma de T
ClF
F
F

Clase
# de átomospegados al
átomo central
# de pares libres en el
átomo central
Arreglo de los pares de
electrones
Geometría
molecular
AB5 5 0triangular
bipiramidal
triangular
bipiramidal
AB4E 4 1triangular
bipiramidal
tetrahedro
deformado
RPECV
bipiramidal deformado
AB3E2 3 2triangular
bipiramidal
en forma
de T
AB2E3 2 3triangular
bipiramidallineal
I
I
I

Clase
# de átomospegados al
átomo central
# de pares libres en el
átomo central
Arreglo de los pares de
electrones
Geometría
molecular
AB6 6 0 octahédricooctahédrico
AB5E 5 1 octahédricopiramidal cuadrada
F
RPECV
Br
F F
FF
F

Clase
# de átomospegados al
átomo central
# de pares libres en el
átomo central
Arreglo de los pares de
electronesGeometría
molecular
AB6 6 0 octahédricooctahédrico
AB5E 5 1 octahédricopiramidal
cauadrada
cuadrada
RPECV
AB4E2 4 2 octahédrico cuadrada plana
Xe
F F
FF


Predicción de la geometría molecular
1. Escribir la estructura de Lewis para una molécula.
2. Contar el número de pares de electrones en el átomo central y el numero de átomos unidos al átomo central.
3. Usar el RPECV para predecir la geometría de la molécula.
¿Cual es la geometría molecular del SO y del SF ?¿Cual es la geometría molecular del SO2 y del SF4?
SO O
AB2E
ligado
S
F
F
F F
AB4E
tetrahedro
deformado

Momentos dipolares y moleculas
polares
H F
Región de alta densidad electrónica
Región de baja densidad electrónica
δ+ δ−
µ = Q x r
Q es la carga
r es la distancia entre dos cargas
1 D = 3.36 x 10-30 C m



¿Cuáles de las siguientes moléculas tienen un
momento dipolar?
H2O, CO2, SO2, y CH4
O
momento dipolar
(molécula polar)
S
momento dipolar
(molécula polar)
CO O
momento no
dipolar (molécula
no polar)
C
H
H
HH
momento no
dipolar
(molécula no polar)

¿Tiene el BF3 un
momento dipolar?

¿Tiene CH2Cl2 un
momento dipolar?