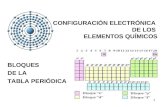
Número de oxidación de los elementos químicos
-
Upload
jeclar1307 -
Category
Education
-
view
88 -
download
3
Transcript of Número de oxidación de los elementos químicos

NÚMERO DE OXIDACIÓN DE LOS ELEMENTOS QUÍMICOS

EXPLORACIÓN DE CONOCIMIENTOS
1. Cómo definimos a un átomo.2. En qué difieren los conceptos ion y átomo.3. Qué es la estequiometria dentro de la
química.


• Qué sucedería si en una reacciónA + B C se considera • A + B >C • A + B ˂C• A + B = C

OXIDACIÓN Y REDUCCIÓN
• OXIDACIÓN: La oxidación se da cuando un elemento o compuesto pierde uno o más electrones.
• REDUCCIÓN: La reducción se produce cuando un elemento o compuesto gana electrones



REGLAS PARA DETERMINAR EL
NÚMERO DE OXIDACIÓN

OBJETIVO : Determinar el número de oxidación de iones metálicos y no-metálicos para comprobar la estabilidad química de un compuesto• Diferencia entre un ion y un átomo
• Cuándo se genera la estabilidad química
• Mediante que enlaces se pueden unir los iones y formar compuestos
EXPLORAR

El número de oxidación es la carga neta que tiene un átomo, es decir el número de electrones que un átomo pone en juego al formar un compuesto.
Na+1Cl-1

PRIMERA REGLA
• Los elementos libres poseen un número de oxidación igual a cero
Na + O2 Na2O
Al + H2 AlH3
Fe + O2 Fe2O3

SEGUNDA REGLA
• En un ion monoatómico el número de oxidación es igual a su carga
Na2O AlH3 Fe2O3
Na O Al H Fe O


TERCERA REGLA
LA OXIDACIÓN DEL OXÍGENO.En los compuestos formados por la unión de iones metálicos y el oxígeno, su número de oxidación es O-2.
Be + O2 BeO
Al + O2 Al2O3

CUARTA REGLA
LA OXIDACIÓN DEL HIDRÓGENO.El hidrógeno tiene una oxidación, H+1.Cuando se enlaza con metales, H-1
Cl + H2 HCl
S2 + H2 H2S
K + H2 KH

QUINTA REGLA
Los no-metales tienen un número de oxidación negativa cuando se unen a un metal, y un número de oxidación positiva cuando se unen al oxígeno.
GaCl3 Cl2O
RbS SO
BaBr2 Br2O5

SEXTA REGLALos metales de transición tienes números de oxidación específicas.
Cu+1+2
Hg+1+2
Au+1+3
Ni+2+3
Fe+2+3
Co+2+3
Cr+2+3
Sn+2+4
Pb+2+4.

COMPUESTO NEUTRO
LA SUMA DE LOS NÚMEROS DE OXIDACIÓN DE LOS IONES QUE FORMAN UN COMPUESTO, MULTIPLICADOS POR SUS RESPECTIVOS SUBINDÍCES ES CERO