Propiedades de las Proteínas y Actividad Enzimática en Productos Agroindustriales
-
Upload
orgrimardono -
Category
Documents
-
view
165 -
download
2
description
Transcript of Propiedades de las Proteínas y Actividad Enzimática en Productos Agroindustriales

“UNIVERSIDAD NACIONAL DE SAN CRISTÓBAL DE HUAMANGA”FACULTAD DE INGENIERÍA QUÍMICA Y METALURGIA
ESCUELA DE FORMACIÓN PROFESIONAL DE INGENIERÍA AGROINDUSTRIAL
COMP. PROD.
AGROINDUSTRIALES(TA 341)
INFORME DE PRÁCTICA DE LABORATORIO Nº 04 y 05”Propiedades de las Proteínas” y “Actividad Enzimática en
Productos Agroindustriales”
DOCENTE :
ESTUDIANTE :
AYACUCHO – PERÚ2012

UNSCH – FIQM INGENIERÍA
AGROINDUSTRIAL
PRÁCTICA N 04
PROPIEDADES DE LAS PROTEÍNAS
I. OBJETIVOS
1.1. Determinar las propiedades de las proteínas: punto isoeléctrico y
desnaturalización.
1.2. Identificar y observar una proteína desnaturalizada.
II. FUNDAMENTO TEÓRICO
Si en una disolución de proteínas se producen cambios de pH, alteraciones en
la concentración, agitación molecular o variaciones bruscas de temperatura, la
solubilidad de las proteínas puede verse reducida hasta el punto de producirse
su precipitación. Esto se debe a que los enlaces que mantienen la
conformación globular se rompen y la proteína adopta la conformación
filamentosa. De este modo, la capa de moléculas de agua no recubre
completamente a las moléculas proteicas, las cuales tienden a unirse entre sí
dando lugar a grandes partículas que precipitan. Además, sus propiedades
biocatalizadores desaparecen al alterarse el centro activo. Las proteínas que se
hallan en ese estado no pueden llevar a cabo la actividad para la que fueron
diseñadas, en resumen, no son funcionales.
Esta variación de la conformación se denomina desnaturalización. La
desnaturalización no afecta a los enlaces peptídicos: al volver a las condiciones
normales, puede darse el caso de que la proteína recupere la conformación
primitiva, lo que se denomina renaturalización.
COMP. PROD. AGROINDUSTRIALES (TA 341) 1

UNSCH – FIQM INGENIERÍA
AGROINDUSTRIAL
III. MATERIALES Y MÉTODOS
3.1 MATERIALES REACTIVOS
- Tubos de ensayo - Acido Acético
- Baño maría - Hidróxido de sodio
- Pipetas - Acetato de sodio
- Vasos de precipitado - Sulfato de cobre II 0,5%
- Albúmina al 1% - pH Metro
- Cloruro de sodio 1% - 6 Huevos
3.2 METODOLOGÍA EXPERIMENTAL
3.2.1 DETERMINACIÓN DEL PUNTO ISOELÉCTRICO
Preparar soluciones de pH distinto mezclando ácido acético y acetato de sodio
en las siguientes proporciones:
pH CH3COONa 0,1 M (mL) CH3COOH 0,1 M (mL)
3,6
3,8
4,0
4,2
4,4
4,6
4,8
5,0
5,2
5,4
5,6
0,4
0,6
0,9
1,3
1,95
2,45
3,0
3,5
3,95
4,1
4,5
4,6
4,4
4,1
3,7
3,05
2,55
2,0
1,5
1,05
0,9
0,5
Agitar bien cada tubo y agregar 1 mL de solución de albúmina de huevo.
Observar y establecer el Punto Isoeléctrico.
COMP. PROD. AGROINDUSTRIALES (TA 341) 2

UNSCH – FIQM INGENIERÍA
AGROINDUSTRIAL
3.2.2 DESNATURALIZACIÓN DE LA ALBÚMINA
Colocar 10 g de albúmina en dos tubos de ensayo.
Al primer tubo agregarle 5 mL de NaCl al 1%. Agitar.
Llevar los dos tubos a calentamiento en agua hirviente. Cuando el segundo
tubo esté caliente, agregar 5 mL de NaCl al 1%. Agitar.
Continuar calentando por 10 minutos. Extraer del agua caliente y enfriar.
Efectuar el examen de Biuret a las dos muestras. Comparar los resultados.
3.2.3 IDENTIFICACIÓN DE PROTEÍNAS O REACCIÓN DE BIURET
A 2 mL de solución de albúmina al 10% (clara de huevo) se le añade 2 mL de
NaOH al 10%, luego se le adiciona unas gotas de solución de CuSO4 (sulfato
cúprico), si observamos que se forma un complejo de color azul intenso nos
indica que hay una reacción positiva ( es decir hay presencia de proteínas).
COMP. PROD. AGROINDUSTRIALES (TA 341) 3

UNSCH – FIQM INGENIERÍA
AGROINDUSTRIAL
IV. RESULTADOS Y DISCUSIÓN
4. 1. DETERMINACIÓN DEL PUNTO ISOELÉCTRICO
Cuando una proteína se acerca demasiado a su punto isoeléctrico, esta tiende
a desnaturalizarse y pierde solubilidad lo cual hace que se formen precipitados,
pudimos observar esta reacción en las soluciones de clara de huevo con el pH
más ácido:
Nº pH Resultado Nº pH Resultado
01 3,6 06 4,6
02 3,8 07 4,8
03 4,0 08 5,0
04 4,2 09 5,2
05 4,4 10 5,4
El tubo con mayor cantidad de precipitados fue el número 02 de pH 3.8 por lo
que decimos que a este pH decimos que se encuentra el punto isoeléctrico.
COMP. PROD. AGROINDUSTRIALES (TA 341) 4

UNSCH – FIQM INGENIERÍA
AGROINDUSTRIAL
4.2. DESNATURALIZACIÓN DE LA ALBÚMINA
La muestra calentada no resulto positivo y la albumina sin calentar se formó el
complejo azul.
4.3. IDENTIFICACIÓN DE PROTEÍNAS O REACCIÓN DE BIURET
A 2 mL de solución de albúmina al 10% (clara de huevo) se le ha ñadido 2 mL
de NaOH al 10%, luego unas gotas de solución de CuSO4 (sulfato cúprico)
Se observa el color violeta índico positivo en la muestra, por lo que concluimos
que contiene proteínas.
V. CONCLUSIONES
Gracias a su reacción tan clara de la precipitación de la albumina en su
punto isoeléctrico, determinarlo es fácil, sin embargo no podemos tener
una precisión suficiente, pues dependemos de la reacción que se
aprecia solo visiblemente.
Por otro lado la identificación de las proteínas se hace con reacciones
igualmente apreciables por un gran cambio de color.
En la desnaturalización de las proteínas, estas pierden muchas
propiedades, entre ellas las que las hacen susceptibles al cambio de
color en la prueba de biuret.
COMP. PROD. AGROINDUSTRIALES (TA 341) 5

UNSCH – FIQM INGENIERÍA
AGROINDUSTRIAL
VI. CUESTIONARIO
6.1. ¿Qué utilidad tienen la determinación del Punto Isoeléctrico, desde el
punto de vista de la aplicación tecnológica o nutricional de las proteínas?
La cualidad anfotérica de las proteínas permite su disociación y determina,
junto a otros factores, su solubilidad. La carga neta de la proteína varía con las
condiciones del medio (pH) en que se encuentra. Así pueden comportarse
como aniones o cationes (ácidos o bases), o precipitar cuando la carga neta es
cero. La primera cualidad permite que las proteínas tengan una cierta
capacidad tamponadora o amortiguadora. Por otro lado, La precipitación se
produce a un pH determinado (punto isoeléctrico para cada tipo de proteína y
es de crucial importancia en la industria alimentaria, tanto para evitar que
precipiten proteínas como para conseguirlo. El punto isoeléctrico es
característico de cada proteína y esto permite lograr la precipitación selectiva
de proteínas de un medio. No obstante, la solubilidad (le las proteínas no
depende exclusivamente del pH, del medio, sino que influyen también tanto el
número de grupos polares y apolares corno su distribución. Así, es posible que
una proteína con un escaso número de interacciones hidrofobias no precipite
en su punto isoeléctrico debido a la hidratación y a la repulsión estérica.
Investigue cuáles son los puntos isoeléctricos de las siguientes
proteínas: caseína, albúmina, globulina (glicinina en soja)
Sustancia Punto Isoeléctrico
Caseina 4.6
Albúmina 4.7
Globulina G1 (lisozima) 10.7
Globulina G2 5.5
Globulina G3 5.8
COMP. PROD. AGROINDUSTRIALES (TA 341) 6

UNSCH – FIQM INGENIERÍA
AGROINDUSTRIAL
VII. REFERENCIAS BIBLIOGRAFICAS
Víctor Manuel Rodríguez Rivera, Edurne Simón Magro, “Bases de la
Alimentación Humana”. España. Editorial Netbiblo, 2da Edición, S.L. p.
193.
Angel Gil Hernández, “Tratado de Nutrición: Composición y Calidad
Nutritiva de los Alimentos”, España, Editorial Medica Panamericana, 2da
Edición, Tomo II. páginas 80 y 6,
Antonio Peña Díaz Antonio Peña, “Bioquímica”, México 2004, Editorial
Limusa p. 96.
COMP. PROD. AGROINDUSTRIALES (TA 341) 7

UNSCH – FIQM INGENIERÍA
AGROINDUSTRIAL
PRÁCTICA N 05
ACTIVIDAD ENZIMÀTICA EN PRODUCTOS AGROINDUSTRIALES
I. OBJETIVOS
1.1 Observar y medir la actividad enzimática de enzimas presentes en la
levadura durante el proceso de fermentación en diferentes harinas de
origen vegetal.
1.2 Observar la inactividad de enzimas presentes en algunos productos por
acción del calor, de antioxidantes y del pH.
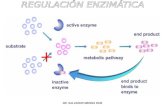
II. FUNDAMENTO TEÓRICO
Las enzimas, funcionan como catalizadores naturales en las reacciones
bioquímicas. Ellas no cambian o se utilizan durante su reacción. Por ejemplo,
durante la fermentación, las enzimas que se elaboran a partir de células de
levadura, convierten las moléculas de azúcar en moléculas de etanol, pero las
moléculas de levadura no disminuyen durante el proceso. Por esta razón,
pequeñas cantidades de enzimas comerciales dan grandes resultados y al
comparar con otros métodos de procesamiento, son mucho más económicos.
Las enzimas (una gran parte), se derivan de organismos fúngicos y
bacterianos. Algunos productos se elaboran a partir de plantas como la papaya,
la piña, etc. ó a partir de productos que se generan de tejidos de animales,
como por ejemplo la lipasa pancreática.
Las enzimas son muy específicas en el trabajo que realizan. Por ejemplo, las
enzimas de amilasa, solo trabajan en almidón, las enzimas de proteasa lo
hacen con proteínas, etc., esto permite que las enzimas contengan
características que son de gran beneficio en procesamientos industriales.
III. MATERIALES Y METODOS
COMP. PROD. AGROINDUSTRIALES (TA 341) 8

UNSCH – FIQM INGENIERÍA
AGROINDUSTRIAL
3.1 MATERIALES
Prueba de probeta
Probeta graduada de 100 ml
Baño maría
Harinas de origen vegetal: trigo, camote, quinua, etc.
Inactivación de enzimas presentes en la papa y manzana
Cocinas
Vasos de precipitación
Ácido cítrico
Bisulfito de sodio
Solución de guayacol 0,05%
Solución de peróxido de hidrógeno 0,05%
Muestras vegetales: papas, manzanas, limones y frutas diversas.
3.2 METODOLOGÍA
3.2.1 PRUEBA DE LA PROBETA
Pesar 1 g de levadura y disolver en 30 ml. de agua potable en un vaso de 250
ml. añadir seguidamente una mezcla de 9 g de harina de trigo y 1 g de harina
de otro origen.
Mezclar rigurosamente con la ayuda de un agitador. En seguida transferir a una
probeta graduada de 100 ml., observar el volumen inicial y llevar a incubar a un
Baño María a 26,5C. Anotar el volumen de la suspensión a intervalos de 5
minutos, comparando así la rapidez y acción de las levaduras. Conjuntamente
llevar un control conteniendo harina de trigo.
Registrar estos resultados y obtener la rapidez de las levaduras expresadas en
el tiempo necesario para alcanzar el "máximo". Así una levadura de acción
enzimática mediana necesitará 90 minutos dando un N90, mientras que una
levadura rápida necesitará solo 75 minutos a la cual le corresponderá el N75;
esta variación en el tiempo también depende del tipo de harina o mezcla de
COMP. PROD. AGROINDUSTRIALES (TA 341) 9

UNSCH – FIQM INGENIERÍA
AGROINDUSTRIAL
ellas.
3.2.2 INACTIVACIÓN DE ENZIMAS PRESENTES EN ALGUNOS
PRODUCTOS AGROINDUSTRIALES
3.2.2.1 EFECTO DEL TIEMPO DE CALENTAMIENTO
Pelar una muestra de papa y/o otras muestras asignadas por el profesor, cortar
en rodajas de 2 cm. de espesor, colocar en un recipiente con agua hirviente por
el período de 1, 2, 4, 6, 8, 10 y 12 minutos; dejar una rodaja de testigo y
realizar la prueba de guayacol en c/u de las rodajas es decir añadirle 1 ml de
guayacol al 0,05% y 1 ml de peróxido de hidrógeno al 0,05% de tal forma de
cubrir la superficie de la rodaja con las dos soluciones.
Observar que sucede después de 3 minutos
Determinar el tiempo necesario para la inactivación de enzimas presentes en
las papas.
3.2.2.2. EFECTO DE LOS ANTIOXIDANTES
EFECTO DEL ÁCIDO CITRICO
a) Tomar 10 g de pulpa de manzana en 3 tubos de ensayo.
b) Añadir 1 mL de ácido cítrico al 1%, 2,5% y 5% respectivamente a los
tubos
c) Mezclar bien y comparar con un cuarto tubo que contiene 10 g de pulpa
y 1 mL de agua, luego de 30 minutos de reposo.
3.2.2.3. EFECTO DEL PH
Cortar cubitos de manzana de 1 cm. de arista aproximadamente.
Bañar los cubitos con cada una de las soluciones siguientes: ácido
COMP. PROD. AGROINDUSTRIALES (TA 341) 10

UNSCH – FIQM INGENIERÍA
AGROINDUSTRIAL
cítrico 0,5%, HCl 2M, zumo de limón y agua destilada
Verificar el pH de las soluciones
Dejar en reposo los cubitos por 30 minutos y comparar los resultados
IV. RESULTADOS Y DISCUSIÓN
4.1. PRUEBA DE LA PROBETA
Determinar el tiempo necesario para encontrar el máximo desarrollo de la
fermentación por acción de enzimas de la harina y levadura.
Tiempo Volumen
0 36
5 38
10 46
15 60
20 73
25 85
El máximo volumen alcanzado a los 25 min. Fue de 85 mL. Probablemente el
tiempo optimo este muy cerca, pues ha alcanzado más del doble de su volumen.
COMP. PROD. AGROINDUSTRIALES (TA 341)
0 5 10 15 20 250
10
20
30
40
50
60
70
80
90
36 38
46
60
73
85
Volumen
Tiempo (min)
Volu
men
(mL)
11

UNSCH – FIQM INGENIERÍA
AGROINDUSTRIAL
4.2. INACTIVACIÓN DE ENZIMAS PRESENTES EN ALGUNOS
PRODUCTOS AGROINDUSTRIALES
4.2.1. EFECTO DEL TIEMPO DE CALENTAMIENTO
A partir de la muestra 6, la que se hirvió por 8
minutos, vemos que las enzimas ya no dan
un resultado positivo al análisis con el
guayacol, por lo que decimos que el tiempo
óptimo es de 8 minutos.
4.2.1. EFECTO DE LOS ANTIOXIDANTES
EFECTO DEL ÁCIDO CITRICO
El primer tubo de la izquierda contiene la
muestra de manzana solo con agua, y se
puede apreciar claramente que el de la
derecha no ha sufrido oxidación, por lo
que el pH más ácido evita que las
enzimas se degraden produciendo este
color anaranjado.
4.2.2. EFECTO DEL PH
COMP. PROD. AGROINDUSTRIALES (TA 341) 12

UNSCH – FIQM INGENIERÍA
AGROINDUSTRIAL
En el tubo con ácido cítrico se observa una ligera oxidación; con el HCl, la
oxidación es mucho menor, lo mismo con el zumo de limón, pese a ser menos
ácido que la solución con HCl, ha protegido más a los trozos de manzana, y
finalmente el agua destilada, que posee un pH neutro, ha protegido en algo la
oxidación gracias a que aísla a los trozos de manzana del oxígeno del aire, mas
no del que contiene en sí.
V. CONCLUSIONES
La velocidad con la que la levadura produce CO2 es muy rápida, por lo que
se le ha aprovechado durante tantos años con tan buenos resultados.
Además de no contener enzimas u otras sustancias que puedan ser
nocivas para el consumo humano.
La acción de calor se ha podido observar en la prueba de guayacol, en la
cual determinamos para la muestra el tiempo mínimo necesario para la
inactivación de las enzimas de la papa, pues, estas pasado cierto tiempo
expuesto a la temperatura de ebullición del agua, ya no pueden mantener
su capacidad catalítica. En este ensayo, hemos desnaturalizado al punto
de destruir a algunas enzimas que se identifican con el guayacol, por lo
que ya pueden reactivarse.
El pH al ser un factor de actividad enzimática varia la velocidad y
capacidad de estas de cumplir con su actividad por lo que variando
ligeramente el pH podemos modificar la velocidad y prolongar la vida útil
de algunos alimentos.
VI. CUESTIONARIO
6.1 ¿Cuál es el complejo enzimático que participa en el proceso
fermentativo del pan?
COMP. PROD. AGROINDUSTRIALES (TA 341) 13

UNSCH – FIQM INGENIERÍA
AGROINDUSTRIAL
Enzima o Complejo
EnzimáticoEvento Bioquímico Descripción
Invertasa Inversión de la sacarosa
Desdobla la sacarosa que
se agregó a la harina en
glucosa y fructosa.
α-amilasa y α-
amilasa.
La conversión de almidón
en dextrinas y maltosa.
Hidrolizan el almidón en
polisacáridos más
pequeños, como las
dextrinas y la maltosa.
MaltasaLa conversión de la
maltosa en glucosa.
Hidroliza la maltosa en dos
unidades de glucosa.
ZimasaLa utilización de la
glucosa y la fructosa.
Convertir la glucosa y la
fructosa - producidas a
partir de la inversión de la
sacarosa agregada y de la
hidrólisis del almidón - en
etanol y dióxido de carbono.
Proteasas
La modificación de la
estructura de las
proteínas del gluten.
Gracias a esto, se pueden
formar las complejas redes
de gluten capaces de
retener el gas producido.
6.2 ¿Cuáles son las enzimas presentes en todos los vegetales?
Las peroxidasas constituyen un ubicuo grupo de enzimas, presentes en todos
los vegetales superiores que han sido investigados y en los leucocitos. Suelen
contener un grupo prostético hemo (ferriprotoporfirina), no obstante, también
pueden utilizar otros grupos.
6.3 Explique que se entiende por inactivación de enzimas.
Las enzimas se pueden inactivar (desnaturalizar) principalmente por
envenenamiento, contaminación microbial, sedimentación y desnaturalización
química. Se utiliza este proceso para evitar que determinadas enzimas
COMP. PROD. AGROINDUSTRIALES (TA 341) 14

UNSCH – FIQM INGENIERÍA
AGROINDUSTRIAL
cumplan distintas funciones perjudiciales para un determinado proceso, o por
que han cumplido con su trabajo y deben de separarse o incluso conservarse.
6.4 Investigue cuál es el mecanismo general del pardeamiento
enzimático, indique las reacciones químicas.
Se denomina pardeamiento enzimático la transformación, enzimática en sus primeras
etapas de compuestos fenólicos en polímeros coloreados, frecuentemente pardos o
negros. Las fases de su transformación son los siguientes:
VI. REFERENCIAS BIBLIOGRAFICAS
Alicia Hernandez, Et al, “Microbiología Industrial”, Editorial EUNED, pp.
183-184.
Gonzalo Sergio Opazo Quesney, “Caracterización Histológica y
Bioquímica de desórdenes fisiológicos en Paltas (persea americana mill.)
cv. hass en Almacenaje Refrigerado, en dos Estados de Madurez.”
Universidad Católica de Valparaíso Facultad de Agronomía - Taller de
Licenciatura, QUILLOTA, CHILE 2000, página 18.
Cheftel, 2000. Introducción a la bioquímica y tecnología de los alimentos.
Vol 1. Editorial Acribia. Páginas 309-316
COMP. PROD. AGROINDUSTRIALES (TA 341) 15