TEMA 10: REGULACIÓN DE LA ACTIVIDAD ENZIMÁTICA Las enzimas llevan a cabo una serie de reacciones...
-
Upload
carmelo-roque -
Category
Documents
-
view
116 -
download
5
Transcript of TEMA 10: REGULACIÓN DE LA ACTIVIDAD ENZIMÁTICA Las enzimas llevan a cabo una serie de reacciones...

TEMA 10: REGULACIÓN DE LA ACTIVIDAD ENZIMÁTICA
Las enzimas llevan a cabo una serie de reacciones secuenciales que constituyen las rutas metabólicas
A B C Y Z
Dichas rutas están perfectamente coordinadas entre sí y cada una está regulada de forma muy precisa.
La velocidad de cada ruta está controlada para que refleje las necesidades generales de la célula.
La primera enzima de la ruta suele ser limitante de la velocidad (“enzima regulador”)

MECANISMOS DE REGULACIÓN ENZIMÁTICA
1. Control a nivel de sustrato
2. Inhibición reversible por productos
(retroalimentación)
3. Activación/inhibición alostérica (nivel celular)
4. Modificación covalente (supracelular):• Reversible: fosforilación, metilación,
acetilación, ADP-ribosilación, etc.
• Irreversible: activación proteolítica

1.- 1.- CONTROL A NIVEL DE SUSTRATOCONTROL A NIVEL DE SUSTRATO
Mediante interacción de los sustratos y productos de cada Mediante interacción de los sustratos y productos de cada reacción con la enzimareacción con la enzima
hexoquinasahexoquinasaGlucosa + ATP -------> Glucosa-6-fosfato + ADPGlucosa + ATP -------> Glucosa-6-fosfato + ADP
El propio producto de la reacción puede El propio producto de la reacción puede inhibir inhibir competitivamentecompetitivamente a la enzima a la enzima
_

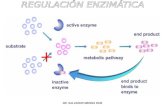
2.- CONTROL POR RETROALIMENTACIÓN 2.- CONTROL POR RETROALIMENTACIÓN (Negativa) (Negativa)
Un aumento de concentración del producto final de una Un aumento de concentración del producto final de una ruta metabólica inhibe una de las primeras reacciones de ruta metabólica inhibe una de las primeras reacciones de la ruta (generalmente la primera)la ruta (generalmente la primera)
A ---> B ---> C ---> D ---> EA ---> B ---> C ---> D ---> E
E actúa como inhibidor del primer enzimaE actúa como inhibidor del primer enzima..
Ello impide:Ello impide:• La utilización innecesaria del primer sustratoLa utilización innecesaria del primer sustrato• La acumulación del producto finalLa acumulación del producto final• Se evita la acumulación de intermediosSe evita la acumulación de intermedios
(al ser la mayoría R. Reversibles)(al ser la mayoría R. Reversibles)
_

RUTAS METABÓLICAS CONTROLADAS POR RETROALIMENTACIÓN
Glicolisis Fosfofructokinasa ATP
Neoglucogénesis FBP fosfatasa AMP
Bios. Ács. Grasos AcetilCoA carboxilasa AcilCoA
Bios. Colesterol HMGCoA reductasa Colesterol
Bios. Purinas PRPP sintetasa AMP,GMP,IMP
RUTA ENZIMA INHIBIDOR

- - Presentan una Presentan una cinética sigmoidalcinética sigmoidal, indicativa de efectos , indicativa de efectos cooperativos en la unión del sustrato.cooperativos en la unión del sustrato.
- - Su actividad está regulada por otras moléculas Su actividad está regulada por otras moléculas efectoras.efectoras.
- - Pueden Pueden mantener las concentraciones de sus sustratosmantener las concentraciones de sus sustratos en valores bastante constantes:en valores bastante constantes:
* Existe una concentración crítica de sustrato * Existe una concentración crítica de sustrato ([S]c([S]c) )
por debajo de la cuál la enzima es prácticamente inactivapor debajo de la cuál la enzima es prácticamente inactiva
* Un pequeño aumento de la concentración de * Un pequeño aumento de la concentración de
sustrato, por encima de la ([S]c, da lugar a un notable sustrato, por encima de la ([S]c, da lugar a un notable
aumento de la actividad enzimáticaaumento de la actividad enzimática
- - Son proteínas con Son proteínas con múltiples subunidadesmúltiples subunidades (múltiples (múltiples centros activos y catalíticos)centros activos y catalíticos)
3.- ENZIMAS ALOSTÉRICAS3.- ENZIMAS ALOSTÉRICAS

ENZIMAS ALOSTÉRICASENZIMAS ALOSTÉRICAS
“Bioquímica” Mathews, van Holde y Ahern. Addison Wesley 2002
Enzimaineficaz
Enzimamuyeficiente
ENZIMAS HOMOTRÓPICAS: El sitio de unión es a la vez el sitio activo y el sitio regulador. El sustrato puede funcionar como modulador.
ENZIMAS HETEROTRÓPICAS: El modulador es un metabolito diferente del sustrato. El sitio regulador es distinto del sitio regulador.

“Bioquímica” Mathews, van Holde y Ahern. Addison Wesley 2002
+
-
La unión de inhibidores o activadores alostéricos no afecta a la Vmax, per si altera la Km

http://www.upo.es/depa/webdex/biocel/Tecnicas/documentos/ENZYMAS-definitivo-.ppt#477,54,Diapositiva 54

http://www.upo.es/depa/webdex/biocel/Tecnicas/documentos/ENZYMAS-definitivo-.ppt#478,55,Diapositiva 55

REGULACIÓN DE LA ASPARTATO CARBAMOILTRANSFERASAREGULACIÓN DE LA ASPARTATO CARBAMOILTRANSFERASA(Regula la síntesis de pirimidinas)(Regula la síntesis de pirimidinas)
“Bioquímica” Mathews, van Holde y Ahern. Addison Wesley 2002


4.- MODIFICACIONES COVALENTESExisten enzimas que están inactivas hasta que se activan
por unión covalente con otras moléculas y viceversa.ADP-ribosilación- metilación, acetilaciónAlgunas modificaciones son reversibles y otras no.
OH
H
OH
OH
H
HH
CH2OH
OHO
OH
H
OH
OH
H
HH
CH2OH
O
OH
H
OH
OH
H
HH
CH2OH
O ....
OH
H
OH
OH
H
HH
CH2OH
HO O P
O
O-
O-
OH
H
OH
OH
H
HH
CH2OH
OOH
OH
H
OH
OH
H
HH
CH2OH
O ....
Pi
EJEMPLO: Glucógeno fosforilasaLibera glucosa a partir de glucógeno
A. FOSFORILACIÓN/DESFOSFORILACIÓN (serina, treonina, tirosina e histidina)

Fosforilasa fosfatasa
Fosforilasa quinasa
Fosforilasa b(menos activa)
Fosforilasa a(más activa)
Cadena lateralde Ser14
Cadena lateralde Ser14

Suele haber fenómenos de modificación covalente de
enzimas en la respuesta celular a diferentes señales:
1. Neurotransmisores
2. Hormonas
3. Factores de crecimiento
4. Estímulos morfogenéticos y de
diferenciación
5. Muerte celular programada (apoptosis)
6. Estímulos antigénicos
7. Luz y otros agentes físico-químicos

B. ACTIVACIÓN POR RUPTURA PROTEOLÍTICA
EJEMPLO: Proteasas pancreáticas (tripsina, quimotripsina, carboxipeptidasa)
Se sintetizan en el páncreas de forma inactiva denominada zimógeno (mayores que la enzima activa) para evitar que digieran el tejido pancreático.
En el intestino se activan por ruptura protelítica y finalmente son degradadas

ACTIVACIÓN DE ZIMÓGENOS POR PROTEOLISIS
INHIBIDOR
ZIMÓGENOS PROTEASAS PROTEASAS
“Bioquímica” Mathews, van Holde y Ahern. Addison Wesley 2002
Autoactivación

PROCESO EN CASCADA DE LA COAGULACIÓN DE LA
SANGRE
“Bioquímica” Mathews, van Holde y Ahern. Addison Wesley 2002

ISOENZIMAS: Son formas diferentes (pero relacionadas) de una enzima que catalizan la misma
reacción. A menudo difieren en unas pocas sustituciones de aminoácidos, afinidad por el sustrato,
Vmáx y/o propiedades reguladoras.
COMPLEJOS MULTIENZIMÁTICOS: Son asociaciones de enzimas.
Corazón Riñón Hematíe Cerebro Leucocito Músculo Hígado