TEMA 5 PROTEÍNAS. GRUPO CARBOXILO GRUPO AMINO Fórmula general de un aminoácido Biomoléculas...
-
Upload
hermenegildo-matute -
Category
Documents
-
view
20 -
download
2
Transcript of TEMA 5 PROTEÍNAS. GRUPO CARBOXILO GRUPO AMINO Fórmula general de un aminoácido Biomoléculas...

TEMA 5
PROTEÍNAS

PROTEÍNAS
GRUPO CARBOXILO
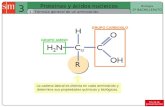
GRUPO AMINOFórmula general de un
aminoácido
Biomoléculas formadas por C, H, N, y O. Llevan pequeñas cantidades de P y S
Son macromoléculas enormemente diversas.
Su monómero es una molécula sencilla llamada AMINOÁCIDO.
La cadena lateral es distinta en cada aminoácido y determina sus propiedades químicas y biológicas
CARBONO ASIMÉTRICO



PROPIEDADES DE LOS AMINOÁCIDOS
ACTIVIDAD ÓPTICA
CARÁCTER ANFÓTERO





CARÁCTER ANFÓTERO DE LOS AMINOÁCIDOS. EFECTO TAMPÓN

PUNTOS ISOELÉCTRICOS DE LOS AMINOACIDOS
Ácido aspártico 2,98 Glicina 5,97 Prolina 6,63
Ácido glutámico 3,22 Glutamina 5,70 Serina 5,68
Alanina 6,02 Histidina 7,59 Tirosina 5,67
Arginina 10,76 Isoleucina 6,02 Treonina 5,60
Asparagina 5,41 Leucina 5,98 Triptófano 5,88
Cisteína 5,02 Lisina 9,74 Valina 5,97
Fenilalanina 5,48 Metionina 5,06





AMINOÁCIDOS ÁCIDOS

AMINOÁCIDOS BÁSICOS

AMINOÁCIDOS NEUTROS APOLARES

AMINOÁCIDOS NEUTROS POLARES





Formación de un enlace peptídico
Grupo Amino - terminal
Grupo Carboxilo -terminal
Plano del enlace peptídico
Reaccionan el grupo carboxilo de un aminoácido y el amino de otro Enlace peptídico

Enlace peptídico. Roolpi..swf





• .













ESTRUCTURA TERCIARIA DE LAS PROTEÍNAS
Estructura filamentosa Estructura globular









protein_structure[2].swf



PROPIEDADES DE LAS PROTEÍNAS
Especificidad
Solubilidad
Desnaturalización
Regulación del pH

Desnaturalización y renaturalización de una proteína
La desnaturalización es la pérdida de las estructuras secundaria, terciaria y cuaternaria.
Puede estar provocada por cambios de pH, de temperatura o por sustancias desnaturalizantes.
En algunos casos la desnaturalización puede ser reversible.
Desnaturalización
Renaturalización
PROTEÍNA NATIVA PROTEÍNA DESNATURALIZADA

protein[1].swf


CLASIFICACIÓN DE LAS PROTEÍNAS
SEGÚN SU ESTRUCTURA TERCIARIAProteínas globularesProteínas filamentosas.
SEGÚN SU COMPOSICIÓN QUÍMICAHoloproteínasHeteroproteínas (cadena peptídica + grupo prostético)
GlucoproteínasLipoproteínas Cromoproteínas
SEGÚN SU FUNCIÓN

Enzimática
Estructural
Transporte
Hormonal
Defensiva
Movimiento
Regulación del pH
Reconocimientocelular
Reserva
FUNCIONES
DE LAS
PROTEÍNAS


COMPOSICION ALMIDON, GRASA Y PROTEINA.swf

Estructura primaria de las proteínas
• Todas las proteínas la tienen.
• Indica los aminoácidos que la forman y el orden en el que están colocados.
• Es diferente incluso en la misma proteína de especies diferentes.
• Todas las proteínas tienen una secuencia de AA exclusiva.

Estructura secundaria de las proteínas: -hélice • La cadena se va enrollando en espiral.
• Los enlaces de hidrógeno intracatenarios mantienen la estructura.
Estructura secundaria de las proteínas: hoja plegada
Los enlaces de hidrógeno intercatenarios mantienen unidas las cadenas.

Estructura terciaria de las proteínasSe establece sobre la estructura secundaria, por plegamientos de la misma.
La estructura se estabiliza por uniones entre radicales de aminoácidos alejados unos de otros.
• Enlaces de hidrógeno.• Atracciones electrostáticas.• Atracciones hidrofóbicas.• Puentes disulfuro.• Fuerzas de Van der Waals
Codos en los que la estructura secundaria no existe
Fragmentos de α-hélice
Los codos de estos plegamientos se producen en zonas en las que la estructura secundaria está debilitada o no existe.
Enlaces que mantienen la
estructura

Estructura cuaternaria de las proteínas
Proteínas formadas por varias cadenas peptídicas unidas por
cadenas que forman la estructura cuaternaria


Propiedades ácido-básicas de los aminoácidos
En una disolución acuosa (pH neutro) los aminoácidos forman iones dipolares.
Un ion dipolar se puede comportar como ácido o como base según el pH de la disolución.
Las sustancias que poseen esta propiedad se denominan anfóteras.
EN UN MEDIO BÁSICO
El aminoácido se comporta como una base. El aminoácido se comporta como un ácido.
EN UN MEDIO ÁCIDO









Estructuras proteicas
Una proteína es un polipéptido con una disposición espacial tridimensional determinada y una función característica .
la secuencia de AA que forman la proteína,
• El número de polipéptidos diferentes que pueden formarse es: 20n
Número de aminoácidos de la cadena
Para una cadena de 100 aminoácidos, el número de las diferentes cadenas posibles sería:
1267650600228229401496703205376 ·10100
Esta disposición
es consecuencia dede los dobleces que establecen los enlaces no peptídicos
de los enlaces, tanto débiles como fuertes que se establecen como consecuencia de esta disposición espacial

Clasificación de las proteínas según su estructura terciaria
PROTEÍNAS FIBROSAS PROTEÍNAS GLOBULARES
• Generalmente, los polipéptidos que las forman se encuentran dispuestos a lo largo de una sola dimensión.
• Son proteínas insolubles en agua.
• Tienen funciones estructurales o protectoras.
COLÁGENO
QUERATINAS
FIBRINA
Se encuentra en tejido conjuntivo, piel, cartílago, hueso, tendones y córnea.
Forman los cuernos, uñas, pelo y lana.
Interviene en la coagulación sanguínea.
• Más complejas que las fibrosas.
• Plegadas en forma más o menos esférica.
GLOBULINAS
ALBÚMINAS
HISTONAS
Reserva de aminoácidos.
Diversas funciones, entre ellas las inmunoglobulinas que forman los anticuerpos.
Se asocian al ADN permitiendo su empaquetamiento.

Diversidad funcional de las proteínas
Debido a la gran diversidad estructural, las proteínas pueden tener funciones diversas.
FUNCIÓN EJEMPLO
Ovoalbúmina, caseína
Hemoglobina,
Actina, miosina, flagelina ...
Trombina, fibrinógeno, inmunoglobulinas...
Insulina, glucagón, somatotropina...
Histonas, queratina, colágeno, elastina...
Catalasa, ribonucleasa...
DE RESERVA
DE TRANSPORTE
MOTORA
PROTECTORA O DEFENSIVA
HORMONAL
ESTRUCTURAL
ENZIMÁTICA




Aminoácidos hidrófobos
Alanina (Ala) Valina (Val) Leucina (Leu) Isoleucina (Iso)
Metionina (Met) Fenilalanina (Fen) Triptófano (Trp)

Serina (Ser)
Aminoácidos polares hidrófilos
Glicocola (Gli)
Glutamina (Gln)
Prolina (Prl)Treonina (Tr)
Asparagina (Asn)
Tirosina (Tir)
Cisteína (Cis)

AMINOÁCIDOS ÁCIDOS
(Carga negativa)
Aminoácidos ácidos y básicos
AMINOÁCIDOS BÁSICOS(carga positiva)
Lisina (Lis)
Arginina (Arg)
Histidina (His)
Ácido aspártico (Asp)
Ácido glutámico (Glu)

HETEROPROTEÍNA GRUPO PROSTÉTICO EJEMPLO
Glucoproteína Glúcido fibrinógeno
Clasificación de las proteínas: heteroproteínas
En su composición tienen una proteína (grupo proteico) y una parte no proteica (grupo prostético).
Cromoproteína Pigmento
Porfirínicas Grupo hemo (hemoproteínas) hemoglobina
No porfirínicas Cobre, Hierro o retinal rodopsina
Nucleoproteína Ácidos nucleicos cromatina
Fosfoproteína Ácido fosfórico caseína
Lipoproteína LípidoLipoproteínas de la sangre