Electroforesis en Gel de Poliacrilamida Con SDS
-
Upload
maria-jesus-osorio -
Category
Documents
-
view
176 -
download
0
description
Transcript of Electroforesis en Gel de Poliacrilamida Con SDS
-
1
Electroforesis en gel de poliacrilamida con Dodecil sulfato de sodio (SDS):
Mtodo efectivo para la aproximacin del peso molecular de protenas
alimentarias
Claudio Toms Barraza Mandujanoa, Mara Jess Osorio Alfaroa
a Estudiante de Ingeniera en Alimentos, Facultad de Ciencias Qumicas y Farmacuticas, Universidad de
Chile, Calle Sergio Livingstone Pohlhammer 1007 (ex Olivos), Independencia - Av. Vicua Mackenna 20,
Santiago, Chile.
Resumen
La electroforesis en gel de poliacrilamida con SDS, en presencia de un agente reductor como 2-mercapto etanol, es un
mtodo utilizado para la purificacin y caracterizacin de protenas. Este mtodo se basa en la diferencia de migracin
de las protenas en un gel, debido a la carga negativa que stas adquieren con el SDS y a la presencia de un campo
elctrico en la cmara electrofortica: Las protenas de mayor peso molecular aparente, es decir, mayor tamao,
migrarn ms lento, puesto que, les ser ms difcil atravesar el gel. Para este estudio, el uso de la electroforesis
permiti de forma exitosa la obtencin de los pesos moleculares aproximados para las distintas muestras de protenas
alimentarias: protenas de leche, protenas de soya, protenas de zapallo, casenas, mioglobina y ovoalbmina.
Considerando la posibilidad de que las muestras sufran aglomeraciones (formacin de dmeros, trmeros, etc) y
degradacin, se obtuvieron valores de pesos moleculares acorde a la literatura, y otros, explicables bajo el principio de la
degradacin o aglomeracin de las protenas.
Palabras claves: electroforesis, poliacrilamida, SDS, 2-mercapto etanol, zapallo, leche, soya, casena, mioglobina,
ovoalbmina, peso molecular.
1. Introduccin
La electroforesis es un mtodo analtico til para
la separacin y caracterizacin de protenas. Este
mtodo, se basa en el desplazamiento de las
protenas en un campo elctrico, es por esta
razn, que las protenas deben adquirir carga
antes de someterse a este proceso, la cual es
otorgada por el detergente Dodecil sulfato de
sodio (SDS), el cual se une aproximadamente
cada dos residuos de aminocidos a la protena,
por lo mismo, se puede decir que la carga de la
protena, es proporcional a su masa. En general,
la electroforesis de protenas se realiza en geles
de poliacrilamida, los cuales retrasan el
desplazamiento de stas segn su masa, pero
tambin segn su forma. El SDS, se encarga de
otorgar carga neta negativa a las protenas y
altera su conformacin nativa, permitiendo que
todas las protenas presenten una forma similar
(Nelson y Cox, 2005).
La utilizacin de 2-mercapto etanol, provoca la
reduccin de los puentes disulfuro presentes en la
estructura terciaria de algunas protenas
(Maldonado, 2013).
Al aplicar una diferencia de potencial, las
protenas que presentan carga neta negativa,
migrarn por el gel, con direccin al nodo. Como
la relacin carga/masa ser aproximadamente
igual para todas las protenas y su forma no ser
un interferente, stas migrarn segn su tamao,
el cual se ver afectado principalmente por su
peso molecular. A mayor peso molecular
aparente, ms tiempo demorar la protena en
recorrer el gel y llegar al nodo, debido a la
-
2
dificultad que tendr al atravesar la malla del gel
de poliacrilamida (Maldonado, 2013).
Para la determinacin del peso molecular de
protenas presentes en muestras problema, se
debe utilizar una curva de calibracin, en la cual
se presente el logaritmo del peso molecular
(log(PM)) de protenas patrn vs su movilidad
electrofortica relativa1 (Rf); Posteriormente, al
realizar la electroforesis con SDS, se podr medir
la movilidad electrofortica relativa de las
protenas desconocidas e interpolar el valor del
logaritmo de su peso molecular (Nelson y Cox,
2005).
El objetivo de este estudio, fue demostrar que la
electroforesis en gel de poliacrilamida, con Dodecil
Sulfato de Sodio, es un mtodo efectivo para
determinar el peso molecular de distintas
protenas alimentarias (Maldonado, 2013).
2. Materiales y Mtodos
2.1 Materiales
2.1.1 Preparacin, corrida y carga del gel:
Agua destilada, Tris-HCl (pH 6.8), Tris-Base (pH
8.8), acrilamida, bisacrilamida, Am persulfato,
TEMED, SDS, amortiguador de corrida (Glicina
192 mM, Tris-Base 25 mM y 0,1% SDS), vidrios,
vaso de precipitado, agua saturada en butanol y
peineta.
2.1.2 Preparacin de las muestras proteicas:
Buffer de carga (Tris-HCl 100 mM, SDS 8%, azul
de bromo fenol, glicerol 40% y 2-Mercaptoetanol
20%), micropipeta y fuente de poder.
Las muestras proteicas analizadas fueron:
protena de zapallo, de soya, de leche, casenas,
ovoalbmina y mioglobina.
1 Distancia que recorre la protena desde el inicio del gel separador, hasta el centro de cada banda observada, dividido en la distancia que ha migrado el in lder.
2.1.3 Tincin de las protenas separadas en el gel:
Agua destilada, recipiente plstico, solucin
teidora (metanol, agua, actico 5:5:2 y 0,1% azul
coumassie R-250), solucin desteidora (25%
etanol, 10% cido actico glacial) y bao de agua
a 50 C.
2.2 Mtodos
2.2.1 Preparacin del gel:
Los geles fueron facilitados por el docente del
trabajo prctico, el cual mont los vidrios y sobre
estos, agreg la mezcla que se detalla en la tabla
1; Posteriormente, coloc una mezcla de agua
saturada en butanol sobre la mezcla del gel. Se
mantuvo a temperatura ambiente hasta observar
la gelificacin y luego se retir el agua saturada en
butanol, lavando con agua destilada.
Tabla 1: Preparacin del gel de poliacrilamida.
10% Separador (mL)
5% Concentrador (mL)
Agua destilada (mL) 3.85 2.100 0,5 M Tris-HCl (pH 6.8) - 0.4% SDS (mL)
----- 0.380
1.5 M Tris-Base (pH 8.8) - 0.4% SDS (mL)
2.60 ----
30% Acrylamide -0.8% Bis (mL)
3.34 0.500
10% Am Persulfate (L)
0.10 0.030
TEMED (L) 0.01 0.003 SDS 10% 0.10 0.030
2.2.2 Corrida y carga del gel:
El gel se mont en la cmara electrofortica, a
continuacin se aadi solucin de amortiguador
de corrida hasta llenar la cmara.
Las muestras proteicas fueron entregadas listas
de parte del docente, esto quiere decir, los
extractos proteicos se mezclaron en la proporcin,
1 parte de buffer de carga (Tris-HCl (pH 6.8) 100
mM, SDS 8%, azul de bromo fenol, glicerol 40% y
2-Mercaptoetanol 20%) con 3 partes de muestra;
Luego las muestras se hirvieron por 5 minutos.
-
3
El primer bolsillo del gel se carg con un estndar
de peso molecular y las muestras fueron cargadas
en los bolsillos del gel con micropipeta, en el
orden: protenas de leche, protenas de soya,
casenas, protenas de zapallo, mioglobina y
ovoalbmina. La cmara fue tapada y conectada a
la fuente de poder a 200 V, cuidando mantener
constante este voltaje. El tiempo de corrida, fue de
59 minutos y comprendi desde que se conect la
cmara a la fuente de poder, hasta que el frente
de corrida alcanz el final del gel.
2.2.3 Tincin de las protenas separadas en el gel:
Luego de terminar la corrida, los vidrios fueron
desmontados y se lav el gel con agua destilada.
Posterior a esto, en un recipiente plstico se situ
el gel junto a solucin teidora y se llev a bao
de agua 50 C por 30 minutos para acelerar el
proceso; Transcurridos los 30 minutos, se retir la
solucin teidora y se aadi solucin desteidora
al gel, en la cual se dej reposando por 6 das.
Finalmente, el gel se retir de la solucin, y fue
puesto en una mica, para poder medir
posteriormente la migracin de las protenas.
2.2.4 Determinacin de los Rf y de la masa
molecular aparente:
Utilizando una regla, se midi la distancia del
inicio del frente de corrida hasta el centro de cada
banda observada, esto tambin se le realiz al
estndar de peso molecular conocido con el cual
se realiz una curva de calibracin, y, mediante
esta, se pudo encontrar las masas moleculares
aparentes de cada banda.
3. Resultados
3. 1 Corrida del gel
Los resultados de la corrida del gel en la
electroforesis se muestran en la Figura 1. Con los
Rf calculados a partir del gel y los pesos
moleculares de las muestras patrn, se construyo
la tabla 2. Adems, se realiz una grafica con los
datos de los pesos moleculares en funcin del Rf
en la figura 2 y 3.
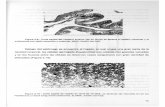
Figura 1: Electroforesis con SDS, donde P es la corrida de los
patrones y M son las distintas muestras problema, M1: Leche,
M2: Soya, M3: Casenas, M4: Zapallo, M5: Mioglobina y M6:
Ovoalbmina.
Tabla 2: Datos experimentales de los 10 patrones utilizados
(Peso molecular en KDa y migracin relativa Rf). FM:
Migracin del in lder.
Patrn Migracin cm Rf PM kDa Log(PM)
P1 0,2 0,053 170 2,230
P2 0,5 0,132 130 2,114
P3 0,8 0,211 100 2,000
P4 1 0,263 70 1,845
P5 1,3 0,342 55 1,740
P6 1,6 0,421 40 1,602
P7 2,2 0,579 35 1,544
P8 2,5 0,658 25 1,398
P9 3,3 0,868 15 1,176
P10 3,7 0,974 10 1,000
FM 3,8
Figura 2: Grfico de peso molecular de los patrones vs su
migracin relativa (Rf).
0
50
100
150
200
0 0,5 1 1,5
PM
kD
a
Rf
PM vs Rf
-
4
Figura 3: Representacin lineal de los datos expuestos en la
figura 2. Logaritmo del peso molecular de los patrones vs su
migracin relativa (Rf).
3.2 Determinacin de los Rf y de la masa
molecular aparente
Mediante la curva de calibracin hecha con la
corrida de los patrones y los Rf obtenidos para
cada muestra, se obtuvieron las distintas masas
moleculares aparentes, resumidas en la tabla 3.
Tabla 3. Pesos moleculares aparentes obtenidos por regresin lineal de los patrones y los Rf de cada muestra tras la electroforesis.
Muestra Migracin cm Rf PM kD LOG(PM)
Leche
L1 0,3 0,0769 138,026 2,139
L2 0,9 0,2307 87,919 1,944
L3 1,1 0,2820 75,647 1,878
L4 1,3 0,3333 65,087 1,813
L5 1,5 0,3846 56,002 1,748
L6 2,3 0,5897 30,692 1,487
L7 2,8 0,7179 21,0769 1,323
L8 3,4 0,8717 13,425 1,127
L9 3,7 0,9487 10,715 1,029
FM 3,9
Soya
S1 0,8 0,2105 93,294 1,969
S2 1 0,2631 79,955 1,902
S3 1,1 0,2894 74,018 1,869
S4 1,3 0,3421 63,435 1,802
S5 1,45 0,3815 56,503 1,752
S6 1,6 0,4210 50,328 1,701
S7 2,2 0,5789 31,679 1,500
S8 2,4 0,6315 27,150 1,433
S9 2,6 0,6842 23,268 1,366
y = -1,2732x + 2,2379 R = 0,9811
0
1
2
3
0 0,5 1 1,5
Log
(PM
)
Rf
Log PM vs Rf
-
5
S10 3,1 0,8157 15,821 1,199
FM 3,8
Caseina
C1 1,2 0,3076 70,169 1,846
C2 1,4 0,3589 60,374 1,780
C3 2,2 0,5641 33,089 1,519
C4 2,6 0,6666 24,496 1,389
C5 3,5 0,8974 12,453 1,095
FM 3,9
Zapallo
Z1 1,25 0,3205 67,580 1,829
Z2 1,35 0,3461 62,686 1,797
Z3 2,05 0,5256 37,038 1,568
Z4 3 0,7692 18,134 1,258
FM 3,9
Mioglobina
M1 1,2 0,3076 70,169 1,846
M2 1,3 0,3333 65,087 1,813
M3 2,05 0,5256 37,038 1,568
M4 2,5 0,6410 26,408 1,421
M5 3,6 0,9230 11,551 1,062
M6 3,9 1 9,219 0,964
FM 3,9
Ovoalbumina
O1 0,1 0,0270 159,767 2,203
O2 0,9 0,2432 84,762 1,928
O3 1,8 0,4864 41,543 1,618
O4 2,05 0,5540 34,078 1,532
O5 2,3 0,6216 27,954 1,446
O6 2,5 0,6756 23,857 1,377
O7 2,7 0,7297 20,361 1,308
O8 3,5 0,9459 10,802 1,033
O9 3,7 1 9,219 0,964
FM 3,7
Mioglobina repetida
M11 1,2 0,3428 63,295 1,801
M12 1,3 0,3714 58,209 1,764
M13 1,5 0,4285 49,231 1,692
M14 1,9 0,5428 35,215 1,546
M15 2,3 0,6571 25,189 1,401
M16 3,2 0,9142 11,853 1,073
M17 3,5 1 9,219 0,964
FM 3,5
-
6
4. Discusin y Conclusin
La leche esta principalmente constituida de
protenas como las casenas (s1, s2, y k), -
lactoalbminas y -lactoglobulinas, con pesos
moleculares de 23, 25, 23, 19, 14,2 y 18,4 kD
respectivamente (Swaisgood, 1992). En la
electroforesis, se obtuvieron alrededor de 5
bandas intensas, con 4 de ellas ntidas. La
correspondiente a los 21 KDa, fue la banda ms
difusa y cuyo peso molecular podra ser incluida
en la familia de la casenas, pero no podramos
afirmar a qu tipo de casena corresponde, ya que
las bandas de este tipo de protena van desde 19
a 25 KDa y nuestra medicin no es del todo
optima, as, al afirmar a que tipo de casena
corresponde nuestra protena nos conducira a un
error. Por otra parte, las 4 bandas restantes fueron
ms ntidas e intensas, pero no son atribuibles a
ningn tipo de protena de la leche ya que sus
pesos moleculares fueron de 10, 13, 30 y 56 KDa
respectivamente. Las bandas de 10 y 13 KDa
pueden deberse a una degradacin por parte de
los tratamientos previos a la electroforesis que
sufren las protenas, facilitando la formacin de
pptidos de menor peso molecular o podran ser
tambin, parte de -lactoalbminas, pero como
presentan una diferencia significativa se puede
asegurar. Los 30 y 56 KDa registrados pueden
deberse a la formacin de co-agregados proteicos
de de 57 y 64 KDa (Jovanovic et al., 2007) cuya
estabilizacin se produce por la formacin de
puentes disulfuro, pero esto implicara que hubo
una mala desnaturalizacin de la protena, ya sea
por la baja accin del 2-mercapto etanol o el SDS.
A partir de los valores obtenidos de los pesos
moleculares de la protena de soya, podemos
asignar en base a la literatura que, los valores de
23, 27 y 31 kD corresponden a sub unidades de
globulinas 7S o tambin llamadas Vicilinas
(Rodrguez-Oubia, 1997). Para los valores de 50
a 70 KDa podemos sealar que corresponden a
subunidades de globulinas 11s que se mantienen
unidas por interacciones no covalentes (Adachi,
Takenaka y Col., 2001). En ambos casos, no se
obtienen los valores referenciales de la protena
(400-200 KDa), ya que el medio reductor y la
utilizacin del SDS en la electroforesis,
desnaturalizan la protena y a su vez la divide por
subunidades obteniendo finalmente valores
muchos ms pequeos que el de la protena
completa.
Para la caracterizacin de las casenas, se
obtuvieron 5 bandas: A 70,2 KDa, 60,4 KDa, 33
KDa, 24,5 KDa y 12,5 KDa. Las casenas son un
grupo de protenas, que representan alrededor del
80% de las protenas de la leche. Son protenas
del tipo globulinas. Las 3 fracciones que se
presentan principalmente en estas protenas son
y k, las cuales se diferencian en su peso
molecular y en su cantidad de grupos fosfato. La
-casena pesa alrededor de 27,3 KDa, la -
casena pesa alrededor de 24,1 KDa y la k-
casena pesa alrededor de 19 KDa (Fernndez,
2005). Existen dos tipos de -casena, la s1,
que pesa alrededor de 23,6 KDa y la -s2, que
pesa alrededor de 25,3 KDa (Ribadeau-Dumas y
Grapping, 1989). Adems, existe una fraccin
minoritaria, de -casena, que pesa alrededor de
21 KDa (Alais, 1985). El valor de 12,5 KDa se
puede deber a la degradacin de cualquiera de los
tipos de casena, mientras que el valor de 24,5
KDa posiblemente corresponde a la fraccin de -
casena del extracto, o bien, a una de las dos
fracciones de la -casena; El valor de 33 KDa
observado, puede deberse a una dimerizacin o
trimerizacin de subunidades degradadas de
estas fracciones proteicas; El valor de 60,4 KDa,
puede deberse principalmente a la formacin de
algn trmero, que podra ser entre unidades de k-
casena o bien, una mezcla entre las distintas
fracciones casenicas presentes en la muestra;
Finalmente el valor de 70,2 KDa tambin puede
deberse a la formacin de algn trmero o
tetrmero de k-casena por ejemplo.
-
7
Para la caracterizacin de las protenas del
zapallo, se encontraron 4 seales luego de la
realizacin de la electroforesis. Las semillas de
zapallo son ricas en globulina, la cual tiene un
peso molecular de aproximadamente 112 KDa
(HARA, WADA, WAKABAYASHI y MATSUBARA,
1976). Se observaron bandas de peso molecular
aparente de 67,6 KDa, 62,7 KDa, 37,0 KDa y 18,1
KDa. La globulina se separa en sus dos
subunidades y en presencia del SDS, cuyos
pesos son aproximadamente 63 y 56 KDa, pero al
estar tambin en presencia de un agente reductor,
para cada subunidad se observan bandas de
polipptidos de alrededor de 36 y 22 KDa (Hara,
Wada, Wakabayashi y Matsubara, 1976). Por lo
mismo, el peso molecular aparente de 67,6 y 62,7
KDa, podran deberse a la trimerizacin de la
subunidad de 22 KDa, a la agregacin de las dos
subunidades entre ellas, o bien, a la seal (en
caso de que hubiese fallado el agente reductor) de
las dos subunidades, y . Adems, el peso
molecular aparente de 37 kDa, es esperable que
sea la subunidad de 36 KDa, mientras que el peso
molecular aparente de 18,1 KDa podra ser la
subunidad de 22 KDa, o bien, una degradacin de
la subunidad de 36 KDa.
El extracto de mioglobina, present bandas a los
63,3 KDa, 58,2 KDa, 49,2 KDa, 35,2 KDa, 25,2
KDa, 11,9 KDa y 9,2 KDa. La mioglobina de vaca
tiene un peso molecular de 17.800 y un solo grupo
hemo (Cheftel J.C. y Cheftel H., 1999). Los
valores de 11,9 y 9,2 KDa, evidencian una
degradacin de la protena, pues esta debiese
presentar bandas en valores cercanos a los 17,8
KDa. Se observ una banda a 25,2 KDa, la cual
podra deberse a la unin entre la mioglobina
(17,8 KDa) y alguno de sus pptidos degradados
de menor peso molecular, que haya presentado
un valor de alrededor de 7,3 KDa; Adems, la
banda observada a 35,2 KDa, podra deberse a la
dimerizacin de la mioglobina, puesto que mostr
un valor de alrededor del doble al esperado;
Tambin, se observ una banda a los 49,2 KDa,
que podra deberse a la formacin de un trmero
de distintas formas, pudiendo llevar dos unidades
de mioglobina y una unidad de mioglobina
degradada de alrededor de 13,6 KDa, o bien, tres
unidades de la mioglobina degradada, entre otras;
Por ltimo las bandas observadas a 58,2 y 63,3
KDa, podran atribuirse a la trimerizacin de la
unidad de mioglobina.
En la muestra de ovoalbmina la banda ms
intensa se encuentra a 41,5 KDa y condice muy
cercanamente con los 45 KDa de literatura
(Jimnez e Iregui, 2008). Las dems bandas
pueden ser producto de la degradacin de la
protena, ya que adems de la accin del medio
reductor por parte del 2-mercapto etanol y el SDS
en la preparacin de las muestras de protenas
para la electroforesis, estas son sometidas
tambin a un hervor de 5 minutos, cuyos efectos
pueden incidir directamente en la integridad de la
protena.
Cabe mencionar, dos hechos relevantes en la
realizacin de la electroforesis:
1) Las muestras de protenas de zapallo y la de
casena, no se vieron claramente, presentaban
bandas muy tenues y desteidas comparndolas
con las muestras de los dems bolsillos, esto no
es debido a diferencia en los volmenes de carga
de los bolsillos, puesto que todos fueron cargados
con 20 L. No se encuentra un motivo claro a la
existencia de esta situacin, ni en el mtodo
prctico, ni buscando en literatura.
2) La muestra de mioglobina fue situada en el
bolsillo nmero 6 y el nmero 8, puesto que una
pequea cantidad de ovoalbmina (perteneciente
al bolsillo 7), escurri al bolsillo 6 al ser introducida
en su bolsillo, pese a que no hay grandes
diferencias en los pesos moleculares obtenidos,
se utilizaron los valores del bolsillo 8, para evitar
cualquier error que pudiese causar la
contaminacin.
Los pesos moleculares obtenidos para cada
muestra, no fueron sumados para sacar el peso
molecular total de la protena, debido a que cada
-
8
muestra presentaba una variada cantidad de
protenas, lo cual impide saber el peso molecular
de cada protena en algunos casos, pues existe
degradacin, o aglomeracin de subunidades
diferentes.
En definitiva, el uso de la electroforesis permiti
de forma exitosa la obtencin de los pesos
moleculares aproximados para las distintas
muestras de protenas con SDS y 2-mercapto
etanol. Considerando la posibilidad de que las
muestras sufran aglomeraciones (formacin de
dmeros, trmeros, etc) y degradacin, cuando el
tratamiento previo a la electroforesis no sea el
correcto, y la complejidad de determinar el peso
entre protenas muy similares como las casenas,
no menoscaban el real potencial que tiene esta
herramienta para el anlisis bioqumico de los
alimentos. Por lo tanto, el uso de electroforesis
con 2-mercapto etanol y SDS ha demostrado ser
un mtodo efectivo para la determinacin
cuantitativa del peso aproximado de protenas
alimentarias.
5. Referencias Bibliogrficas
ADACHIA, M., KANAMORI, J., MASUDA, T.,
YAGASAKI, K., KITAMURA, K., MIKAMI, B. y UTSUMI,
S. 2003. Crystal structure of soybean 11S globulin:
glycinin A3B4 homohexamer. PNAS, 100, 7395-7400.
ALAIS, C. 1985. Ciencia de la leche: principios de
tcnica lechera. Sevilla, Revert.
BRAVERMAN, J.B.S. (1980). Introduccin a la
bioqumica de alimentos. 2 edicin. Mxico, El Manual
Moderno. Captulo 2 y captulo 5.
CHEFTEL, J.C. y CHEFTEL, H. 1999. Introduccin a la
bioqumica y tecnologa de los alimentos. 3 edicin.
Zaragoza, Acribia. Volumen I.
FERNNDEZ, J.M. 2005. Estructura y funcin de
protenas y pptidos: Mioglobina, hemoglobina,
miosina, casena, colgeno, gluten, lactoalbmina y
ovoalbmina. 1 edicin. Departamento de Ingeniera
Qumica. Universidad de Sevilla. Espaa.
HARA, I. WADA, K. WAKABAYASHI, S. y
MATSUBARA, H. 1976. Pumpkin (Cucurbita sp.) seed
globulin I. Purification, characterization, and subunit
structure. Oxford Journal.
JIMNEZ, A. IREGUI, C. 2008. In Vitro/In Vivo
Characterization And Evaluation Of Aeromonas
hydrophila Lipopolysacharides (LPS). Acta biol.
Colomb., Vol. 13 No. 2, 2008 147 162
NELSON, D. y COX, M. 2005. LEHNINGER: Principios
de bioqumica. 4 edicin. Barcelona. Omega.
MALDONADO, H. 2013. Gua de trabajos prcticos.
Facultad de Ciencias Qumicas y Farmacuticas.
Universidad de Chile. Chile.
RIBADEAU-DUMAS, B. y GRAPPING, R. 1989. Milk
protein analysis. Le Lait 69(5): 357-416.
RODRGUEZ-OUBIA, J. 1997. Estudio fitosociolxico
das quiroeiras de Erica erigena R. Ross da Serra da
Capelada (Galicia, NO da pennusula Ibrica). Nova
Acta Cientifica compostelana (bioloxia), 7:97-101.
SWAISGOOD, H. 1992. Symposium: genetic
perspectives on milk proteins: comparative studies and
nomenclature. Series of the Department of Food
Science, Noah Carolina State University,Raleigh
27695-7624, FSR92-27, 3054-3061.
-
9
6. Anexos
Para el clculo del peso molecular de cada banda, expuesto en la tabla 3, se utiliz regresin lineal de la
curva obtenida de las protenas estndar: Y(x) = -1,2732x + 2,2379.
Por ejemplo, para el peso molecular de L1:
Y(x) = -1,2732x + 2,2379.
Rf = x =
= 0,0769,
Luego log(PM) = Y(x) = -1,2732(0,0769) + 2,2379 = 2,139
Finalmente, PM = =138,026 KDa.