Hematoma subdural espinal y hemorragia intraventricular tras punción lumbar
Transcript of Hematoma subdural espinal y hemorragia intraventricular tras punción lumbar
61 189
CARTAS AL DIRECTOR
HEMATOMA SUBDURAL ESPINAL YHEMORRAGIA INTRAVENTRICULAR TRASPUNCIÓN LUMBAR
Sr. Director: La punción lumbar (PL) es una técnicamuy utilizada, ya sea con fines diagnósticos, o como mediopara alcanzar el canal raquídeo en anestesias neuroaxiales.La aparición simultánea de un hematoma subdural espinal(HSE) y una hemorragia intraventricular tras una PL, es unhecho excepcional y de fisiopatología no bien conocida1.Nuestro objetivo es analizar los mecanismos fisiopatológi-cos que justifican esta rara asociación.
Presentamos el caso de una mujer de 77 años con insufi-ciencia renal crónica leve y fibrilación auricular en trata-miento con acenocumarol. Durante un ingreso hospitalario,se sustituyó el acenocumarol por una heparina de bajo pesomolecular (HBPM), enoxaparina 60 mg/24h (Clexane®,Sanofi Aventis). Ante la sospecha de una hidrocefalia nor-motensiva, se realizó un test de infusión mediante una PL,obteniéndose líquido cefalorraquídeo (LCR) claro, sin rastrode sangre macroscópica.
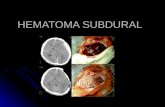
Ocho días después, acudió al servicio de urgencias, pordolor lumbar y dificultad para mover ambos miembros infe-riores. En la exploración presentaba una paraplejia y unnivel de abolición sensitiva por encima del ombligo. Laresonancia magnética (RM) raquídea demostró la existenciade una lesión D12-L3, isointensa en secuencia T1 y hetero-génea en T2 (Figura 1A). Con la sospecha de hematomasubdural, se realizó laminectomía y drenaje del hematomaque ocupaba el espacio subdural y subaracnoideo espinal.En el postoperatorio, presentó una disminución del nivel deconsciencia, demostrándose en la tomografía computarizada(TC) craneal, la aparición de una hemorragia intraventricu-lar, con sangre en ambos ventrículos laterales (Figura 1B).Dos días después, presentó una disnea súbita, y fallo car-diorrespiratorio, falleciendo con el diagnóstico probable detromboembolismo pulmonar.
Los hematomas espinales más frecuentes son los de loca-lización epidural, siendo los subdurales muy raros1,2. Entrelos secundarios, los más frecuentes son los relacionados contrastornos de la coagulación y punciones lumbares1,2, siendomás frecuentes tras anestesias epidurales (1/150.000) quetras anestesias subaracnoideas1 (1/220.000).
Nuestra paciente estaba siendo tratada con enoxaparina60 mg/24 h. Teniendo en cuenta los antecedentes de insufi-ciencia renal y que pesaba unos 50 Kg, esta dosis estaríapróxima a la anticoagulación terapéutica. Se ha discutidomucho sobre el riesgo de la PL en pacientes que recibenHBPM2. La mayoría de los autores establecen un margen deseguridad entre 4 y 12 horas2. Nuestra paciente había reci-bido la última dosis 12 horas antes de la PL.
El origen de los HSE tras una PL, podría explicarse portres mecanismos3. Uno, la punción directa de los vasos, losde mayor calibre se hallan en el espacio epidural, en el espe-sor de la duramadre y en el espacio subaracnoideo3. En elespesor de la aracnoides y en la interfase duramadre-arac-noides, sólo hay pequeños capilares y vénulas. Por tanto, esmás probable que los HSE se originen de vasos de capasdurales internas o del espacio subaracnoideo, que sangren
hacia el espacio subdural. El segundo mecanismo es la hipo-tensión de LCR. Se sabe que el espacio subdural no es unespacio anatómico real, sino que la interfase dura-aracnoi-des, está ocupada por células neuroteliales y pequeñosvasos4. La pérdida de LCR produciría un deslizamiento dela aracnoides sobre la duramadre, desgarrando los pequeñosvasos de esta interfase4. El tercer mecanismo es el “efectotienda” de la aguja, que separa la duramadre de la aracnoi-des.
Cuanto mayor sea el grosor de la aguja utilizada, mayorpérdida de LCR y mayor probabilidad de romper vasos3. Eluso de agujas biseladas incrementa la probabilidad de cor-tarlos con su filo. En las agujas punta de lápiz, este riesgoes menor, pero producen más “efecto tienda”3. El que la téc-nica sea poco traumática, como sucedió en nuestro caso, noexcluye la aparición de hematomas espinales, ya que losvasos rotos pueden estar alejados del lugar de punción (porel efecto tienda).
La aparición simultánea de una hemorragia intraventricu-lar es muy infrecuente y de fisiopatología no conocida1.Podría tener un origen intracraneal, por una crisis hiperten-siva o alguna patología vascular subyacente1. En nuestrapaciente no se había demostrado ninguna anomalía vascularen la RM cerebral. Otros autores sugieren que la sangreintraventricular procedería del canal espinal. Para que suce-da esto, son precisas tres condiciones5: el desplazamientocefálico de la sangre, favorecido al mezclarse ésta con elLCR, que la diluye y evita que se coagule, por su efectofibrinolítico. En nuestra paciente, existía sangre tanto en elespacio subdural como en el subaracnoideo. El encama-miento prolongado, habría favorecido la migración de lasangre hacia el espacio intracraneal. La segunda condiciónes la comunicación libre entre cisterna magna y el IV ven-trículo. Nuestra paciente tenía una hidrocefalia comunican-te. La tercera, la dificultad para la reabsorción del LCR enla convexidad cerebral, que empujaría la sangre hacia elinterior de los ventrículos.
Los HSE suelen producir dolor dorsal, seguido de défi-
Fig. 1. A. Resonancia magnética raquídea que muestra la existencia de unalesión D12-L3. B. Tomografía computarizada que muestra la aparición deuna hemorragia intraventricular.
61-71 - 189-199 27/3/09 15:41 Página 189
cits neurológicos. Los síntomas suelen aparecer antes de 24horas tras la PL, aunque pueden comenzar en sólo unosminutos o retrasarse varias semanas1,2. En nuestro caso laevolución fue subaguda, apareciendo el dolor lumbar a losseis días de la PL, y los síntomas neurológicos dos días des-pués.
La RM es el método diagnóstico de elección. Suelen serposteriores a la médula espinal y en cortes axiales tienenforma de media luna2. A menudo son lesiones extensas, queocupan varios segmentos espinales. Nuestro caso es típicoen cuanto a su extensión (cuatro cuerpos vertebrales) y mor-fología del coágulo (forma de semiluna en cortes axiales),pero no en la localización (anterolateral a la médula espi-nal).
El tratamiento conservador sólo está indicado en pacien-tes sin déficits neurológicos o cuando el estado general con-traindica la cirugía2. En el resto, el tratamiento de elecciónes la evacuación quirúrgica antes de que aparezcan déficitscompletos e irreversibles.
El pronóstico de los HSE depende del estado neurológi-co preoperatorio y del tiempo transcurrido desde el inicio delos síntomas2. Si aparece una hemorragia intracraneal o lahemorragia subdural se extiende al espacio subaracnoideo,como sucedió en nuestro caso, el pronóstico es peor.
En conclusión, los HSE son una complicación muy pocofrecuente de la PL. La existencia simultánea de una hemo-rragia intraventricular es un hecho excepcional, de mecanis-mos no conocidos y que ensombrece aún más el pronóstico.
P. Varela Rois*, J. González García*,M.ª T. Pérez Rodríguez***, M. J. Paseiro García*,
I. D. Carcacía Hermilla***Servicio de Neurocirugía.**Servicio de Radiología.
***Medicina Interna. Complejo Hospitalario Universitario deVigo (CHUVI).
BIBLIOGRAFÍA
1. Peiró CM, Caballer N, Errando CL, Moliner S. Hematoma espinal ycerebral postpunción lumbar diagnóstica con evolución letal. Rev EspAnestesiol Reanim. 2003;50(9):481-5.
2. Kreppel D, Antoniadis G, Seeling W. Spinal hematoma: a literaturesurvey with meta-analysis of 613 patients. Neurosurg Rev. 2003;26(1):1-49.
3. Reina MA, López A, De Andrés JA. Origen de los hematomas subdu-rales espinales. Estudio anatómico en cadáveres. Rev Esp AnestesiolReanim. 2004;51(5):240-6.
4. Reina MA, De Leon Casasola O, López A, De Andrés JA, Mora M,Fernández A. The origin of spinal subdural space: Ultrastructural fin-dings. Anesth Analg. 2002;94(4):991-5.
5. Stübgen JP. Intraventricular blood after “atraumatic” lumbar puncture:a report of two cases. Child´s Nerv Syst. 1995;11(8):492-3.
IMPLICACIONES ANESTÉSICAS EN EL MANEJODE UN PACIENTE CON HEMOFILIA A SOMETIDOA CIRUGÍA DE RESECCIÓN DE METÁSTASISHEPÁTICAS
Sr. Director: La hemofilia A o hemofilia clásica, es untrastorno de la coagulación hereditario recesivo ligado al
cromosoma X (afectación casi exclusiva de los varones),caracterizado por la ausencia o deficiencia severa del factorVIII en el plasma sanguíneo. Las primeras manifestacionesclínicas de hemorragia suelen acontecer en la infancia tem-prana, con deficiencia de factor VIII menor del 1%, o, en lahemofilia leve con 5-25% del valor normal de factor VIII,esta condición puede resultar inadvertida, incluso con ligeroalargamiento de TTPA, resultando en hemorragias única-mente durante traumatismos o intervenciones quirúrgicas1.Son frecuentes las hemorragias articulares espontáneas enestos pacientes, a diferencia de las formas adquiridas, don-de pueden observarse extravasaciones masivas subcutáneaso mucosas. Presentamos el caso de un varón con hemofiliaA leve sometido a cirugía de resección hepática bajo anes-tesia general.
Paciente varón de 72 años de edad y 68 kg de peso diag-nosticado de metástasis hepáticas de un carcinoma colorrec-tal que se iba a someter a cirugía laparoscópica de resecciónhepática. Entre sus antecedentes destacaban hipertensiónarterial y diabetes mellitus no insulinodependiente, así comoleucemia linfática crónica tipo B en tratamiento con rituxi-mab y quimioterapia CVP (ciclofosfamida, vincristina yprednisolona). También tenía hemofilia clásica A leve diag-nosticada en su juventud por aparición de hemorragias den-tales y subcutáneas incoercibles ante traumatismos. Habíasido intervenido previamente de colectomía subtotal conanastomosis iliosigmoidea término-lateral por neoplasia desigma en obstrucción. En el postoperatorio inmediato deaquella intervención precisó plasma fresco congelado, crio-precipitados y 2.500 UI de factor VIII recombinante cada 12horas durante 5 días hasta conseguir una actividad superioral 80%. Recibió posteriormente quimioterapia.
Para la resección de las metástasis presentaba Rx tórax yECG normales, mientras que el estudio preoperatorio revelóun hematocrito de 40%, 164.000 plaquetas.microL, TTPA de41 seg, TTPA-ratio de 1,59 y actividad de protrombina del100% con una concentración de factor VIII de 0,23 UI ml-1.Tras consultar con el servicio de hematología se decidió pau-tar factor VIII recombinante 2.500 UI cada 12 horas iv duran-te 3 días iniciándose una hora antes de la cirugía, así comodesmopresina 0,3 μmKg-1 y ácido tranexámico 25 mgKg-1
cada 8 horas como antifibrinolítico coadyuvante, tras la inter-vención durante 7 días. La actividad del factor VIII (estudiofarmacocinético) fue del 112,1% previamente a la cirugía.
El paciente fue premedicado con ranitidina iv. y midazo-lam oral. En quirófano se monitorizó ECG, presión arterialinvasiva, saturación arterial de oxígeno, profundidad anesté-sica (BIS), presión venosa central mediante vía central dealto flujo, gasto e índice cardiaco mínimamente invasivos.La anestesia consistió en 0,01 mg Kg-1 de atropina y 2 mgKg-1 de propofol y mantenimiento con oxígeno y aire (FiO2
0,4), sevofluorano 1-2%, atracurio y remifentanilo 0,15 µgKg-1 min-1 para mantener el BIS 40-60. La temperatura cor-poral fue mantenida entre 36-37ºC utilizando manta térmi-ca. La intervención duró 100 minutos y transcurrió sin inci-dencias. Las pérdidas sanguíneas estimadas fueron de 700ml y se repusieron 1.000 ml de gelatinas y 2.000 ml de cris-taloides. El paciente fue extubado en quirófano y trasladadoa la unidad de reanimación. En el postoperatorio no se evi-
CARTAS AL DIRECTOR
190 62
61-71 - 189-199 27/3/09 15:41 Página 190