Hiperandrogenismo en adolescente
-
Upload
yesenia-huizar -
Category
Documents
-
view
547 -
download
1
Transcript of Hiperandrogenismo en adolescente

Hiperandrogenismoen la adolescente
C. Richard, S. Jonard, D. Dewailly
La fisiopatología del hiperandrogenismo, que se manifiesta desde el punto de vista clínicosobre todo por la presencia de hirsutismo, acné y/o alteración menstrual, se debeesencialmente a la hiperproducción ovárica o suprarrenal de andrógenos. Su carácterpatológico resulta difícil de establecer en el período peripuberal debido a la existencia deinmadurez fisiológica del eje hipotálamo-hipofisario. Su etiología más frecuente es elsíndrome de ovarios polimicroquísticos (SOPMQ). Su diagnóstico en la mujer adulta sebasa en criterios precisos que requieren su adaptación al caso particular de laadolescente. La evaluación clínica de la rapidez de instalación y de la intensidad de lossignos de hiperandrogenismo así como el estudio bioquímico sistemático de iniciopermiten descartar las demás causas, particularmente los tumores ováricos ysuprarrenales, el déficit de 21-hidroxilasa, las endocrinopatías y las causas iatrogénicas.Dejando aparte el tratamiento etiológico, la actuación terapéutica consiste en laadministración de antiandrógenos, principalmente acetato de ciproterona. En caso deSOPMQ, cuando se asocian alteraciones metabólicas, la educación sanitaria respecto alas normas higienicodietéticas resulta fundamental.© 2006 Elsevier SAS. Todos los derechos reservados.
Palabras Clave: Hirsutismo; Espanomenorrea; Síndrome de ovarios polimicroquísticos;Déficit de 21-hidroxilasa; Acetato de ciproterona
Plan
¶ Introducción 1
¶ Fisiología 2
¶ Signos clínicos de hiperandrogenismo 2Hirsutismo 2Acné y seborrea 3Alopecia 3Alteraciones menstruales 3Signos de virilización 3
¶ Estudio de laboratorio 3
¶ Etiología del hiperandrogenismo en la adolescencia 3Hiperandrogenismos tumorales 3Hiperandrogenismos funcionales 4Hiperandrogenismos iatrogénicos 6Hiperandrogenismo y otras endocrinopatías 6
¶ Tratamientos 6Tratamientos etiológicos específicos 6Antiandrógenos 6Tratamientos cosméticos 7Tratamiento del acné aislado 7Caso particular del síndrome de ovarios polimicroquísticos 7
¶ Conclusión 7
■ IntroducciónLos síntomas de hiperandrogenismo, como el acné o
la seborrea, así como la irregularidad menstrual, sonfrecuentes en la adolescente. Estos síntomas suelen sertransitorios, y se deben al aumento fisiológico de losandrógenos ováricos y suprarrenales y a la falta demadurez del eje hipotálamo-hipófiso-ovárico durante losprimeros años que siguen a la menarquia. A vecespersisten, e incluso se agravan, poniendo de manifiestouna anomalía ovárica o suprarrenal, y el caso másfrecuente es el del síndrome de ovarios polimicroquísti-cos (SOPMQ).
Aunque, del mismo modo que en la mujer adulta,resulta relativamente fácil reconocer una causa grave, elabordaje del hiperandrogenismo benigno en la adoles-cente es un ejercicio a veces difícil, ya que la distinciónentre la «androgenización» fisiológica de la pubertad yel SOPMQ resulta a menudo ardua. El diagnóstico deSOPMQ no es sin embargo una urgencia, y lo funda-mental es detectar lo más precozmente posible lainsulinorresistencia y la obesidad incipiente que amenudo se asocian, con el fin de prevenir sus ulteriorescomplicaciones en relación con la fecundidad y losriesgos metabólicos y cardiovasculares.
¶ E – 802-A-36
1Ginecología-Obstetricia

■ FisiologíaEl hiperandrogenismo puede ser secundario a una
hiperproducción de andrógenos ovárica o suprarrenal.Sin embargo, su expresión clínica está condicionada porla concentración de globulina transportadora de hor-monas sexuales (SHBG), por la conversión periférica(5-a-reductasa) y por el nivel de receptores de losandrógenos. Todos estos parámetros están influidos porfactores étnicos, genéticos y personales. La unidadpilosebácea reacciona, por tanto, frente al hiperandro-genismo de forma muy variable.
La adrenarquia o pubertad suprarrenal es contempo-ránea del desarrollo y de la maduración de la zonareticulada de la corticosuprarrenal. Entre los 6 y los8 años, aparecen variaciones de la actividad de lasenzimas de la biosíntesis de los andrógenos suprarrena-les, responsables de una producción importante dedeshidroepiandrosterona (DHEA) y de su sulfato(DHEAS) [1].
Al inicio de la pubertad, aparecen picos nocturnos dehormona luteinizante (LH), que después se hacendiurnos mientras que su amplitud y frecuencia aumen-tan [2]. Además, la bioactividad de las gonadotrofinas
aumenta. En la teca y el estroma ováricos, que handesarrollado receptores para la LH, se inicia entonces labiosíntesis de andrógenos, que provoca el aumento dela su concentración plasmática. Estas modificaciones sonparalelas a las del eje hormona del crecimiento (GH)/factor de crecimiento tipo insulina-1 (IGF1), cuyahiperactividad provoca una insulinorresistencia fisioló-gica y selectiva, con aumento de la concentraciónplasmática de insulina y disminución de la producciónhepática de SHBG y de proteína transportadora delfactor de crecimiento tipo insulina-1 (IGFBP1) [3].
■ Signos clínicosde hiperandrogenismo
HirsutismoConsiste en la aparición de pelos duros y pigmentados
en territorios masculinos (cara, tórax, espalda, línea alba,huecos inguinales, caras internas y posteriores de losmuslos). Se evalúa mediante la puntuación de Ferriman yGallwey (Cuadro I), cuyo límite patológico es superior a6 (en su forma modificada de nueve ítems).
Cuadro I.Puntuación de Ferriman-Gallwey.
Labio superior 1 Algunos pelos en el borde externo
2 Pequeño bigote en el borde externo
3 Bigote que se extiende por la mitad externa
4 Bigote completo
Mentón 1 Algunos pelos diseminados
2 Pelos diseminados con zonas de concentración
3 y 4 Barba ligera o significativa
Pecho 1 Algunos pelos periareolares
2 Además algunos pelos mediales
3 Tres cuartas partes de la superficie recubiertas
4 Vello recubre todo el pecho
Parte superior de la espalda 1 Algunos pelos diseminados
2 Un poco más pero aún diseminados
3 y 4 Vellón ligero o denso que recubre completamente la mitad superior de la espalda
Mitad inferior de la espalda 1 Mechón sacro de pelo
2 Igual con extensión lateral
3 Tres cuartas partes de la superficie recubiertas
4 Vello difuso sobre toda la superficie
Mitad superior del abdomen 1 Algunos pelos mediales
2 Más numerosos y siempre mediales
3 y 4 Parte superior completamente recubierta
Mitad inferior del abdomen 1 Algunos pelos mediales
2 Raya medial de pelos (reguero)
3 Banda medial de pelos
4 Vello en forma de rombo
Brazo; muslos; piernas 1 Vello escaso que no afecta a más de la cuarta parte de la superficie del segmento dela extremidad
2 Un poco más extensa: cubrimiento incompleto
3 y 4 Cubrimiento completo leve o denso
Antebrazo 1 Cubrimiento completo de la cara posterior
2 Vello escaso
3 y 4 Vello denso
.
E – 802-A-36 ¶ Hiperandrogenismo en la adolescente
2 Ginecología-Obstetricia

Es preciso diferenciarlo de la hipertricosis, no depen-diente de andrógenos, simple exageración de la distri-bución femenina normal, con la que no comparte lascausas.
Acné y seborreaEl acné es una afectación hormonodependiente del
folículo pilosebáceo de tipo retentivo, por aumento dela producción de sebo e hiperqueratosis del conductoexcretor, y/o de tipo inflamatorio, por colonizaciónbacteriana.
Clínicamente, la forma retentiva se caracteriza porcomedones y microquistes, y la forma inflamatoria, porpápulas y pústulas. Frecuentemente, se trata de unaforma mixta que asocia ambos tipos de lesiones.
El cuadro de hiperandrogenismo es habitualmenteinflamatorio y grave, de topografía masculina (mentón,cuello, tórax) y a menudo de aparición precoz, antesincluso del desarrollo puberal.
AlopeciaExcepcional en la adolescencia, la alopecia de la
coronilla es también un signo de hiperandrogenismoque puede variar desde el aspecto ralo en la coronillahasta la existencia de calvicie con esbozo de entradasfrontales, que constituye un signo mayor de virilización.También en este caso, la alopecia aislada no es siempreel signo de un hiperandrogenismo y puede poner demanifiesto otras causas como las carencias de hierro, losproblemas psicológicos o las causas autoinmunitarias.
Alteraciones menstrualesLo más frecuente es que se trate de una espanomeno-
rrea que, no obstante, puede considerarse como fisioló-gica durante los dos años posteriores a la menarquia.Esta opinión muy clásica ha sido, sin embargo, rebatidapor algunos autores que han mostrado recientementeque la alteración del ciclo precoz en la adolescenteconstituye un poderoso factor predictivo del inicio deun SOPMQ [4].
Las demás expresiones del hiperandrogenismo son:amenorrea a menudo secundaria o, de modo más infre-cuente, metrorragias.
Signos de virilizaciónEn las etiologías tumorales, el hiperandrogenismo
puede ser de expresión más rápida y más grave consignos mayores de virilización:• apariencia masculina e hipertrofia muscular;• voz grave;• hipertrofia clitorídea y de los labios mayores.
■ Estudio de laboratorio
La toma de muestras debe efectuarse entre las 8 h ylas 10 h de la mañana, al principio de la fase folicular otras un tratamiento progestágeno breve.
Los tres principales andrógenos que es necesariodeterminar son:• testosterona (T) plasmática, reflejo de la producción
ovárica, suprarrenal o mixta;• sulfato de deshidroepiandrosterona (DHEAS), reflejo
exclusivamente suprarrenal;• 17-hidroxiprogesterona (17-OHP) plasmática, marca-
dor del déficit de 21-hidroxilasa.Estas determinaciones permiten una orientación
diagnóstica que se ilustra en la Figura 1. Las demásdeterminaciones que se consideran en función de laorientación diagnóstica son:• prolactina, que debe determinarse si existe galactorrea
o alteración del ciclo;• cortisol libre urinario (CLU), que es indispensable
cuando existe sospecha clínica de hipercorticismo.
■ Etiologíadel hiperandrogenismoen la adolescencia
Hiperandrogenismos tumoralesLos signos clínicos de hiperandrogenismo son en este
caso claros, acompañándose frecuentemente de signosde virilización; su aparición es reciente y la evoluciónrápida. Los valores de una o varias determinacionesiniciales están por encima de los umbrales de alarma.
Tumores ováricos virilizantesConstituyen una causa muy poco frecuente de hipe-
randrogenismo en la adolescencia, tratándose casisiempre de tumores benignos.
El diagnóstico se basa en la elevación considerable delos andrógenos ováricos, con una concentración detestosterona plasmática al menos tres veces por encimadel valor normal superior del laboratorio (es decir,generalmente, superior a 1,5 ng ml-1).
La ecografía mostrará una neoformación parauterinamixta ya que estos tumores tienen tendencia a necro-sarse, haciendo cohabitar zonas líquidas ecogénicas yzonas más densas.
La clasificación histológica simplificada de los tumo-res ováricos virilizantes incluye los tumores de célulasde Sertoli-Leydig, de células del hilio, de células lipídi-cas, de células granulotecales, de estroma funcional y los
“ Punto fundamental
La intensidad y la velocidad de aparición de lossignos clínicos de hiperandrogenismo sonprimordiales. Permiten diferenciar las etiologíasgraves de las benignas.
17-OHP (ng ml-1) DHA-S (mmol l-1)
> 5 2-5 < 2
Prueba de la ACTH
> 12 < 12
Déficit de 21-hidroxilasa
Testosterona (ng ml–1)
< 20 > 20
Tumor suprarrenal
Tumor ovárico
< 1,5
> 1,5
¿Oligoanovulación?
Sí No
Sí No
Ecografía: ¿OP?
SOPMQ
Idiopática
Figura 1. Árbol de decisiones. Orientación diagnóstica. OP:ovario poliquístico; SOPMQ: síndrome de ovarios polimicroquís-ticos.
Hiperandrogenismo en la adolescente ¶ E – 802-A-36
3Ginecología-Obstetricia

disgerminomas [5]. Los tumores de células del hilio, decélulas lipídicas y de estroma funcional no se desarro-llarán en este artículo ya que se trata de tumores de lamujer menopáusica o del embarazo.
Tumores de células de Sertoli-Leydig
Son los más frecuentes y constituyen el 0,5 % de lostumores ováricos [6]. La edad más frecuente de presenta-ción es entre los 20-40 años. Se trata de tumores cuyotamaño medio varía entre 5-15 cm, formados por unparénquima lleno, raramente quístico.
Tumores de células granulotecales
Clásicamente, estos tumores producen sobre todoestrógenos aunque, de modo infrecuente, pueden serandrogénicos [7]. Este fenómeno se debería a la presenciade células estromales en su interior.
Disgerminomas
Se trata del ginandroblastoma y del gonadoblastoma.Estos tumores asocian elementos del estroma y de lasestructuras germinales. Se desarrollan a partir de góna-das disgenéticas pertenecientes a pacientes con cariotipoXY o XO/XY. Son responsables de un síndrome devirilización por lo general poco acentuado en pacientesde fenotipo femenino normal o ambiguo. Se trata detumores sólidos, más o menos voluminosos, a menudobilaterales. Presentan frecuentemente numerosas calcifi-caciones intratumorales.
Tumores suprarrenalesSon muy infrecuentes, a menudo malignos, sospe-
chándose ante la presencia de signos clínicos asociadosde hipercorticismo y de valores muy elevados deDHEAS.
La ecografía abdominal es la exploración que debepracticarse en primera instancia. El escáner abdominales la exploración de elección, en ocasiones completadocon RM y gammagrafía con noryodocolesterol.
Hiperandrogenismos funcionalesSíndrome de ovarios polimicroquísticos
Tanto en la adolescente como en la mujer adulta, esla etiología más frecuente de hiperandrogenismo; sinembargo, su diagnóstico es difícil ya que los síntomaspueden confundirse con los de la androgenizaciónfisiológica del período peripuberal, que constituyen laexpresión clínica de un defecto de maduración del ejehipotálamo-hipófiso-ovárico. Durante el período peri-puberal, las alteraciones del ciclo son frecuentes y seasocian habitualmente a signos clínicos moderados dehiperandrogenismo.
Fisiopatología
Todavía se conocen mal los factores fisiopatológi-cos que predisponen al SOPMQ. Abbott et al. (2002)han postulado la hipótesis de una «reprogramación inútero», según la cual, el ovario fetal estaría programadogenéticamente para ser espontáneamente hiperandrogé-nico. El hiperandrogenismo sistémico «reprogramaría» eldesarrollo y la función posterior del tejido adiposo y delhipotálamo, lo que tendría respectivamente comoconsecuencias en la pubertad una insulinorresistenciapatológica y la hipersecreción de LH [8].
El fenómeno primitivamente responsable de la altera-ción de la función ovulatoria en el SOPMQ parece ser elexceso de síntesis de andrógenos por las células tecales,bajo la influencia de factores extraováricos y, sobre todo,intraováricos [9].
El hiperandrogenismo se encuentra también amplifi-cado por el hiperinsulinismo, que aumenta la fracciónlibre activa de los andrógenos circulantes disminu-yendo su proteína de transporte (SHBG) y los efectos dela LH sobre la síntesis esteroidea de las células tecales [10].
Dos fenómenos esenciales constituyen las alteracionesdel desarrollo folicular:• crecimiento excesivo de los folículos secundarios de
los estadios 1-5 (pequeños folículos que miden2-5 mm) [11] muy probablemente debido al efectotrófico de los andrógenos;
• inhibición de la evolución hacia la selección de unfolículo dominante que contribuye a la acumulaciónde los folículos inmaduros.
¿Cómo diagnosticar un auténtico síndromede ovarios polimicroquísticos en una adolescente?
Clásicamente, las tres manifestaciones clínicas cardi-nales del SOPMQ son:• hiperandrogenismo, del modo más frecuente mode-
rado, de instalación peripuberal, particularmente conhirsutismo de evolución lenta [12];
• alteraciones ovulatorias del tipo de oligomenorrea oamenorrea primaria o secundaria reversible conprogestágenos, por tanto «normoestrogénica» (tipo2 de la Organización Mundial de la Salud [OMS]);
• síndrome metabólico, con obesidad de tipo androide(índice de masa corporal [IMC] inferior a 25 o adipo-sidad abdominal con perímetro superior a 88 cm) y,más raramente, acantosis nigricans, signo de insuli-norresistencia grave [10].Esta asociación se encuentra con escasa frecuencia en
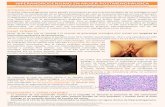
la adolescente, salvo en casos particulares. Además, eldiagnóstico es complicado debido a que la pubertadfisiológica puede asimilarse a un mini-SOPMQ, pordefinición transitorio. La presentación de un auténticoSOPMQ sólo podrá detectarse por la persistencia de lasanomalías clínicas, de laboratorio y ecográficas, más alláde un cierto tiempo (2 años para la mayoría de autores).Los exámenes de laboratorio son difíciles de interpretarpara un caso particular. La imagen ecográfica de losovarios resulta igualmente de interpretación delicada enesta edad (Fig. 2).
Argumentos clínicosPara distinguir un auténtico SOPMQ de un mini-
SOPMQ fisiológico en una adolescente, algunos elemen-tos de la anamnesis y de la exploración física puedenayudar, siendo fácil el diagnóstico en algunos casos:• persistencia de la alteración de las menstruaciones dos
años después de la menarquia;• hiperandrogenismo asociado (hirsutismo, acné grave);• contexto familiar de SOPMQ;• antecedentes personales:
C adrenarquia prematura (en algunas poblaciones) [1];C peso insuficiente al nacer, ¡o excesivo!;
• situación metabólica:C obesidad;C adiposidad central, que traduce un hiperinsuli-
nismo;C acantosis nigricans, de modo más infrecuente.Atención, sin embargo, a los diagnósticos «demasiado
fáciles» ya que algunas etiologías de hiperandrogenismopueden llevar a engaño (cf. infra).
Figura 2. Aspecto de ovarios polimicroquísticos mediante eco-grafía suprapúbica en una adolescente.
E – 802-A-36 ¶ Hiperandrogenismo en la adolescente
4 Ginecología-Obstetricia

A la inversa, el diagnóstico puede ser más difícil enlas situaciones menos claras como, por ejemplo, unbanal acné asociado a alteraciones del ciclo, pudiendoconsiderarse ambos como normales en esta edad.
Por estas dos razones, siempre es necesario un estudiocomplementario que debe ser razonable y razonado.
Pruebas complementariasLaboratorio. En las situaciones clínicas (demasiado)
evidentes, el papel del laboratorio consiste en evitar quese ignoren las causas graves de hiperandrogenismo, quepueden a veces constituir trampas diagnósticas. Resultapues obligatorio, en todos los casos, determinar la T total,la 17-OHP y, en algunos casos, el DHEAS, siguiendo elalgoritmo propuesto en la Figura 1. No hay que olvidarla verificación del CLU ante la menor sospecha clínicade hipercorticismo, así como la de la prolactina si elhiperandrogenismo se acompaña de alteración impor-tante del ciclo y/o de galactorrea, infrecuente sinembargo a esta edad. Es necesario, no obstante, tener encuenta que una hiperprolactinemia funcional, moderaday fluctuante acompaña a un SOPMQ en el 15-30% delos casos [13].
En situaciones menos claras, el laboratorio resultapoco rentable para el diagnóstico positivo del SOPMQ yla reciente conferencia de consenso de Rotterdam [14]
propone de simplificar las costumbres.Resulta poco útil buscar una elevación de la LH
plasmática basal y aún menos después de la prueba deGnRH, así como una elevación de la relación LH/FSH.
La búsqueda de un hiperandrogenismo en el labora-torio se basa en la determinación de la T total, a vecescompletada con la de la SHBG, permitiendo el cálculodel índice de T libre (ITL). Es inútil determinar algunosandrógenos (androstenodiona, deshidrotestosterona[DHT], etc.) diferentes de los que se incluyen en elestudio sistemático (cf. supra).
Resulta inútil buscar marcadores sofisticados delhiperinsulinismo y/o de la insulinorresistencia (IR),salvo en un contexto familiar de IR genética. En cam-bio, es conveniente buscar en todos los casos unaposible diabetes, excepcional no obstante a esta edad, ysobre todo anomalías lipídicas, que están lejos de serinfrecuentes en la adolescente (elevación de los triglicé-ridos, disminución del colesterol-lipoproteínas de altadensidad [HDL]). Cuando están presentes, estas anoma-lías se integran en el síndrome metabólico asociado alSOPMQ, que se constituye muy a menudo desde laadolescencia.
Diagnóstico por imagen. La ecografía es el examen dereferencia. Sin embargo, en la adolescente, lo másfrecuente es que sólo sea posible la vía suprapúbica, loque hace más difícil la obtención de los criterios diag-nósticos oficiales del SOPMQ, definidos para la víaendovaginal [15]. Estos criterios, denominados «deRotterdam», son:• aumento del volumen ovárico (volumen por ovario
superior a 10 cm3);• ecoestructura que contenga más de 12 imágenes
anecoicas (folículos) de 2-9 mm por ovario.Este último criterio es muy difícil de obtener por vía
suprapúbica: en caso de una adolescente, es preciso portanto dar preferencia al primero: un volumen porovario superior a 10 cm3. Es posible también ayudarsede criterios secundarios como la hipertrofia estromalhiperecogénica, la forma globulosa de los ovarios(relación longitud/anchura superior a 0,7) o unarelación fondo uterino/eje ovárico mayor (U/O) infe-rior a 1; sin embargo, estos criterios tienen una sensi-bilidad y/o especificidad mediocres [15] (véasefotografía).
Déficit de 21-hidroxilasa en su formade manifestación tardía («no clásica»)
El déficit de 21-hidroxilasa constituye el 95% de lasenzimopatías suprarrenales responsables de hiperandro-genismo en la adolescencia. El déficit de 11-b-hidroxilasa es muy infrecuente, y la autenticidad deldéficit de 3-b-hidroxiesteroide deshidrogenasa nunca seha demostrado.
Se trata de una enfermedad genética que se transmitede modo autosómico recesivo y que se caracteriza porun gran polimorfismo. Su frecuencia se estima en1/1.000 nacimientos. Según las poblaciones que seconsideren, constituye el 3-10% de las causas dehiperandrogenismo.
Fisiopatología
La hiperplasia congénita de las suprarrenales pordéficit de 21-hidroxilasa se debe a la afectación del genque codifica para el citocromo P450 C21.
En las formas no clásicas, lo más frecuente es que setrate de la mutación puntual V281L, frente a la cual lospacientes pueden ser homocigotos o heterocigo-tos [16]. En este último caso, el otro alelo puede serportador de una mutación más invalidante (estado dedoble heterocigosis) pero que no se expresa, ya que estáparcialmente compensada por la mutación V281L.
Estas mutaciones genéticas provocan una reduc-ción del 20-50% de la actividad enzimática de la21-hidroxilasa.
Esta alteración de la cinética enzimática es responsa-ble de la acumulación de precursores, principalmente dela progesterona (P) y de la 17-hidroxiprogesterona(17-OHP) [17].
El exceso de precursores se convierte en parte enandrógenos responsables del hiperandrogenismo supra-rrenal sin anomalía gluco o mineralcorticoide.
Esta enfermedad se expresa durante o después de lapubertad ya que en este período se operan cambios enla esteroidogénesis que favorecen su expresión.
Clínica y laboratorio
El bloqueo de 21-hidroxilasa de manifestación tardíase caracteriza por una gran diversidad de fenotiposclínicos. Los signos clínicos, cuando existen, se mani-fiestan en el período peripuberal y no poseen un carác-ter específico.
El diagnóstico de laboratorio se establece a partir devalores basales de 17-OHP superiores a 5 ng ml-1 y, en
“ Conducta que debeseguirse
Para el diagnóstico de un SOPMQ en laadolescente, es conveniente utilizar los criterios deRotterdam:• la oligoovulación o la anovulación se traducendel modo más frecuente en espanomenorrea;• el hiperandrogenismo clínico y/o bioquímico sedefine mediante hirsutismo y/o acné grave y/oelevación de la T total, a condición de considerarpara esta última un límite superior a la normalidadadaptado a la adolescente, esto es, 0,5 ng ml-1;• el aspecto de ovarios polimicroquísticos en laecografía, bastando en este caso con un volumenovárico >10 cm3.De los tres, son suficientes dos criterios [14].
Hiperandrogenismo en la adolescente ¶ E – 802-A-36
5Ginecología-Obstetricia

la prueba de la ACTH, superiores a 12 ng ml-1 (pruebaque se realiza si la 17-OHP basal está comprendida entre2-5 ng ml-1) (Fig. 1).
El aumento de la T, de la delta-4 androstenodiona (A)y del DHEAS es moderado, sin llegar a los valorestumorales, similar al que se observa en el SOPMQ.
Diagnóstico por imagen
La hiperplasia suprarrenal, aunque incons-tante, merece investigarse de forma sistemática en elestudio inicial, mediante la realización de una tomogra-fía computarizada abdominal [17]. Esta exploración deberepetirse cada 5 años, sobre todo si no se juzga útilinstaurar un tratamiento con dexametasona (cf. infra).
Hirsutismo idiopáticoCorresponde al 5-15% de las causas de hiperandroge-
nismo [18]. Su definición debe ser rigurosa: persistenciade ciclos menstruales regulares y ovulatorios, ausenciade hiperandrogenismo bioquímico y de estigma ecográ-fico de SOPMQ. En estas condiciones, el hirsutismoidiopático es relativamente infrecuente, excepto endeterminadas etnias (cuenca mediterránea). En estasituación, los andrógenos se secretan en cantidadnormal pero la actividad del receptor de los andrógenosse encuentra aumentada debido a un mayor número detripletes CAG (cf. supra).
Hiperandrogenismos iatrogénicosLas clases terapéuticas responsables de este tipo de
efectos secundarios están representadas por los esteroi-des anabolizantes, los progestágenos de síntesis deriva-dos de la nortestosterona, los anticomiciales, losanálogos de la adrenocorticotropina (ACTH) y la meto-pirona [19]. Estos tratamientos conciernen poco a laadolescente, exceptuando el valproato sódico. Esteúltimo, según Nelson et al. [20], sería capaz de reproducirlas anomalías funcionales de la teca halladas en elSOPMQ natural (cf. supra), por su interferencia con losfenómenos posgenómicos.
Hiperandrogenismo y otrasendocrinopatías
Síndrome de CushingAnte la presencia de hirsutismo, incluso moderado, y
oligoespanomenorrea, es siempre preciso buscar signosque orienten hacia un síndrome de Cushing: discretaeritrosis facial, distribución faciotroncular de la grasa,presencia de algunas estrías horizontales en el abdomen,equimosis fáciles [21].
La sospecha clínica se confirma mediante la elevacióndel cortisol libre urinario, que constituye un criteriodiagnóstico muy bueno. Una concentración superior a300 µg día-1 es casi patognomónica. Entre 60-300µg día-1, la prueba de frenado rápido (determinación delcortisol plasmático a las 8 h de la mañana, habiendoingerido la paciente 1 mg de dexametasona la víspera amedianoche) es indispensable. Una concentración quese mantenga por encima de 3 µg 100 ml-1 debe llevar ainvestigaciones en medio especializado (ciclo nictameraldel cortisol y de la ACTH, prueba de frenado «fuerte»con dexametasona, prueba de la metopirona, prueba dela hormona liberadora de corticotropina [CRF], catete-rismo de los senos petrosos inferiores), que permitanorientar las exploraciones morfológicas (tomografíacomputarizada o resonancia magnética [RM] suprarrenaly/o hipofisaria).
Las causas pueden ser ACTH-dependientes (enferme-dad de Cushing, secreción ectópica de ACTH) o ACTH-independientes (tumor o hiperplasia autónoma,primitivamente suprarrenal) [21].
Hiperprolactinemia
El exceso crónico de prolactina, independientementede su etiología, puede provocar la estimulación de lasecreción de andrógenos suprarrenales, en particular delDHEAS, y por tanto un hiperandrogenismo que, porregla general, es moderado. En la práctica se observaprincipalmente en las pacientes que presentan unprolactinoma [15].
Lo más frecuente es sin embargo que la existencia deuna hiperprolactinemia en una adolescente hiperandro-génica corresponda a un SOPMQ (cf. supra). No obs-tante, si la hiperprolactinemia persiste de forma establede un control a otro, es conveniente sospechar unaasociación SOPMQ-prolactinoma, que no es ni muchomenos infrecuente aunque sea, sin duda, casual.
Acromegalia
A menudo se cita el hirsutismo entre las manifesta-ciones cutáneas de la acromegalia [22], aunque raramenteconstituye el motivo inicial de consulta. Ningún estudioha demostrado una relación causal entre ambas enfer-medades. El exceso de GH y/o de IGF1 y el hiperinsuli-nismo debidos a la acromegalia podrían constituir enteoría causas favorecedoras de la génesis de hirsutismoy de SOPMQ. Es preciso tener presente esta posiblesituación ya que los síntomas de acromegalia son amenudo poco claros en la adolescente.
■ Tratamientos
Tratamientos etiológicos específicos
Tratamiento de los tumores ováricoso suprarrenales
El tratamiento será siempre quirúrgico mediantelaparoscopia o laparotomía. En función de los criteriosde malignidad peroperatorios y anatomopatológicos, seimpone muy a menudo un tratamiento complementariodel tratamiento quirúrgico de los tumores suprarrenales,a base de mitotano o 2-4’-diclorodifenildicloroetano(Op’DDD).
Tratamiento del déficit de 21-hidroxilasa
El recurso sistemático a la corticoterapia a largo plazose discute actualmente [23].Para algunos autores [23], sóloes necesaria en caso de hiperplasia suprarrenal consta-tada en la tomografía computarizada y/o si se desea unembarazo. En este caso, se prescriben pequeñas dosis dedexametasona en toma vespertina (del modo másfrecuente, 0,25 mg día-1). Las consecuencias clínicas delhiperandrogenismo se tratan más rápida y eficazmentemediante acetato de ciproterona, utilizado de acuerdocon el esquema habitual (cf. infra) [24].
No se considerará aquí el tratamiento antes y duranteel embarazo de las pacientes que presentan un déficit de21-hidroxilasa, pero es conveniente insistir acerca de lanecesidad de determinar precozmente el genotipo, apartir de la adolescencia, con el fin de informar yaconsejar a la paciente sobre las medidas que hay queadoptar en función de su genotipo [16].
Antiandrógenos
Acetato de ciproterona
Se trata de un progestágeno dotado de efectos antigo-nadótropo y antiandrogénico. A la dosis de 1 mg día-1,solamente se expresa el efecto progestágeno y, porencima de ella, el efecto antiandrogénico depende de ladosis.
E – 802-A-36 ¶ Hiperandrogenismo en la adolescente
6 Ginecología-Obstetricia

Mecanismo de acción
Posee un efecto central de frenado de la secreciónhipofisaria de LH y FSH, lo que provoca la inhibicióncompleta de la función ovárica.
Su efecto periférico es doble: por una parte, inhibi-ción de la unión de la dihidrotestosterona (DHT) a sureceptor y, por otra parte, frenado de la acción deenzimas suprarrenales implicados en la esteroidogénesis
Posología
El esquema clásico consiste en la asociación de laciproterona acetato (CPA) (50 mg día-1) a un estrógenonatural (17-b-estradiol) en comprimido, gel o parche (de1 a 2 mg d-1) durante 20 o 21 días al mes. Segúndeterminadas especificaciones, esta asociación sólo escontraceptiva a partir del 3.er ciclo de utilización. Elefecto antigonadótropo está presente desde el primerciclo de utilización.
Espironolactona
Su estructura es parecida a la de la progesterona. Seune a los receptores mineralcorticoides, pero también alos receptores de la progesterona y de los andrógenos.No posee efecto antigonadótropo.
Mecanismo de acción
Su acción antiandrogénica proviene, por unaparte, de la disminución de la biosíntesis de testosteronapor inhibición del citocromo P450 y, por otra parte, dela inhibición de la unión de la DHT a los receptores delos andrógenos.
Posología
Su efecto a dosis de 200 mg día-1 de modo conti-nuado es claro a partir del 3.er mes de utilización. Espreferible utilizarla en asociación con un progestágenoo un estroprogestágeno ya que, sola, es responsable dealteraciones del ciclo y no tiene efecto contraceptivo.
Flutamida
Algunos autores [25] la proponen en las adolescentes,a dosis de 250 mg día-1, en asociación con un estropro-gestágeno de 3.a o 4.a generación (drospirenona), ya queno posee efecto contraceptivo. Es necesario un períodode observación más largo antes de poder aconsejar suutilización amplia.
Tratamientos cosméticosResulta muy evidente que el tratamiento farmacoló-
gico del hiperandrogenismo, independientemente de sucausa, debe acompañarse de un tratamiento cosmético,mediante técnicas de decoloración o mediante técnicasde depilación por métodos de arrancamiento físico oquímico. La depilación eléctrica o con láser, en manosexpertas, permite eliminar de modo definitivo el folí-culo pilosebáceo. Debe reservarse para las zonas másinconvenientes desde el punto de vista estético (cara,pezón, línea puboumbilical).
Existe un nuevo producto, la eflornitina, que consti-tuye el primer producto tópico que retarda el creci-miento del pelo. Algunas proteínas denominadaspoliaminas son necesarias para el crecimiento y ladiferenciación de las células del folículo piloso. Laproducción de estas poliaminas depende de la actividadde un enzima, la ornitina descarboxilasa. La eflornitinaactuaría bloqueando esta enzima.
Tratamiento del acné aisladoEl acetato de ciproterona no es más que una solución
terapéutica entre otras. Según la importancia y laextensión del acné:
• tratamiento local ante un acné de la cara moderada-mente inflamatorio (peróxido de benzoílo, antibióti-cos en gel, etc.);
• antibioticoterapia sistémica (ciclinas) y/o un estropro-gestágeno que contenga acetato de ciproterona(2 mg día-1), ante un acné inflamatorio de la cara oque se extienda de la cara al tronco;
• isotretinoína ante un acné macroquístico grave y/oresistente a un tratamiento bien llevado a cabo.
Caso particular del síndromede ovarios polimicroquísticos
Normas higienicodietéticasEl principal interés del diagnóstico precoz del SOPMQ
desde la adolescencia consiste en sensibilizar a lasjóvenes pacientes respecto a sus complicaciones meta-bólicas y proporcionarles educación sanitaria en relacióncon el respeto a las normas higienicodietéticas. Ellocomporta un abordaje global dirigido a corregir losdemás factores de riesgo cardiovascular (tabaco), acon-sejar una actividad física regular, alcanzar y mantenerun peso lo más fisiológico posible gracias a una dietaequilibrada. Es preciso investigar sistemáticamenteposibles trastornos de la conducta alimentaria (bulimia),ya que requieren un tratamiento especializado.
Tratamiento insulinosensibilizanteDiversos estudios han mostrado la eficacia de la
metformina sobre la tolerancia glucídica y, también,sobre el hiperandrogenismo. Su utilización podríaconstituir un buen complemento cuando el síndromemetabólico está en primer plano y es resistente a lasmedidas higienicodietéticas. Su utilización a largo plazodesde la adolescencia, propuesta por algunos autores [25],no deja de plantear problemas éticos y económicos.
Anticoncepción estroprogestágenaSi no existe indicación de un tratamiento antiandro-
génico, se puede utilizar un estroprogestágeno, obliga-toriamente de 3.a o 4.a generación, no androgénico,para corregir las alteraciones del ciclo y/o las manifesta-ciones menores de hiperandrogenismo. Actúa aumen-tando la SHBG y disminuyendo la concentración séricade gonadotrofinas, lo que colabora a la disminución delos andrógenos. Desde el punto de vista metabólico,provoca un discreto aumento de la insulinorresistenciaaunque nada prueba que su efecto sea nocivo a largoplazo [26].
■ ConclusiónEl diagnóstico de hiperandrogenismo en la adoles-
cencia se basa en un buen análisis clínico, completadocon algunos exámenes bioquímicos y morfológicos,según una estrategia actualmente bien establecida.Aunque el SOPMQ es, con mucho, la etiología másfrecuente, continúa siendo un diagnóstico de elimina-ción. Una vez establecido, es preciso analizar la repercu-sión metabólica actual y futura, con el fin de informar
“ Punto fundamental
El tratamiento del SOPMQ en la adolescenciaasocia un tratamiento antiandrogénico a laeducación higienicodietética para prevenir otratar posibles alteraciones metabólicas.
Hiperandrogenismo en la adolescente ¶ E – 802-A-36
7Ginecología-Obstetricia

y educar a la adolescente sobre su impacto sobre lafertilidad y su riesgo cardiovascular. La existencia de unsíndrome metabólico no debe llevar a la abstenciónterapéutica frente al hiperandrogenismo, del que nodebe subestimarse el impacto psicosocial. Finalmente,este diagnóstico debe llevar también a un estudiofamiliar, que permite diagnosticar un SOPMQ en el 50%de las hermanas de la paciente.
■ Bibliografìa[1] Ibanez L, Dimartino-Nardi J, Potau N, Saenger P. Premature
adrenarche: normal variant or forerunner of adult disease?Endocr Rev 2000;21:671-96.
[2] Apter D, Bützow TL, Laughlin GA, Yen SS. Gonadotropin-releasing hormone pulse generator activity during pubertaltransition in girls: pulsatile and diurnal patterns of circulatinggonadotropins. J Clin Endocrinol Metab 1993;76:940-9.
[3] Ibanez L, Potau N, Carrascosa A. Possible genesis ofpolycystic ovary syndrom in the periadolescent girl. CurrOpin Endocrinol Diab 1998;5:19-25.
[4] van Hooff MH, Voorhorst FJ, Kaptein MB, Hirasing RA,Koppenaal C, Schoemaker J. Predictive value of menstrualcycle pattern, body mass index, hormone levels andpolycystic ovaries at age 15 years for oligo-amenorrhoea atage 18 years. Hum Reprod 2004;19:383-92.
[5] Lobo RA. Ovarian hyperandrogenism and androgenproducing tumors. Endocrinol Metab Clin North Am 1991;20:773-805.
[6] Young RH, Scully RE. Ovarian Sertoli-Leydig cell tumors: aclinicopathological analysis of 207 cases. Am J Surg Pathol1985;9:543-69.
[7] Caron PH, Cogne M, Rumeau JL, Hoff J. Androgenicgranulosa cell tumor of the ovary: in vivo hormonal studies.J Endocrinol Invest 1993;16:545-8.
[8] Abbott DH, Dumesic DA, Franks S. Developmental origin ofpolycystic ovary syndrome-a hypothesis. J Endocrinol 2002;174:1-5.
[9] Strauss III JF, Dunaif A. Molecular mysteries of polycysticovary syndrome. Mol Endocrinol 1999;13:800-5.
[10] Dunaif A. Insulin resistance and the polycystic ovariansyndrome: mechanism and implications for pathogenesis.Endocr Rev 1997;18:774-800.
[11] Webber LJ, Stubbs S, Stark J, Trew GH, Margara R, Hardy K,et al. Formation and early development of follicles in thepolycystic ovary. Lancet 2003;362:1017-21.
[12] Dewailly D, Cortet-Rudelli C, Deroubaix-Allard D.Definition, clinical manifestations, and prevalance of PCOS.In:Azziz R, Nestler JE, Dewailly D, editors. Androgen excessdisorders in women. Philadelphia: Raven Press-Lippincott;1997. p. 259-68.
[13] Zacur HA. Prolactin abnormalities in PCOS. In: Azziz R,Nestler JE, Dewailly D, editors. Androgen excess disorders inwomen. Philadelphia: Raven Press-Lippincott; 1997.p. 287-94.
[14] The Rotterdam ESHRE/ASRM sponsored PCOS consensusworkshop group. Hum Reprod 2004;19:41-7.
[15] Balen AH, Laven JS, Tan SL, Dewailly D. Ultrasoundassessment of the polycystic ovary: international consensusdefinitions. Hum Reprod Update 2003;9:505-14.
[16] Forest MG, Morel Y. Formes non classiques dites « tardives »du déficit en 21-hydroxylase : diagnostic différentiel avec leshétérozygotes et conseil génétique. Rev Fr Endocrinol Clin1992;33:47-61.
[17] Dewailly D, Cortet-Rudelli C, Decanter C. Pathophysiologyand clinical manifestations of nonclassic 21-hydroxylasedeficiency. In: Azziz R, Nestler JE, Dewailly D, editors.Androgen excess disorders in women. Philadelphia: RavenPress-Lippincott; 1997. p. 173-80.
[18] Azziz R, Carmina E. Idiopathic Hirsutism: definition,prevalence and inheritance. In: Azziz R, Nestler JE,Dewailly D, editors. Androgen excess disorders in women.Philadelphia: Raven Press-Lippincott; 1997. p. 529-34.
[19] Cortet-Rudelli C, Desailloud R, Dewailly D. Drug-inducedandrogen excess. In:Azziz R, Nestler JE, Dewailly D, editors.Androgen excess disorders in women. Philadelphia: RavenPress-Lippincott; 1997. p. 613-24.
[20] Nelson-DeGrave VL, Wickenheisser JK, Cockrell JE,Wood JR, Legro RS, Strauss 3rd JF, et al. Valproate potentiatesandrogen biosynthesis in human ovarien theca cells.Endocrinology 2004;145:799-808.
[21] Diamanti-Kandarakis E, Chrousos GP. Cushing’s disease andandrogen excess. In:Azziz R, Nestler JE, Dewailly D, editors.Androgen excess disorders in women. Philadelphia: RavenPress-Lippincott; 1997. p. 569-84.
[22] Deroubaix-Allard D, Prevost G, Dewailly D.Acromegaly andandrogen excess. In:Azziz R, Nestler JE, Dewailly D, editors.Androgen excess disorders in women. Philadelphia: RavenPress-Lippincott; 1997. p. 585-91.
[23] Azziz R, Dewailly D. Diagnosis, screening, and treatment ofnonclassic 21-hydroxylase deficiency. In:Azziz R, Nestler JE,Dewailly D, editors. Androgen excess disorders in women.Philadelphia: Raven Press-Lippincott; 1997. p. 181-92.
[24] Spritzer P, Billaud L, Thalabard JC, Birman P, Mowszowicz I,Raux-Demay MC, et al. Cyproterone acetate versushydrocortisone treatment in late-onset adrenal hyperplasia.J Clin Endocrinol Metab 1990;70:642-6.
[25] Ibanez L, Valls C, Cabre S, De Zegher F. Flutamide-metformin plus ethinylestradiol-drospirenone for lipolysisand antiatherogenesis in young women with ovarianhyperandrogenism: the key role of early, low-dose flutamide.J Clin Endocrinol Metab 2004;89:4716-20.
[26] Korytkowski MY, Mokan M, Horwitz MJ, Berga SL.Metabolic effects of oral contraceptives in women withpolycystic ovary syndrome. J Clin Endocrinol Metab1995;80:3327-34.
C. Richard.S. Jonard.D. Dewailly ([email protected]).Service de gynécologie endocrinienne et de médecine de la reproduction, centre hospitalier universitaire de Lille, hôpital Jeanne deFlandre, 2, avenue Oscar-Lambert, 59037 Lille cedex, France.
Cualquier referencia a este artículo debe incluir la mención del artículo original: Richard C., Jonard S., Dewailly D. Hyperandrogénie chezl’adolescente. EMC (Elsevier SAS, Paris), Gynécologie, 802-A-36, 2006.
Disponible en www.emc-consulte.com (sitio en francés)Título del artículo: Hyperandrogénie chez l’adolescente
Algoritmos Ilustracionescomplementarias
Vídeos /Animaciones
Aspectoslegales
Informaciónal paciente
Informacionescomplementarias
Autoevaluación
.
E – 802-A-36 ¶ Hiperandrogenismo en la adolescente
8 Ginecología-Obstetricia