Universidad Nacional Autónoma de México Facultad de Química Glosario de términos. Prácticas de...
-
Upload
juan-francisco-guzman-quiroga -
Category
Documents
-
view
219 -
download
0
Transcript of Universidad Nacional Autónoma de México Facultad de Química Glosario de términos. Prácticas de...

Universidad Nacional Autónoma de MéxicoFacultad de Química
Glosario de términos. Prácticas de Métodos espectroscópicos, Estructura y Propiedades de
Proteínas.
Hugo Alfredo Brito Arellano
Bioquímica experimental
Profesoras:
Sobeida Sánchez NietoBertha Reséndiz Vázquez
Mayo de 2010
Índice • Absorbencia • Blanco • Botón • Centrifugación • Coeficiente de extinción molar • Contaminantes de proteínas • Cromatografía de afinidad • Cromatografía exclusión molecular • Cromatografía de intercambio iónico • Cuerpo negro • Curva patrón • Desviación negativa• Desviación positiva • Elución • Espectro electromagnético • Espectro de absorción• Espectro de emisión• Espectrofotometría • Espectrofotómetro • Fotodetector • Fuente de la proteína • Fuente de radiación • Hidrofílico • Hidrofóbico • Lactato deshidrogenasa (LDH)

• Ley de Lambert y Beer • Ley de Lambert desviaciones
instrumentales • Ley de Lambert desviaciones químicas• Ley de Lambert desviaciones reales• Longitud de una onda • Luz monocromática • Monocromador • Precipitación por salado • Proteína • Región UV • Región visible • Salting in • Salting out • Sobrenadante • Solvatación • Técnica de biuret • Técnica de bradfor • Técnica de Lowry• Transmitancia
• Absorbancia
A = - log T = - log P / P0Donde T es la transmitancia, (P) la potencia de luz que alcanza al detector cuando está interpuesta la muestra y (PO) cuando está interpuesto un “blanco”.
• BlancoMuestra que contenga todas los componentes del sistema menos aquel que se desea medir. con el se calibra el instrumento a absorbancia igual a 0.
• Botón:Nombre con el que se denota al sedimento resultante después del proceso de centrifugación.
• Centrifugación Método por el cual se pueden separar sólidos de líquidos de diferente densidad provocando la sedimentación de los sólidos o de las partículas de mayor densidad.

• Coeficiente de extinción molar:
Es una medida de la cantidad de luz absorbida por unidad de concentración. Define que tanta radiación (de longitud de onda de onda adecuada) puede captar un compuesto.
• Contaminantes de proteínas:
Son aquellos compuestos que se encuentran mezclados con la proteína de interés y que restan pureza a la muestra analizada. Generalmente son otras proteínas, carbohidratos, materia sólida y grasas.
• Cromatografía de afinidad:
Método de separación cromatografíca que consiste en separar compuestos mediante la afinidad de alguno de ellos hacia ciertos ligandos específicos como anticuerpos, cofactores o iónes metálicos.
Referencias bibliográficas
Thomas J. Bruno, Paris D. N. Svoronos. Manual de fundamentos espectroscopicos CRC Press, 2005.
Jimeno, Antonio; Ballesteros, Manuel; Ugedo, Luis. Biología. Fuenlabrada: Santillana, 1997.
Atkins, Peter; « teoria cuántica introduccion y principios» New York: Oxford University Press.
Tipler, Paul Allen (1994). Física. 3ª Edición. Barcelona: Reverté.
Burke, John Robert (1999). Física: la naturaleza de las cosas. México DF: International Thomson Editores.
Lehninger, Albert (1993). Principios de Bioquimica 2nd Ed.. Worth Publishers
Voet, Donald; Voet, Judith G. (2004). Bioquimica , 3a edición.

• Cromatografía de intercambio iónico:
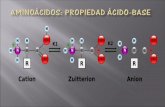
Técnica que separa compuestos en base a la carga de estos. Los grupos cargados sobre la superficie de estas moléculas tienen interacción con grupos presentas en las fase estacionaria. La carga de algunos compuestos depende del pH en el que se encuentran las soluciones. son generalmente Negativas cuando su pI es menor que el pH y positivas cuando el pI es mayor que el pH.
• Cromatografía de exclusión molecular:
También conocida como cromatografía por filtración en gel, separa las partículas de la muestra en función de su tamaño. Generalmente se trata de una cromatografía de baja resolución. En esta cromatografía, la fase estacionaria consiste en largos polímeros entrecruzados que forman una red tridimensional porosa y el tamaño de los poros es tal que algunas moléculas (las demasiado grandes) no podrán ingresar a esos poros, en tanto que otras (las suficientemente pequeñas) podrán pasar libremente.
Los poros quedan conectados formando una malla o red, lo cual determina una serie de caminos a ser recorridos por las moléculas que acceden al interior de esta.
De esta forma se unen a resinas con carga opuesta y la elución se lleva a cabo usando un gradiente de concentración de sales en orden creciente de concentración.

• Cuerpo negro:
Un cuerpo negro es un objeto teórico o ideal que absorbe toda la luz y toda la energía radiante que incide sobre él. Nada de la radiación incidente se refleja o pasa a través del cuerpo negro. A pesar de su nombre, el cuerpo negro emite luz y constituye un modelo ideal físico para el estudio de la emisión de radiación electromagnética.
• Curva patón:
Marco de referencia que se construye de cantidades conocidas de una sustancia que se utiliza para determinar la cantidad de proteínas presente en una muestra .
• Desviación negativa:
Se dan cuando la magnitud medida es menor que la real y llevan a que no se obtengan relaciones lineales. (Por ejemplo Abs en función de concentración en la ley de Beer)
• Desviación positiva:
Ocurren cuando la magnitud medida es mayor que la real y llevan a que no se obtengan relaciones lineales. (Por ejemplo Abs en función de concentración en la ley de Beer)
• Elución:
Extracción de una sustancia absorbida desde un lecho poroso o columna de cromatografía mediante un disolvente adecuado.
Espectro electromagnético :
Se refiere a la distribución energética del conjunto de las ondas electromagnéticas.
En determinaciones colorimétricas, se cumple una relación proporcional entre la intensidad de color que da una reacción y la cantidad del reactivo que la provoca.

• Espectro de emisión:
Es un conjunto de frecuencias de las ondas electromagnéticas emitidas por átomos de ese elemento, en estado gaseoso cuando se le comunica energía. El espectro de emisión de cada elemento es único y puede ser usado para determinar si ese elemento es parte de un compuesto desconocido.
• Espectrofotometría:
Método instrumental de análisis, para medir la absorción de radiación que interactúa con la materia. Es considerada una técnica cualitativa y cuantitativa.
Referido a un objeto se denomina espectro electromagnético o simplemente espectro a la radiación electromagnética que emite (espectro de emisión) o absorbe (espectro de absorción) una sustancia.
• Espectro de absorción:
Fracción de la radiación electromagnética incidente que un material absorbe dentro de un rango de frecuencias.

• Fuente de proteína:
Es la materia prima desde la cual se pretende extraer una proteína de interés. Puede ser vegetal o animal.
• Fuente de radiación:
Lámparas empleadas en el espectrofotómetro que tienen intensidad constante en el rango de longitud de onda que cubren ( usualmente es lámpara de tungsteno para luz visible y deuterio para ultravioleta) Esta radiación se hace incidir sobre las soluciones para efectuar el análisis.
• Espectrofotómetro:
Instrumento que permite comparar la radiación absorbida o transmitida por una solución que contiene una cantidad desconocida de soluto, y otra que contiene una cantidad conocida de la misma sustancia.
• Fotodetector:
Transductor de luz que proporciona una señal eléctrica como respuesta a la radiación óptica que incide sobre la superficie sensor. Existen dos tipos fundamentales de detectores de luz, los térmicos y los fotónicos que operan con mecanismos de transducción diferentes.

• Hidrofílico:
Comportamiento de toda molécula que tiene afinidad por el agua. En una disolución o coloide, las partículas hidrófilas tienden a acercarse y mantener contacto con el agua. Las moléculas hidrófilas son a su vez lipófobas, es decir no tienen afinidad por los lípidos o grasas y no se mezclan con ellas.
• Hidrofóbico:
En el contexto fisicoquímico, el término se aplica a aquellas sustancias que son repelidas por el agua o que no se pueden mezclar con ella. Un ejemplo de sustancias hidrófobas son los aceites.
• Lactato Deshidrogenasa (LDH):
Enzima catalizadora que se encuentra en muchos tejidos del cuerpo, pero su presencia es mayor en el corazón, hígado, riñones, músculos, glóbulos rojos, cerebro y pulmones. Se prohíbe cualquier forma de reproducción parcial o total de esta
obra. De hacerlo incurriría en un delito en agravio de su autor intelectual <<emostar>> Copyrygth© México 2010
Notas

En la que: I1 I0 son las intensidades saliente y entrante respectivamente; a es el coeficiente de absorción, l es la longitud atravesada por la radiación, c es la concentración del medio.
• Ley de Lambert-Beer (desviaciones instrumentales)
Provienen de la utilización de luz no monocromática, ya que la pureza espectral del haz de radiación proveniente de la fuente, depende del ancho de banda espectral del monocromador. La deducción de la ley de Beer supone radiación monocromática y los monocromadores en realidad proporcionan una banda de longitudes de onda.
• Ley de Lambert-Beer (desviaciones químicas )
Dependen de la naturaleza química del sistema en estudio. Las desviaciones son causadas, generalmente, por equilibrios en solución que involucran a la especie absorbente y alteran su concentración originando desviaciones positivas o negativas.
lceII 0
1
Corresponde a la categoría de las oxidorreductasas, dado que cataliza una reacción redox, en la que el piruvato es reducido a lactato gracias a la oxidación de NADH a NAD+. Participa en el metabolismo energético anaerobio, reduciendo el piruvato (procedente de la glucólisis) para regenerar el NAD+, que en presencia de glucosa es el sustrato limitante de la vía glucolítica.
• Ley de Lambert –Beer
Es una relación empírica que relaciona la absorción de luz con las propiedades del material atravesado.Relaciona la intensidad de luz entrante en un medio con la intensidad saliente después de que en dicho medio se produzca absorción. La relación entre ambas intensidades puede expresarse a través la siguiente relación:

• Luz
Es la clase de energía electromagnética radiante que puede ser percibida por el ojo humano. En un sentido más amplio, el término luz incluye el rango entero de radiación conocido como el espectro electromagnético.
• Luz monocromática:
La luz monocromática es aquella que está formada por componentes de un solo color. Es decir, que tiene una sola longitud de onda, correspondiente al color a diferencia de la luz blanca que está formada por muchos componentes.
• Monocromador:
Rejilla o prisma insertado en un espectrofotómetro que tiene la capacidad de filtrar la luz blanca de modo que se obtenga luz monocromática de una determinada longitud de onda.
• Ley de Lambert-Beer (desviaciones reales)
Provienen de los cambios en el índice de
refracción del sistema analítico, pues como e depende del índice de refracción de la muestra, la ley de Beer sólo se cumple para bajas concentraciones, en donde el índice de refracción es esencialmente constante, ya que no es la absortividad la que es constante sino la expresión:e = e verdadero h /(h 2+2)2 donde h es el índice de refracción de la solución.
• Longitud de Onda:
Es la distancia que recorre la onda en el intervalo de tiempo transcurrido entre dos crestas o valles consecutivos (máximos consecutivos) describe cuán larga es la onda.

logre la formación de un precipitado de proteínas que dependiendo de la naturaleza de la mezcla tendrá una composición característica.
• Proteína:
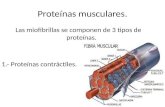
Las proteínas son macromoléculas formadas por cadenas de aminoácidos que desempeñan un papel fundamental para la vida y son las biomoléculas más versátiles y más diversas. Son imprescindibles para el crecimiento del organismo. Realizan una enorme cantidad de funciones diferentes, entre las que destacan:Estructural, Reguladora, Transportadora, Defensiva, Contráctil.
• Región UV:
Zona del espectro electromagnético comprendida entre los 400 nm y los 15 nm. Su nombre proviene de que su rango empieza desde longitudes de onda más cortas de lo que los humanos identificamos como el color violeta.
• Precipitación:
Técnica empleada para separar o purificar sustancias que se encuentran disueltas en un solvente, puede inducirse la precipitación mediante frotamiento, temperatura, inserción de cristales, formación de complejos o cambios en el medio de disolución como el pH o la concentración de sales.
• Precipitación por salado:
Técnica que se emplea para la separación y purificación de proteínas. Consiste en saturar el medio de disolución con sal de modo que se afecten las interacciones de solvatación y se
Esta técnica tiene como objetivo la formación de materia sólida que dada una diferencia de gravedad se deposita en el fondo del recipiente.

• Sobrenadante:
Fracción que permanece en la parte superior de un recipiente una vez que este fue sometido a un proceso de centrifugación.
• Solvatación:
Proceso de atracción y asociación de moléculas de un disolvente con moléculas o iones de un soluto. Al disolverse los iones en un solvente, se dispersan y son rodeados por moléculas de solvente. A mayor tamaño del ion, más moléculas de solvente son capaces de rodearlo, y más solvatado se encuentra el ion.
• Región visible:
Zona del espectro electromagnético que el ojo humano es capaz de percibir. A la radiación electromagnética en este rango de longitudes de onda se le llama luz visible o simplemente luz. No hay límites exactos en el espectro visible; un típico ojo humano responderá a longitudes de onda desde 380 a 780 nm.
• Salting in:
Fenómeno que se da cuando una proteína globular aumenta su solubilidad al incrementar la concentración de iones en el medio.
• Salting out:
Fenómeno que ocurre cuando una concentración excesiva de iones en un medio determinado provoca la disminución en la solubilidad de proteínas presentes y estas precipitan.

• Técnica de Bradford:
Se basa en la unión de un colorante, Comassie Blue G-250 (también Serva Blue) a las proteínas. El colorante, en solución ácida, existe en dos formas una azul y otra naranja. Las proteínas se unen a la forma azul para formar un complejo proteína-colorante con un coeficiente de extinción mayor que el colorante libre. Este método es sensible (1-15 μg), simple, rápido, barato y pocas sustancias interfieren en su determinación. Entre las sustancias que interfieren están los detergentes y las soluciones básicas.
• Técnica de Lowry:
Este procedimiento involucra la formación de un complejo cobre - proteína en solución alcalina. Este complejo reduce al reactivo fosfomolibdico- fosfotungstato lo que produce una intensa coloración azul medible espectrofotométricamente.
• Técnica de Biuret:
Se basa en la formación de un complejo coloreado entre el Cu2+ y los grupos NH de los enlaces peptídicos en medio básico. 1Cu2+ se acompleja con 4 NH y la intensidad de coloración es directamente proporcional a la cantidad de proteínas (enlaces peptídicos) y la reacción es bastante específica, de manera que pocas sustancias interfieren. La sensibilidad del método es muy baja y sólo se recomienda para la cuantificación de proteínas en preparados muy concentrados (por ejemplo en suero).

La transmitancia de una muestra está normalmente dada porcentualmente, definida como:
Este método se basa en la reacción de Biuret, donde los enlaces peptídicos reaccionan con el Cu2+ en condiciones alcalinas produciendo Cu+, después se reduce el reactivo de Folin por las proteínas tratadas con cobre a azul heteropolimolibdeno. El color se desarrolla en la segunda reacción (con el fosfomolibdotungstato) y es primeramente debida a los aminoácidos tirosina, triptófano, y en menor grado por cisteína, cistina e histidina.
• Transmitancia:
Magnitud que expresa la cantidad de energía que atraviesa un cuerpo en la unidad de tiempoSu expresión matemática es:
Donde I0 es la intensidad del rayo incidente e I es la intensidad de la luz que viene de la muestra.
0II
T
%)100(%0II
T