DAMAGE CONTROL INTRAHOSPITALARIO - … · Laparotomía exploradora inmediata con control rápido...
Transcript of DAMAGE CONTROL INTRAHOSPITALARIO - … · Laparotomía exploradora inmediata con control rápido...
DAMAGE CONTROL
INTRAHOSPITALARIO
Dra. Nuria Martín Marata
Anestesiología Hospital Vall d’Hebrón
Área de Traumatología
17 Mayo 2017
• Mujer 20 años (50kg, 1,55m)
• No AMC
• No AP de interés
• Código PPT 0
• Alfa 1
• Charlie 1/5
• Romeo 2
• Hotel 2
• Golf 12
Valoración extrahospitalaria
• Hora de activación: 00:32 am
• Llegada al hospital: 01:31 am
• Accidente de tráfico de alta energía: colisión coche-muro,
copiloto, sin cinturón de seguridad.
• TCE con pérdida de conocimiento inicial, recuperación
hasta GCS12 (O3V4M5). No alteración pupilar. No fetor
enólico. Hemodinámicamente y respiratoriamente
estable. Abdomen doloroso a la palpación y con defensa.
Vómito in situ de características hemáticas.
• EF: temperatura piel fría. Palidez.
Manejo extrahospitalario
A. Se canaliza acceso vascular de grueso
calibre y se inicia fluidoterapia con
cristaloides a razón 20-30mL/kg durante el
traslado.
B. Ante la sospecha de sangrado activo pero
con estabilidad hemodinámica, decidimos
no iniciar fluidoterapia para evitar
aumentar TAS y favorecer el sangrado.
C. Por mecanismo lesional, sospechamos
lesiones graves. Decidimos IOT por
alteración de GCS e iniciamos
fluidoterapia con cristaloides (20-30mL/kg).
D. Ante la sospecha de lesión intracraneal
iniciamos fluidoterapia +/- soporte
vasoactivo con fármacos para mantener
TAS>120mmHg.
•Analgesia: Fentanilo 50 mg.
•Antiemético: granisetron 1mg
•TA 102/54 mmHg, FC 100 lpm. SatO2 99% con mascarilla
de alto flujo de O2
Fluidoterapia: 500 + 500mL de Suero Salino
Normal ClNa 0’9% (SSN).
Valoración intrahospitalaria (Kirschner)
• Portadora de collarín cervical y de una vía periférica gruesa.
• Vía aérea libre. Ventilación espontánea. No asimetrías en tórax a la inspección, palpación o auscultación. FR 18rpm. SatO2 99% (mascarilla de alto flujo de O2)
• PANI 82/50. RS 120lpm. Pulsos periféricos débiles pero simétricos. No evidencia de puntos sangrantes externos. Abdomen distendido con discreto hematoma a nivel epigástrico. Defensa abdominal.
• GCS de 8 (O2/V2/M4) ,agitación creciente y PICNR pero con exotropia del ojo izquierdo hacia temporal sin deformidad facial evidente. Movilización espontánea puntual de las 4 extremidades con retirada al dolor de forma simétrica.
Resucitación
A. En la valoración inicial destaca la alteración del nivel de consciencia. Procedemos a IOT y trasladamos para realizar TC craneal.
B. Sospechamos sangrado activo. Activamos protocolo de transfusión masiva y administramos 1g ácido tranexámico. Realizamos EcoFAST. Si es positivo indicaremos laparotomía emergente.
C. Canalizamos otro acceso venoso para iniciar fluidoterapia. Cursamos pruebas de laboratorio. Debemos valorar realizar bodyTC diagnóstico.
D. La paciente se encuentra en shock. Iniciamos perfusión de NAD para mantener tensiones.
• Canalizamos otro acceso venoso periférico de grueso
calibre
• Analítica + reserva de sangre
• Ringer Acetato 1000mL
• IOT. Inducción de secuencia rápida (MDZ
6mg+Fentanilo 150mg + Rocuronio 60mg). TET #7.
Conectada a respirador muestra una capnografía de 26
mmHg.
Valoración secundaria (intrahospitalaria) • Abdomen distendido y timpánico (hemiabdomen superior) con
incipiente hematoma. No deformidades esqueléticas apreciables a la exploración.
• E-FAST:
Líquido libre intraabdominal (Morrison
y receso esplenorrenal).
Correcto deslizamiento de hojas
pleurales sin signos de neumotórax.
Corazón con taquicinesia sin
asimetrías ni derrame pericárdico.
Vena cava inferior (parcialmente por artefactos) muestra
diámetro de 12 mm e imágen de colapsabilidad.
• Constantes
• PANI 76/42 mmHg
• FC 136 lpm
• ¿Más fluidoterapia?
• 500mL de hidroxietilalmidón (HEA) 130/ 0’4.
• Monitorización invasiva
• GSA inicial: Hb 9’7 gr/dL, pH 7’25 y EB – 11, lactatos
2’39 mmol/L , PaO2/FiO2 > 300 (FiO2 0’6), PEEP+5.
PaCO2 34 mmHg.
• Colocación de sondas orogástrica y vesical con discreta
hematuria macroscópica.
Tras la reposición inicial con Ringer
Acetato y HEA 130/0’4...
PAI 104/55 mmHg (PAM 72mmHg)
FC 112 lpm
SpO2 100%.
Damage control
A. Parece evidente que la paciente presenta un sangrado intraabdominal activo. Debemos optar por la hipotensión permisiva hasta que controlemos la hemorragia de forma quirúrgica.
B. Parece que el sangrado está controlado por la normalización de las tensiones tras la fluidoterapia. Decidimos trasladar a bodyTC para descartar otras lesiones.
C. Avisamos a equipo de cirugía general y procedemos a laparotomía emergente.
D. Estamos ante un TCE + sangrado abdominal activo. Estabilizamos a la paciente y trasladamos a bodyTC para descartar lesión intracraneal.
Damage Control Resuscitation
•Desde su llegada al hospital hasta ese momento:
• Ácido tranexámico 1 gr + perfusión (1gr en 8 horas).
• Complejo protrombínico 1000 UI.
• Fibrinógeno 2gr.
• Ringer Acetato 1000mL.
• HEA 130/0’4 500mL.
• Noradrenalina 0.3 ug/Kg/min para mantener PAM > 80 mmHg.
•Avisamos equipo de Cirugía General y organizamos
traslado a sala TC.
Activamos Protocolo de Transfusión
Masiva
Damage Control Surgery vs TC A. Se trata de una paciente con sangado activo y
HD inestable. Probablemente no aguantará el
traslado, por lo que se debe proceder a una
laparotomía emergente.
B. A pesar del ecoFAST positivo, el equipo de
cirugía necesita un TC abdominal para
confirmar el origen exacto del sangrado.
Debemos estabilizar a la paciente para
trasladarla al TC.
C. La paciente necesitará una laparotomía pero
seguimos sospechando una lesión
intracraneal. Debemos descartarla para poder
mantener una reanimación hipotensiva durante
la cirugía.
D. Es probable que el sangrado abdominal pueda
controlarse de forma endovascular.
Realizaremos un TC para definir el origen de
la hemorragia.
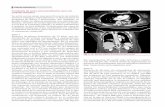
•Gran neumoperitoneo que por su disposición y la asociación de sangrado activo podría tener un origen gástrico.
•Múltiples laceraciones hepáticas de predominio derechos con áreas de extravasación compatible con focos de sangrado activo.
•Área de contusión pancreática (cabeza).
•Pequeña laceración esplénica sin signos de sangrado activo.
•Liquido libre denso compatible con hemoperitoneo.
•Adrenales hipercaptantes e ingurgitadas.
•Asas de intestino delgado engrosadas hipercaptantes en el contexto del shock.
• TC craneal normal HIPOTENSIÓN PERMISIVA
• PAS 80 mmHg.
• Analítica de ingreso (previa reanimación): Hb 9.2 gr/dl ,
leucocitos 16750, plaquetas 212000, TQ 70%, TTPa
32.2seg (ratio 1.32), fibrinógeno 1.32g/L, creat 0.5 mg/dl.
Na 137 mmol/L.
• Tratamiento: LAPAROTOMÍA EXPLORADORA
Laparotomía
• PAI 82/45 mmHg, FC 114lpm
• SpO2 100%.
• Monitorización: análisis contorno de la
onda de pulso + ScvO2 contínua.
VVS de 18% , IC 1’9 ml/min/m2 y ScvO2
72%.
• 2 accesos venosos de grueso calibre
femoral + CVC.
• Hemoperitoneo masivo
contaminado con contenido
gástrico, estallido gástrico,
laceración esplénica en tercio
medio que afecta al hilio y
laceración hepática afectando
a los segmentos V, VI y VII.
• Esplenectomía
• Sutura de laceración
gástrica
• Packing hepático
(lóbulo derecho) con 7
gasas grandes.
• Bolsa de Bogotá
• 10 CH
• 4 PFC
• 2 pool de plaquetas (8 unidades)
• 4 gr de fibrinógeno
• 2 gr de ácido tranexámico (protocolo CRASH-2)
• 4 gr de ClCa2
• 141’75 mEq de HCO3Na+
• 2000 UI de complejo protrombínico
• 2000 ml de Ringer Acetato
• 1000 ml de HEA 130/0’4.
• NAD 0.3-0.9 μg/kg/min.
Evolución postoperatoria
• UCI
• Sedoanalgesiada + VM 48h.
• Revisión quirúrgica: no signos de sangrado ni necesidad de
resección hepática. Se retira packing + cierre de pared abdominal.
• Hospitalización
• Buena evolución postoperatoria; ALTA a domicilio a los 15 días de
ingreso.
Damage Control
• Manejo de las lesiones abdominales
en la Segunda Guerra Mundial
• Damage Control Surgery: cirugía para el control y la estabilización
del paciente.
• Damage Control Resuscitation (DCR)
• Otros: Damage Control Radiology (DCRx), Damage
Control Orthopedics…
• Incremento sustancial de la
supervivencia en los pacientes más graves.
• Mejoras en salud pública y cuidados prehospitalarios gran aumento de los pacientes que sobreviven y que llegan gravemente heridos al hospital
- Lesiones en múltiples órganos, hemorragia masiva y reserva fisiológica
escasa DAMAGE CONTROL
DAMAGE CONTROL SURGERY is a treatment
strategy of temporization; prioritizing physiological
recovery over anatomical repair.
•Damage Control Resuscitation: Nuevas estrategias de resucitación
destinadas a limitar el desequilibrio fisiológico de los pacientes traumáticos.
Damage Control Resuscitation
• Objetivos:
• Tratar el déficit de volumen intravascular
• Prevenir o tratar de forma precoz la coagulopatía aguda del traumático
• Preservar la capacidad de transporte de oxígeno
• Reparar el endotelio
minimizar la pérdida sanguínea
maximizar la oxigenación tisular
optimizar los resultados
• Damage Control (DC) 4 fases:
• DC 0: PreHOSP+URG. Reconocer mecanismo lesional+DCR+traslado a quirófano . Scoop & run. Ác tranexámico, ISR, acceso venoso, prevención hipotermia, profilaxis atb y antitetánica y preparación equipo.
• DC I: QUIR. Laparotomía exploradora inmediata con control rápido del sangrado y la contaminación. Packing y cierre temporal.
• DC II: UCI. Estabilización. Reexplorar (lesiones no detectadas)
• DC III: QUIR. Paciente estabilizado. Cirugía/s definitiva/s
DC 0: DCR
• DCR. Componentes principales:
• <C>ABC
• Hipotensión permisiva
• Limitar cristaloides. Uso temprano de sangre y hemoderivados
• Uso temprano de ácido tranexámico
• DCS (DC I)
Coagulopatía del traumático
• ¿Hipotensión permisiva?
• Objetivo: limitar la reanimación con fluidos
↓disrupción del coágulo y el empeoramiento de la coagulopatía
dilucional.
• Limitada en el tiempo (hasta el control de la hemorragia).
• Ojo si TCE!!!
“Injection of a fluid that will
increase blood pressure has
dangers in itself. If the
pressure is raised before the
surgeon is ready to check
the bleeding that may take
place, blood that is sorely
needed may be lost.”
Si TCE:
PAM>80
PAS>120
PAS 80mmHg
PAM 50mmHg
• Efectos deletéreos de una reanimación con fluidos
excesiva
• Aumento de la lesión por reperfusión y de la adhesión
leucocitaria.
• Aumento de SDRA, SIRS y FMO.
RL es hipotónico
NO administrar
en TCE (1C)
Fluidoterapia
• Restaurar la perfusión tisular en el shock hemorrágico
severo
• ¿Cristaloide? ¿Coloide? ¿Cuál?
• No diferencias en la reducción de mortalidad
Resucitación inicial
• Paciente NORMOTENSO sin signos de hipovolemia NO
FLUIDOS (sí vía periférica)
• Paciente grave HIPOTENSO FLUIDOTERAPIA (dosis
bajas si el sangrado NO está controlado)
Hipotensión permisiva
(PAM 65mmHg, PAS 80-90mmHg)
Fluido de elección: CRISTALOIDE ISOTÓNICO
COLOIDES: uso restringido
• beneficio para HEA (130/04)
• clearence de lactato mejor
• menor daño renal agudo
• 67 pacientes con trauma
penetrante, comparando con suero
salino.
• HEA de última generación
• Indicación correcta
• Dosis adecuadas
• Indicación del HEA: hipovolemia debida a
hemorragia aguda cuando la reposición con
cristaloides no es suficiente.
• Ratio CCHH/PFC/Plaquetas
• PFC>CCHH beneficioso en la supervivencia
• Ratio óptimo no definido.
• PROPPR (pragmatic, randomized optimal platelet and plasma ratios)
• Protocolos de transfusión masiva
- Restaurar la volemia, el transporte de O2 y la capacidad hemostática
- Target de Hb 7-9 g/dL (1C)
¿1:1:1 para todos?
• Protocolos de hemorragia (transfusión) masiva.
• FIBRINÓGENO
• Crioprecipitados > PFC
• Control de las fuentes de sangrado.
• Monitorización de la hemostasia.
• Test viscoelásticos
• Optimización de los parámetros fisiológicos.
o El acido tranexámico reduce la mortalidad
en pacientes con trauma y sangrado.
o No hubo aumento de efectos trombóticos.
o Administrar ácido tranexámico en <3h de la
lesión a todos los pacientes con
TAS<110mmhg, FC>110 y evidencia de
sangrado. 1g en 10 min y 1g en 8h.
o No es caro y puede salvar muchas vidas
cada año en todo el mundo.
Annals of Surgery. Volume 261, Number 2, February 2015
Beneficio en (pacientes en
SHOCK):
-Disminución mortalidad
-FMO
• TC es la vía más rápida y más precisa para definir el lugar y la extensión de las lesiones estrategia de tratamiento.
• PACIENTES INESTABLES • ATLS: no TC.
• Rx torax.76% de lesions graves en tórax pasan desapercibidas.
• Rx lateral cervical. Sensibilidad 52%.
• Rx pelvis. Si pelvis inestable fijación.
• EcoFAST
•El paciente más grave y más inestable es el que
más se beneficia del TC.
- body TC <90seg.
- alta sensibilidad y especificidad en indentificar lesiones
que amenazan la vida.
- ¿por qué estan inestables? SANGRADO. Lo más importante es el
control del sangrado de la forma más precoz y precisa.
DAMAGE CONTROL RADIOLOGY
- Indentificar rápidamente lesiones potencialmente mortales,
incluyendo puntos de sangrado.
- Identificación o exclusión de lesiones craneales o de columna.
- Realizar triage rápido y preciso para derivar a IQ o control de la
hemorragia de forma endovascular.
-Los pacientes SIN
bodyTC tienen una
probabilidad de muerte
más alta (OR: 0.145)
-NNT 17
-1/6 pacientes en shock
-Cambio en la estrategia
de tratamiento 19%
Lancet. 2009 Apr 25;373(9673):1455-61
• Radiología intervencionista. Parte de DCR
• Oclusión arterial temporal con balón.
• Embolización.
• Colocación de stents.
• Hemorragia pélvica o retroperitoneal.
Cirugía más difícil.
• Conservación esplénica (pacientes jóvenes)
Conclusiones • El trauma grave es una causa importante
de muerte y discapacidad en pacientes jóvenes.
• ABCDE
• ≈ 30% de los pacientes llegan COAGULOPÁTICOS
• C de Coagulopatía
• Iniciar DCR aumenta la supervivencia
• Uso temprano de sangre y hemoderivados
• Ácido tranexámico
• Prevenir la hipotermia
• DCS/embolización
• TC es la herramienta más precisa para el diagnóstico de los pacientes graves.