Liquido
-
Upload
api-3702222 -
Category
Documents
-
view
911 -
download
6
Transcript of Liquido

Abril 2006 1
QUÍMICA BIOLÓGICA Tema: El Estado Líquido
Características Generales Presión de Vapor y Vaporización, Tensión
Superficial, capilaridad Viscosidad y fluidez.
.

Abril 2006 2
ESTADO LÍQUIDO
Cuando se enfría un gas pierde parte de su energía cinética en
forma de calor, y la velocidad de las moléculas disminuye, pero si
además este gas se comprime las moléculas caen dentro del campo de
las fuerzas de interacción de Van der Waals y entonces el gas pasa a
estado líquido

Abril 2006 3
DEFINICIÓNEstado intermedio y de transición entre el estado en que las fuerzas de interacción pueden mantener unidos y en posiciones
fijas y determinadas, átomos, iones y moléculas, que es el estado sólido, y el
estado en que reducidas estas interacciones a fuerzas intermoleculares de corto
alcance, las moléculas pueden separarse espontáneamente unas de otras y se llega al
estado gaseoso

Abril 2006 4
¿Cómo?P1 P2 P3 P4
T1 T2 T3 T4
Al disminuir la temperatura y aumentar la presión a un sistema gaseoso,
éste se transforma en líquido

Abril 2006 5
¡ACLARACIÓN!
Si al vapor sólo se le aumenta la presión, se convierte en líquido: El
proceso determina una CONDENSACIÓN
El gas no se convierte enlíquido, aumentando la presión
solamente y es necesario disminuir drásticamente la temperatura:
El proceso determina una LICUACIÓN
Podrías decir la diferencia entre, Vapor y Gas,

Abril 2006 6
SO2, Cl2, NH3, C3H8
Fácilmente Licuables
CH4, O2, CO, N2
Difícilmente licuables
H2, He. Muy difícilmente Licuables
Distancia entre las moléculas
Fuerzas
Atractivas
LICUACIÓN DE ALGUNOS GASES

Abril 2006 7
PRESIÓN DE VAPOR DE UN LÍQUIDOPRESIÓN DE VAPOR DE UN LÍQUIDO
V
L
La Energía Libre de ambas fases debe ser la
misma
dGlíquido = dGvapor
Equilibrio entre la velocidad de evaporación
y la velocidad de condensación, a esto se llama un equilibrio
dinámico
Presión de Vapor

Abril 2006 8
Deducción de la ecuación de Clausius Clapeyron
P1
P2
P3
Nivel del mar
Sobre elNivel del mar
Bajo elnivel del mar
T°C Ebullición del H2O adiferentes Presiones
A 100°C
A menos de100°C
A más de 100°C

Abril 2006 9
P e-Hv/RT
Donde P: PresiónHv : Calor molar de vaporización R : Constante Universal de los Gases.T :Temperatura absolutae : Número Neperiano
Del sistema anterior se puede deducir de que a mayor temperatura mayor presión de vapor.Esto se ve reflejado en las diferentes temperaturas de
ebullición del agua en distintos puntos del país.Para hacer más específicas las afirmaciones tenemos la
siguiente relación:

Abril 2006 10
Para convertir la proporción anterior en igualdad tenemos
P = e-Hv/RT x ConstanteDesarrollando:
LnP = Ln e-Hv/RT x Constante
LnP = Ln e-Hv/RT + Ln Constante
LnP = -Hv/RT Ln e + Ln Constante
LnP = – Hv (1) + CONSTANTE
RT

Abril 2006 11
LnP = – Hv 1 + CONSTANTE
R T
y = -b.x + a
COMPARANDO CON LA ECUACIÓN DE UNA RECTA
Ordenada AbscisaPendienteConstante

Abril 2006 12
REPRESENTANDO EN UNA LÍNEA RECTA
LnP
1 T°K
y2 - y1
x2 - x1
b =
(x1,y1)
(x2,y2)
b= pendiente = - Hv R
Constante a
El valor R en estos casos es de 1,987 Cal / mol°K

Abril 2006 13
Ejemplo N°1El agua tiene una presión de vapor diferente
para cada temperatura de la siguiente manera
T°K-1 T°C PmmHg LnP (20+273)-1 20 21,18 3,053 (30+273)-1 30 36,15 3,587 (40+273)-1 40 61,55 4,119 (50+273)-1 50 99,86 4,603

Abril 2006 14
LnP
1/T°K 3,09 3,19 3,30 3,41 X10-3
4,60
4,12
3,58
3,05
(3,15.10-3 , 4,337) (x1 , y1)
(3,35.10-3 , 3,36) (x2 , y2)
Con estos puntos se puedehallar la pendiente

Abril 2006 15
y2 - y1 = 3,36 - 4,337x2 - x1 3,35.10-3 - 3,15.10-3
Pendiente = b = -4 885 -Hv = -4 885 R -Hv = -4 885 x 1,987 cal/mol Hv = 9 706,5 cal/mol

Abril 2006 16
El calor molar de vaporización para el agua será 9706,5 Cal /mol, esto simplifica
posteriores cálculos, transformando la fórmula general de Clausius Clapeyron, para
dos puntos a la siguiente fórmula :
Ln P2 = Hv 1 - 1
P1 R T1 T2

Abril 2006 17
Ejemplo 2. Tomando en consideración que el agua tiene una temperatura en su punto de ebullición de 100°C a 1 atm ( 760 mm de Hg). ¿Cuál será la presión que se debe aplicar a un autoclave para que la temperatura de ebullición del sistema sea 110°C. (Hv = 9706,5 cal /mol.)
P1 = 760 mm HgT1 = (100 + 273) °KP2 = ???T2 = (110 + 273) °K
Ln P2 = 9706,5 1 - 1
760 1,987 373 383
Reemplazando en la fórmula anterior

Abril 2006 18
Ln P2 = 9706,5 (6,999x10-5) 760 1,987
Ln P2 = 0,3419 760
P2 =( e0,3419) x 760
P2 = 1069,8 mmHg = 1,4Atm

Abril 2006 19
Ejemplo 3.Un Autoclave esta averiado en su detector de temperatura si la presión que se registra es de 1.5 Atm, ¿Cuál será la temperatura en la que se encuentra el sistema?
P1 = 1 Atm.T1 = (100 + 273) °KP2 = 1,5 Atm.T2 = ???
Se debe tomar en cuenta que los sistemas autoclave
funcionan con H2O
Por tanto Hv= 9706,5 cal /molAplicando fórmula

Abril 2006 20
Ln 1,5 = 9706,5 1 - 1
1 1,987 373 T2
0,405 = 4885 (2,68 x 10-3 - 1/T2 )
8,29 x 10-5 = 2,68x10-3 - 1/T2
-2,59 10-3 = - 1/T2
385 °K = T2 = 385 - 273 =
T2 = 112°C

Abril 2006 21
AEOROSOLES
Los aerosoles de aplicación médica y farmacéutica se basan en la conversión de los líquidos volátiles en vapores a la presión y temperatura del ambiente
Gas Licuado
Principio activo
Presentaciones antiasmáticas
en BroncoespasmoSalbutamol

Abril 2006 22
HUMEDAD RELATIVA
H2O
Vapor de H2O Saturada
20°C
A 20°C La presión de vapor
del H2O es:21,18 mm de Hg
Si en el ambiente de Lima hay una presión de vapor
de agua de:19 mm de Hg entonces:
LA HUMEDAD RELATIVA SERÁ: 19 x 100 = 89,7% 21,18

Abril 2006 23
Conociendo la presión de vapor de una sustancia se puede averiguar la concentración. ejemplo: En
un experimento se quiere saber la cantidad de gramos de acetona por ml. en el ambiente (ver figura), sabiendo que, la presión de vapor de
dicha sustancia ha saturado el medio. La temperatura es de 20°C. Si la presión de vapor de
dicha sustancia es de 200 mm de Hg a dicha temperatura diga que cantidad de acetona estará
respirando un individuo por cada litro de aire inspirado

Abril 2006 24
6m.
3m.
4m
Fuente de acetona Olor aromático
Datos P: 200 mm HgT : 20°C = 293 °KV :6x4x3= 72 m3 =72 000 Litros

Abril 2006 25
Aplicando:PV=nRT
200 mm Hg . 1 Atm. 72 000L = n . 0,082 L.Atm. 293°K760 mm Hg °K.mol
788,62 mol = n
La masa molecular de la Acetona es 58 g/mol como 788,62 mol se encuentra en 72 000 L. La concentración en el aire será:
788,62 mol . 58 g/mol72 000L
0,6352 g/L

Abril 2006 26
Ascenso del capilar Cuando un capilar de radio “r”, se sumerge levemente en un líquido, éste experimenta un ascenso hasta una altura “h” debido al equilibrio que existe entre dos fuerzas: ascendente y descendente; la primera es dependiente de una fuerza tangencial denominada “”, tensiòn superficial, mientras que la segunda depende de la masa y la gravedad
Altura
Radio del
capilar
Tensión SuperficialDeducción
Método del ascenso del capilar

Abril 2006 27
Tensión SuperficialDeducción
Método del ascenso del capilar
‿ Fa
: Tensiòn Superficial
Fuerza ascendente
Cos = Fa
Fa = .Cos
Para toda la circunferencia
Fa = 2..r..Cos Capilar

Abril 2006 28
Fuerza descendente
h
Peso = Fuerza
F= m.g
m = .V V= r2h
Por tantoFd = .r2h.g
Ahora igualando Fuerzas tenemos
Fa = Fd

Abril 2006 29
2..r..Cos = ..r2.h.g 2.Cos = .r.h.g
= .r.h.g 2 Cos = .r.h.g
2
Cos , tiende a 1, cuando el líquido moja totalmente; pues el ángulo llega a cero. Cos 0º = 1

Abril 2006 30
DEDUCCIÓN DE LAS UNIDADES
= .r.h.g 2
En el sistema c.g.s.
= .r.h.g = m.L.L.L V . T2
= m.L.L.L L3 . T2
= m.L L .T2
= m.L L .T2
Masa xAceleraciónGramos x cm/seg2
DINAS
cm.
= Dinas
cm.

Abril 2006 31
¿Cuàl será la tensión superficial de una sustancia de densidad 0,812 g/ml. si en el capilar alcanza una altura de 11 mm.y el radio del mismo es de 0,06 cm.?
Reemplazando= .r.h.g
2
= 0,812 g/cm3.0,06cm.1,1cm.980 cm./seg2
2 = 26,26 Dinas/cm.

Abril 2006 32
TENSIÓN SUPERFICIAL
Es la fuerza en dinas/cm. de borde de la película que se opone a la expansión de la superficie
L
}dsA
B C
D
F
La siguiente representación indica las barras metálicas AB y CD unidas a través de una barra de longitud L, igual a 5 cm. La barra AD es móvil y puede prolongarse hasta romper la lámina de líquido ABCD (análoga a una pompa de jabón); ds es el desplazamiento, hasta el límite máximo que permite la resistencia de ABCD, en función de la fuerza F. La masa es 0,5g
m=0,5g

Abril 2006 33
Tomando en cuenta la definición de tensión superficial : Fuerza / longitud. Asumiendo que F= mxg y la masa de m= 0,5g (g= 980 cm/seg2)
= F
d
= F
2L
Reemplazando en
= 0,5g x 980cm./seg2
2x5cm.
Dinas
= 49 Dinas cm.

Abril 2006 34
Ejemplo. El radio típico de un vaso leñoso es aproximadamente de 0,02 cm. ¿Hasta que altura se elevará el agua en dicho vaso a 20°C?
Tensión superficial 20°CLíquido Unidades C.G.S. Unidades SI (Dina.cm-1) (N.m -1 )Acido acético 27,6 0,0276Acetona 23,7 0,0237Benceno 28,9 0,0289CCl4 26,6 0,0266Cloroformo 27,1 0,0271Etanol 22,3 0,0223Eter etílico 17,0 0,0170n Hexano 18,4 0,0184Mercurio 476 0,476Agua 72,75 0,07275

Abril 2006 35
Aplicando:
= h.r..g
2Cos
h = 2Cos
r..g
1
h = 2(72,75Dinas.cm-1)
(0,02cm) (1g.cm-3)(980cm.seg-2)
7,42cm

Abril 2006 36
La tensión superficial de las soluciones acuosas generalmente aumenta, si los solutos son ionizantes NaCl LiCl o sacarosa y otras sustancias que no se acumulan en la zona interfacial aire agua; disminuye cuando se trata de ácidos grasos y aún mas con las sales de estos.
Líquido
Zonas zigzagueantes Apolares.
Los puntos son zonas Polares
Aire

Abril 2006 37
Una solución de ácido caproico[ CH3- (CH2)4-COOH] 0,01 M en agua abate la disminución de la tensión superficial del agua en 15 dina.cm-1. El ácido cáprico 0,0005 M [ CH3- (CH2)8-COOH], disminuye la tensión superficial en un orden de 25 Dinas.cm-1.Los surfactantes más efectivos son los jabones
Palmitato de Sodio, Hexadecanoato de sodio. Jabón
Na+
—

Abril 2006 38
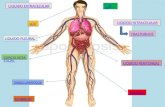
LA ACCIÓN DE LOS SURFACTANTES EN LA RESPIRACIÓN
La superficie más extensa del cuerpo humano en contacto con sus alrededores, es la superficie húmeda interna de los pulmones
Un adulto promedio requiere de un área pulmonar
aproximadamente igual ala de un campo de tenis, para
poder respirar.
Dicha área esta comprendida en un volumen relativamente pequeño del tórax, en los pulmones, y en cientos de millones de espacios diminutos de aire : los alvéolos

Abril 2006 39
Los alvéolos tienen un radio promedio de 0,005cm, comunicados por canales confluentes a través del árbol bronquial
Durante la inhalación normal,la presión alveolar es de 3 mm de Hg por debajo de la presión atmosférica. (760 mm deHg-3mm de Hg)( Presión manométrica = -3mm de Hg).El aire fluye hacia el interior de ellos por los bronquios.El tejido mucoso tiene una tensión superficial de 50 Dinas.cm-1

Abril 2006 40
ECUACION DE YOUNG - LAPLACE(superficies esféricas)
Pi - Po = 2 r
Pi : Presión interna alveolarPo : Presión externa ( Presión que existe entre los pulmones y la cavidad pleural)r: Radio del alvéolo.
Pi - Po = 2 (50 Dinas.cm-1) 0,005cm

Abril 2006 41
2 x 10+4 dinas.cm-2
...pero 760 mm de Hg = 1,013 x 10 +6 dinas.cm -2
Por tantoPi - Po = 15 mm de Hg
La presión del alvéolo es de 757 mm de Hg (-3)la presión Pulmón y cavidad pleural es 756 mm de Hg (-4)
Pi - Po = P757 - 756 = 1 mm de Hg

Abril 2006 42
Esto significa únicamente 1/15 de la presión que se requiere para la expansión de un alvéoloPara superar esto los alvéolos secretan un tipo especial de surfactante, fosfolipoproteico, el cual reduce en forma eficiente la tensión superficialEl surfactante aumenta la con grandes volúmenes y disminuye con pequeños volúmenes, estabiliza los espacios aéreos , evita la sobre distensión y la oclusión.

Abril 2006 43
MECANISMO DEL SURFACTANTE
H2O
Aire
Aire
H2O
Sacos Alveolares
Menor TensiónSuperficial
MayorTensiónSuperficial
Distensión
Disminución del
volumen

Abril 2006 44
El alvéolo puede expandirse sin dificultad 15 000 respiraciones cada día
Por lo tanto la primera respiración de la vida necesita un esfuerzo extraordinario.
En el neonato prematuro aún no funcionan las células que sintetizan el surfactante
En el “Síndrome de angustiarespiratoria de los
recién nacidos”, existe poca cantidad de surfactante.
En un bebe normal, los alvéolos están
plegados en el nacimiento, la diferencia de presión es
de 20 a 30 mm de Hg.

Abril 2006 45
Cuando la superficie del agua se cubre con una película delgada de material tenso activo se reduce la capacidad de evaporación en las represas acuíferas.
H2O
Tensoactivo
30 g de este material puede
servir para 10 000 m2
de área
Esta función la cumple el alcohol cetílico[ CH3- (CH2)14-CH2OH]

Abril 2006 46
AguaOil
MicelaAceite / Agua Agua / Aceite
Estructura de un jabón y su acción
— +
EMULSIONES

Abril 2006 47
Los tensoactivos naturales del organismo son los ácidos biliares, el ácido tauro cólico y el ácido glicocólico que se forman en el hígado y cumplen una función de emulsionantes, para preparar la absorción de los ácidos grasos y los acil glicéridos.

Abril 2006 48
VISCOSIDAD DE LOS LÍQUIDOS.
La viscosidad de un gas, de un líquido puro, o una solución es un índice de su resistencia a fluir. Cuando se estudia la viscosidad se mide la facilidad con que los fluidos circulan a través de un tubo capilar

Abril 2006 49
Radio: R
Radio: r
dr
L
Resistencia de Rozamiento
F= (2rL)dv dr
Donde 2rL es el área de superficie del cilindro interno y dv/dr el gradiente de velocidad. Donde : Viscosidad
Pero la Fuerza es Presión x Area
Pr2= (2rL)dv
dr

Abril 2006 50
dv = P r dr 2 L
Despejando dv
dv = P rdr 2 L0
v
R
r
Integrando
v = P (R2 - r2) 4L
Válido únicamente para el flujo laminar
El flujo laminar depende de los diámetros
pequeños y de la rapidez de los flujos lentos
(capilares sanguíneos).FLUJO NO TURBULENTO
Si las condiciones varían la velocidad corresponde a un flujo TURBULENTO

Abril 2006 51
¿Cómo se puede diferenciar?
El número adimensional de Reynolds
Nr = Dv
: Densidad del Líquido D: Diámetro del capilar v: Velocidad : Viscosidad
Flujo laminar: Valores bajos con Nr
hasta 3000
El flujo turbulento para valores
altos mayores de 4000

Abril 2006 52
Velocidad de flujo: Q (V/t)
V = PR4
t 8L
V: Volumen P: Presión R: Radio del capilar L: Longitud: Viscosidadt :Tiempo de flujo
= PR4t V 8L
ECUACIÓN DE POISEUILLE
Esto se aprovecha para que mediante el viscosímetro de Ostwald se obtenga la viscosidad relativa de los líquidos donde solo se compara densidades y tiempos de flujo.

Abril 2006 53
VISCOSIDAD RELATIVA
A
B
Parte del viscosímetro de Ostwald
muestra = (.t)muestra
referencia (.t)referencia
Capilar
: Densidadt : Tiempo de flujo de A a B
La viscosidad relativa notiene unidades, por lo comúnla sustancia de comparación
es el agua

Abril 2006 54
UNIDADESMáxima Máxima velocidadvelocidad
PresiónPresión
Mínima Mínima velocidadvelocidad
Plano fijoPlano fijo
L
=L.P V
=L.F V.A
=L.F L.s-1.A
=F.s A
=Dinas.seg cm2
o = Gramo cm.seg
POISE

Abril 2006 55
Sustancia Unidad : cP = centipoises*Sustancia Unidad : cP = centipoises*
•Agua Agua 1,005 cP 1,005 cP
•Aceite de Oliva Aceite de Oliva 84 cP84 cP
•Sangre Sangre 2 a 4 cP2 a 4 cP
•PlasmaPlasma 2 cP2 cP
•Suero Suero 1,7 cP1,7 cP
•Líquido cefalorraquídeo Líquido cefalorraquídeo 1,024 cP 1,024 cP
•OrinaOrina 1,00 a 1,14 cP1,00 a 1,14 cP
Valores de Viscosidad
*1 Poise = 100 Centipoises

Abril 2006 56
Area de sección transversal y velocidad de flujo
Sección transversal
cm2
5000
4000
3000
2000
1000
50
40
30
20
10
AORTA ARTERIOLAS VENULAS VENA CAVA ARTERIAS CAPILARES VENAS
VELOCIDADcm/seg

Abril 2006 57
VISCOSIDAD DE LA SANGRE
A. Glóbulos más centrales, la pared del vaso roza con el plasma
Aorta o vaso grande: Mayor velocidad. Menor viscosidad
B.Capilares más periféricos, la pared del vaso roza con el plasmay con los glóbulos rojos. Éstos forman “pilas”
Capilares, Menor velocidad mayor viscosidad

Abril 2006 58
Relación entre presión y flujo
120
100
80
60
40
20
Aorta Arteriolas Vénulas Vena Cava Arterias Capilares Venas
PmmHg

Abril 2006 59
Gracias por su atención