Proceso Isooctano_CSTR-Cinética de Reacción_Dic 01,2013
-
Upload
sin-nombre -
Category
Documents
-
view
75 -
download
0
Transcript of Proceso Isooctano_CSTR-Cinética de Reacción_Dic 01,2013

FP,1
FB,1
FnB,1
FP,2
FiB,2
FnB,2
FP,6
xP,1=0.08xB,1=0.8
FnB,7
FiO,8 = 918kmol/h
FD,9
xP,2=0.12xiB,2=0.73
PROBLEMA
Puede producirse isooctano usando la siguiente ruta de reacción:
R1 :Buteno+ Isobutano→Isooctano
R2 : Isooctano+Buteno→Dodecano
Las reacciones se llevan a cabo en fase líquida en un reactor tipo tanque que normalmente opera a 45°F y 90 psia. Se dispone de dos corrientes de alimentación fresca al proceso, con las siguientes composiciones: una corriente con 80% mol de buteno, 8% mol de propano y el resto de n-butano; mientras que la otra corriente contiene 73% mol de isobutano, 12% mol de propano y el resto de n-butano. Para un flujo de producción de isooctano de 918 kmol/hr:
a) Desarrolle una estructura de recirculación de este proceso.b) Para un reactor tipo tanque perfectamente mezclado, determine el modelo matemático
de la estructura de recirculación del proceso considerando la selectividad en términos de las constantes de reacción (velocidades de reacción) del sistema reaccionante.
c) Enuncie el algoritmo de solución de este problema.
Tb (°C) Códigos de DestinoPropano -42.1 Subproducto 1 Recirculación y Purga/Líq
Isobutano -11.92 Recirculación/Líq
Recirculación y Purga/Líq
Buteno -6.25 Recirculación/Líq
Recirculación y Purga/Líq
n-Butano -0.55 Subproducto 2 Recirculación y Purga/LíqIsooctano 113.44 Producto ProductoDodecano 216.23 Subproducto 3 Subproducto
MIX-1 RCT-1CSTR
SISTEMA DE SEPARACIÓN
1
2
3 4
6
5
9
7
8

BALANCES GLOBALESPropano :FP ,6=FP, 1+F P,2(1)Isobutano :0=F iB ,2−εR1(2)Buteno :0=FB,1−εR 1−εR2(3)n−Butano :FnB , 7=FnB ,1+FnB ,2(4 )Isooctano :F iO, 8=εR1−εR2(5)Dodecano :FD, 9=εR2(6)
Selectividad : S=F iO ,8
εR 1+εR 2(7)
DATOS:F iO ,8=918
kmolh
xP, 1=0.08xB, 1=0.8xP, 2=0.12x iB ,2=0.73
Dado que los datos incluyen las fracciones molares de las corrientes de alimentación, es necesario incluir en el modelo matemático del balance global las ecuaciones constitutivas de dichas corrientes:
CORRIENTE 1:xP, 1+ xB,1+xnB ,1=1 (8 )FP, 1=xP, 1F1(9)FB, 1=xB,1 F1(10)FnB ,1=xnB ,1 F1(11)
CORRIENTE 2:xP, 2+ xiB , 2+xnB , 2=1 (12 )FP, 2=xP, 2F2(13)F iB ,2=x iB ,2F2(14)FnB ,2=xnB , 2F2(15)
CONTEO DE VARIABLES: nvGRADOS DE LIBERTAD
F1, FP,1 , FB,1 ,FnB , 1 , xP, 1 , xB, 1 , xnB ,1 7 ngl=nv-ne
F2, FP, 2, FiB , 2, FnB ,2 , x P,2 , x iB ,2 , xnB ,2 7 ngl=21-15=6FP, 6 1
Estos 6 grados de libertad son los
datos del problema
FnB ,7 1F iO ,8 1FD ,9 1
Ɛ R1 , Ɛ R2 , S 321

Al realizar de nuevo el conteo de variables y ecuaciones considerando las expresiones (8) a (15), se observa que los grados de libertad del proceso global no cambian.
Como se verá más adelante, la sexta variable independiente es la conversión total del buteno (reactivo limitante) en el reactor. Además, hay dos variables independientes adicionales que es necesario especificar para poder resolver este problema: la temperatura de operación del reactor y la razón molar de isobutano a buteno a la entrada del reactor.
Balances de Materia en el Reactor (CSTR-1)
Buteno:
FB, 4=FB, 3−εR1−εR 2(16)
FB, 4=FB, 3−rR1V−r R2V
FB, 4=FB, 3−k R1CB,4C iB ,4V−kR 2CB, 4CiO , 4V
FB, 3−FB, 4=k R1CB,4C iB ,4V +k R2CB,4C iO ,4V
CB, 3q−CB, 4q=k R1CB ,4CiB , 4V +k R2CB ,4C iO, 4V
q=Flujo volumétrico [¿ ] m3
s
CB, 3q=FB, 3[¿ ]
kmol
m3∗m3
s[ ¿ ] kmol
s
Suposición :q3=q4=q ódensidad constante
τ= qV
CB, 3−CB, 4=1τ
[k R1CB ,4C iB ,4+kR2CB, 4C iO , 4 ](16a)
Isobutano:
F iB ,4=F iB ,3−εR1(17)
C iB ,3−C iB ,4=1τ
[k R1CB, 4CiB , 4 ](17a)

Isooctano:
F iO ,4=εR1−εR2(18)
C iO ,4=1τ
[kR 1CB, 4C iB , 4−k R2CB, 4C iO ,4 ](18a)
Dodecano:
FD ,4=εR2(19)
CD ,4=1τ
[kR 2CB, 4CiO , 4 ](19a)
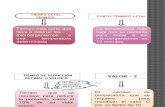
Para propósitos de cálculo, se define el rendimiento Y de sistema reaccionante en términos del producto obtenido y el isobutano consumido en el reactor:
Y=F iO ,8
F iB ,3−F iB ,4
=F iO, 4
F iB, 3−F iB ,4
=CiO , 4
CiB , 3−C iB, 4
(20)
(18a) y (17a) en (20)
CiO , 4
CiB ,3−CiB , 4
=kR 1CB, 4CiB , 4−kR2CB, 4C iO ,4
k R1CB ,4C iB ,4
=1−
k R2k R1
∗C iO ,4
C iB ,4
(20a)
Esta ecuación se puede rearreglar de la siguiente manera
CiO , 4
CiB ,3−CiB , 4
=1−KCiO , 4
C iB ,4
C iO ,4 [1+K (CiB ,3−CiB , 4 )C iB ,4
]=C iB ,3−C iB , 4
C iO ,4=C iB, 3−C iB ,4
1+K(CiB , 3−CiB , 4 )
C iB ,4
(20b)
donde
K=k R2k R1
(21)
La conversión del isobutano es dada por

X iB=C iB ,3−C iB ,4
C iB ,3
C iB ,4=(1−X iB)C iB ,3(22)
Combinando las ecuaciones (20b) y (22) se llega a
C iO ,4=X iBC iB ,3
1+K ( X iB
1−X iB)(20c)
La ecuación (18a) para el isooctano se puede manipular algebraicamente para obtener
C iO ,4=1τ [2kR1CB, 4C iB ,4−(k R1CB,4C iB ,4+kR 2CB, 4CiO , 4 ) ](18b)
De (16a) y (17a) se tiene que:
τ (CB, 3−CB, 4 )=k R1CB, 4CiB , 4+k R2CB ,4C iO ,4(16 b)
τ (C iB ,3−C iB ,4 )=kR1CB, 4C iB ,4 (17b)
Combinando las ecuaciones (16b), (17b) y (18b) se obtiene
C iO ,4=2 (C iB ,3−CiB , 4 )−(CB,3−CB ,4 )
CB, 3−CB, 4=2 (C iB ,3−C iB ,4 )−C iO, 4(18c )
Sustituyendo (20c) y (22) en (18c) se llega a
CB, 3−CB, 4=2 (C iB ,3 X iB )−X iBCiB ,3
1+K ( X iB
1−X iB)
CB, 3−CB, 4=C iB ,3 X iB [ (1−X iB )+2K X iB
(1−X iB )+K X iB ](18d)La conversión total del buteno se define como
X B=CB,3−CB, 4
CB,3
CB, 3−CB, 4=CB, 3 XB(23)

Sustituyendo (23) en (18d) se obtiene
CB, 3X B=C iB ,3 X iB [ (1−X iB )+2K X iB
(1−X iB )+K X iB ]X B=MR ∙X iB [ (1−X iB )+2K X iB
(1−X iB)+K X iB ](18e )donde
MR=CiB ,3
CB,3
(24)
Dado que MR ≥ 1, se deduce que el reactivo limitante es el buteno.
Rearreglando la ecuación (18e) se llega a
(2K−1 ) MR∙ (X iB )2+[MR−(K−1 ) ( XB ) ] ( X iB )−( XB )=0(18 f )
Para calcular la conversión del isobutano XiB de esta ecuación cuadrática, es necesario especificar los valores de tres variables independientes adicionales a las cinco variables especificadas previamente: la temperatura de la reacción (para calcular K), MR y la conversión total del buteno XB.